Clear Sky Science · de
Die Zielsetzung der mitochondrialen Phosphatase PGAM5 lindert Ferroptose und akute Pankreatitis durch Hochregulierung der NRF2-vermittelten FSP1-Expression
Warum gestresste Zellen und schmerzende Bauchspeicheldrüsen wichtig sind
Wenn Zellen zu stark belastet werden, können sie auf Weisen sterben, die dem gesamten Organismus schaden. Eine solche Form des Zelltods, genannt Ferroptose, wird durch Eisen und außer Kontrolle geratene chemische Reaktionen angetrieben, die die Fette in Zellmembranen „verrosten“ lassen. Dieser Prozess wurde mit Gewebeschäden in Verbindung gebracht, einschließlich einer schmerzhaften und mitunter tödlichen Erkrankung, der akuten Pankreatitis. Die Studie hinter diesem Artikel entdeckt einen wichtigen Schalter in den Mitochondrien — den Kraftwerken der Zelle — der die Ferroptose hoch- oder herunterregeln kann, und zeigt, wie das Blockieren dieses Schalters die Bauchspeicheldrüse in einem Mausmodell schützen kann.
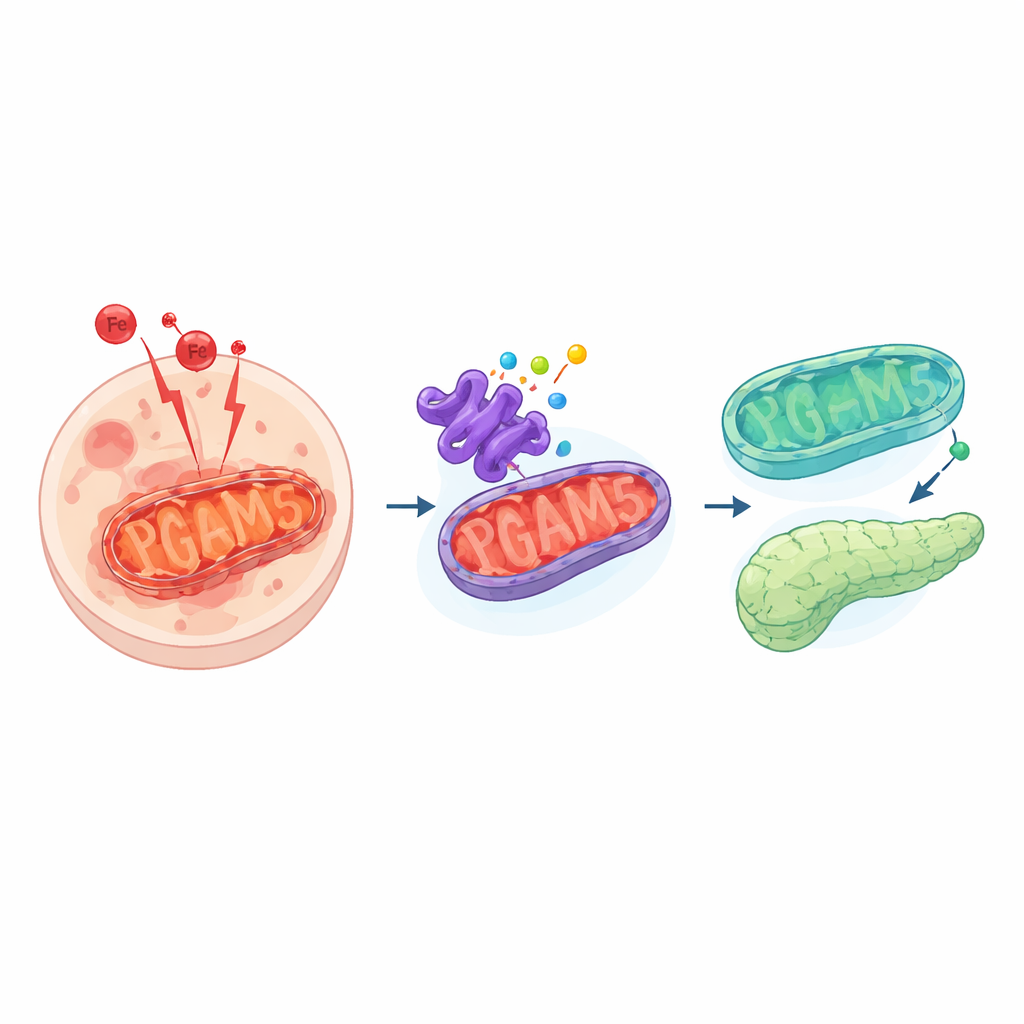
Eine gefährliche Form des Zelltods
Ferroptose unterscheidet sich von vertrauteren Formen des Zelltods wie der Apoptose. Statt einer ordentlichen Selbstzerstörung erleben Zellen bei Ferroptose einen Sturm eisengetriebener Reaktionen, die empfindliche Lipide in ihren Membranen verderben. Dabei entstehen toxische Nebenprodukte und Löcher in Membranen, die schließlich die Zelle töten. Normalerweise halten Schutzsysteme diese Prozesse im Zaum, indem sie reaktive Moleküle entgiften. Versagen diese Systeme oder sind sie überwältigt, kann sich Ferroptose durch Gewebe ausbreiten und zu Erkrankungen von Krebs bis zu Organversagen beitragen.
Ein mitochondrialer Schalter im Visier
Die Forschenden konzentrierten sich auf ein Protein namens PGAM5, das an der inneren Mitochondrienoberfläche sitzt und als Signalknotenpunkt fungiert. PGAM5 hilft, die Mitochondrienform zu steuern, reagiert auf Stress und beeinflusst, wie Zellen mit Oxidation umgehen. Überraschenderweise machten Zellen, bei denen PGAM5 entweder reduziert oder vermehrt vorhanden war, weniger anfällig für Ferroptose. Chemische Hemmung von PGAM5, genetische Herunterregulierung und Überexpression verringerten alle die Ansammlung schädlicher lipideller Nebenprodukte und reduzierte den Zelltod, der durch ein Ferroptose-induzierendes Mittel ausgelöst wurde. Das zeigt, dass das System fein austariert ist: Sowohl zu wenig als auch zu viel PGAM5 führen dazu, dass Zellen in einen geschützteren Zustand gelangen.
Aktivierung eines inneren Schutzschilds
Bei genauerer Untersuchung entdeckten die Autorinnen und Autoren, dass PGAM5 über eine Schutzachse wirkt, an der zwei weitere Akteure beteiligt sind: NRF2 und FSP1. NRF2 ist ein Masterregulator, der im aktiven Zustand im Zellkern eine breite Palette antioxidativer Abwehrmechanismen einschaltet. FSP1 ist einer seiner nachgeschalteten Verteidiger, der hilft, einen fettlöslichen Antioxidans zu regenerieren und so Lipid-Schäden an der Zellmembran verhindert. Wenn PGAM5-Spiegel verändert wurden, stiegen sowohl die mRNA- als auch die Proteinspiegel von NRF2, und NRF2 verlagerte sich leichter vom Zytoplasma in den Zellkern. Dort erhöhte es die Produktion von FSP1. Das Blockieren von FSP1 oder NRF2 nahm den Schutz weg und stellte die Empfindlichkeit gegenüber Ferroptose wieder her, was zeigt, dass die PGAM5–NRF2–FSP1-Kette für die beobachtete Widerstandsfähigkeit essentiell ist.
Energie- stress als versteckter Bote
Die Studie zeigte außerdem, wie mitochondrialer Stress in diese Schutzantwort übersetzt wird. Die Störung von PGAM5 brachte das mitochondriale Gleichgewicht durcheinander und verschob die Energiebilanz der Zelle: Das Verhältnis von niederenergetischen Molekülen (AMP und ADP) zu hochenergetischem ATP stieg, was auf Energiestress hinweist. Dies aktivierte wiederum die energie-sensierende Kinase AMPK. Aktiviertes AMPK modifizierte NRF2 direkt in einer Weise, die dessen Eintritt in den Kern förderte und so die FSP1-Produktion weiter erhöhte. Wurde AMPK aus dem System entfernt, sammelte sich NRF2 nicht mehr im Kern an, sanken die FSP1-Spiegel und die Zellen fielen erneut der Ferroptose zum Opfer. Damit verbindet PGAM5 den Zustand der Mitochondrien mit einer breiteren Energie- und Antioxidantienantwort, die Zellen vor dem eisengetriebenen Tod schützt.
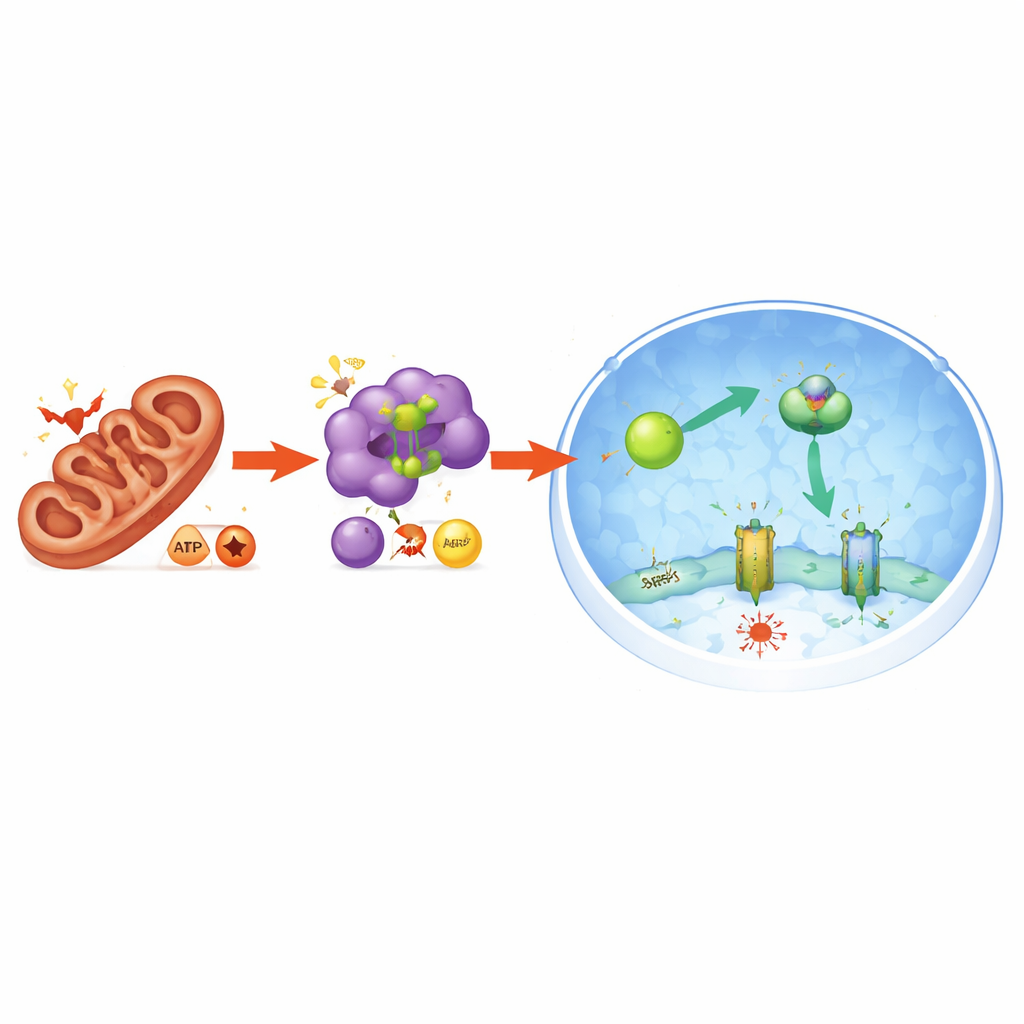
Schutz der Bauchspeicheldrüse in lebenden Tieren
Um zu prüfen, ob dieser Mechanismus in einem ganzen Organ relevant ist, nutzten die Forschenden ein Mausmodell der akuten Pankreatitis, das durch hohe Dosen der Aminosäure Arginin ausgelöst wird. In diesem Modell zeigt die Bauchspeicheldrüse umfangreiche Schäden, erhöhte Blutwerte von Enzymen, die Gewebeschädigung anzeigen, und einen Anstieg entzündlicher Moleküle. Marker der Lipidperoxidation — ein Kennzeichen der Ferroptose — stiegen ebenfalls stark in der Bauchspeicheldrüse an. Die Behandlung der Mäuse mit einem PGAM5-hemmenden Wirkstoff linderte diese Symptome: Blutmarker für Gewebeschädigung sanken, das Pankreasgewebe wirkte unter dem Mikroskop gesünder und entzündliche Signale nahmen ab. Gleichzeitig fielen die Ferroptose-Marker, während AMPK-Aktivität, NRF2- und FSP1-Spiegel in der Bauchspeicheldrüse zunahmen, was dem in Zellkulturen beobachteten Schutzweg entspricht.
Was das für künftige Therapien bedeutet
Zusammengefasst identifiziert die Arbeit PGAM5 als zentralen Kontrollpunkt, der mitochondrialen Stress, den zellulären Energiestatus und ein starkes antioxidatives Programm, das Ferroptose blockiert, miteinander verbindet. Durch das Herunterregeln der PGAM5-Aktivität aktivieren Zellen AMPK und NRF2, erhöhen FSP1 und widerstehen besser eisengetriebenen Lipidschäden. Bei Mäusen verringert diese Strategie die Schädigung der Bauchspeicheldrüse bei akuter Pankreatitis. Für Laien lautet die Botschaft, dass Forschende einen neuen internen „Sicherungsautomaten“ gefunden haben, der eine zerstörerische Form des Zelltods verhindern kann. Obwohl noch viel Arbeit nötig ist, bevor eine klinische Anwendung möglich ist, könnten das Anvisieren von PGAM5 oder seiner nachgeschalteten Partner neue Wege eröffnen, Erkrankungen zu behandeln, bei denen Ferroptose und mitochondriales Versagen eine schädliche Rolle spielen.
Zitation: Ma, S., Qin, J., Luan, J. et al. Targeting mitochondrial phosphatase PGAM5 alleviates ferroptosis and acute pancreatitis by upregulating NRF2-mediated FSP1 expression. Cell Death Dis 17, 252 (2026). https://doi.org/10.1038/s41419-026-08484-9
Schlüsselwörter: Ferroptose, Mitochondrien, akute Pankreatitis, oxidativer Stress, Zelltod