Clear Sky Science · de
Ein kleiner Molekülinhibitor des ARF-GTPase-Proteins 1 begrenzt das Wachstum und die Metastasierung von Leber- und Darmkrebszellen
Warum diese Forschung wichtig ist
Leber- und Darmtumoren gehören zu den tödlichsten Krebserkrankungen, und derzeitige Therapien verkleinern Tumoren oft auf Kosten schwerer Nebenwirkungen. Diese Studie untersucht eine neue Art von Wirkstoff, der nicht einfach schnell teilende Zellen vergiftet, sondern in Krebszellen eindringt und ein von ihnen abhängiges Protein‑„Steuerzentrum“ aufbricht. Indem die experimentelle Verbindung gezielt dieses Zentrum angreift, soll das Tumorwachstum gebremst werden, während gesundes Gewebe weitgehend geschont wird.
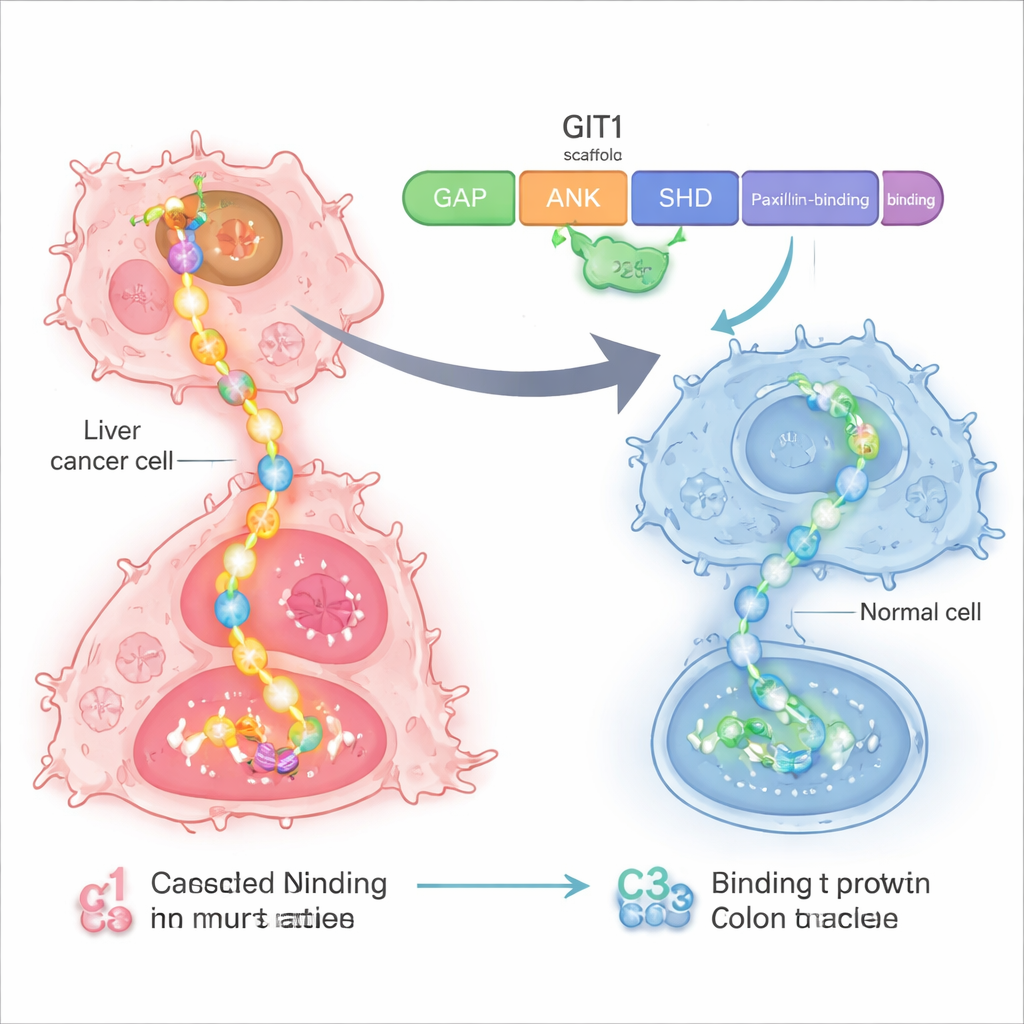
Ein verwundbares Steuerzentrum in Krebszellen
Die Forschenden konzentrierten sich auf ein Protein namens GIT1, das in Zellen als Gerüst oder Verteilerleiste fungiert. In Leber‑ und Darmtumoren werden GIT1 und sein Partnerprotein MAT2B überproduziert. Gemeinsam bauen sie mehrere Komponenten eines wichtigen Wachstumswegs zusammen, bekannt als RAS–RAF–MEK–ERK, einer Signalkette, die Zellen zur Teilung und Migration anregt. Frühere Arbeiten zeigten, dass Tumoren schneller wachsen und leichter metastasieren, wenn GIT1 und MAT2B in hoher Konzentration vorliegen, und dass das Tumorwachstum langsamer wird, wenn diese Proteine reduziert werden. Das machte das GIT1–MAT2B‑Gerüst zu einem attraktiven Ziel für eine präzisere Therapie.
Ein kleines Molekül ohne Bauplan entwerfen
Eine große Herausforderung war, dass die dreidimensionale Kristallstruktur von GIT1 nicht vorliegt, sodass das Team die Proteinform nicht einfach „nachschlagen“ konnte. Stattdessen nutzten sie Computermodelle, um die Struktur eines Bereichs von GIT1 vorherzusagen, der aus Ankyrin‑Repeats besteht und in der Nähe der Andockstellen von MAT2B und anderen Signalmolekülen liegt. Anschließend wurden virtuell umfangreiche Bibliotheken kleiner Moleküle gegen dieses Modell gescreent, um mögliche Bindungspartner zu identifizieren. Von neun in Zellen getesteten Kandidaten stach ein Molekül hervor – bezeichnet als Verbindung 3 (C3). C3 band spezifisch an GIT1, nicht aber an seinen nahen Verwandten GIT2, und reduzierte das ERK‑Aktivierungssignal in mehreren Krebszelllinien.
Krebszellen am Teilen und Ausbreiten hindern
Wenn Leber‑ und Darmkrebszellen mit C3 behandelt wurden, verlangsamte sich ihr Wachstum; bei höheren Dosen starben viele Zellen, während nicht‑krebserregende Leber‑ und Nierenzellen weitgehend unberührt blieben. C3 sorgte dafür, dass Krebszellen am Übergang zwischen G2‑ und M‑Phase des Zellzyklus steckenblieben – dem Kontrollpunkt kurz vor und während der Mitose, wenn sich eine Zelle in zwei Teile teilt. Die Verbindung verringerte außerdem stark die Fähigkeit von Krebszellen, Kolonien zu bilden und über eine Platte zu migrieren – zwei Labormessungen, die mit Tumornachsprossen und Metastasierung verbunden sind. Molekular gesehen schwächte C3 die Interaktionen zwischen GIT1, MAT2B und den RAF–MEK–ERK‑Signalkomponenten, was zu geringerer MEK‑ und ERK‑Aktivität und zu weniger des Zellzyklustreibers Cyclin D1 führte.
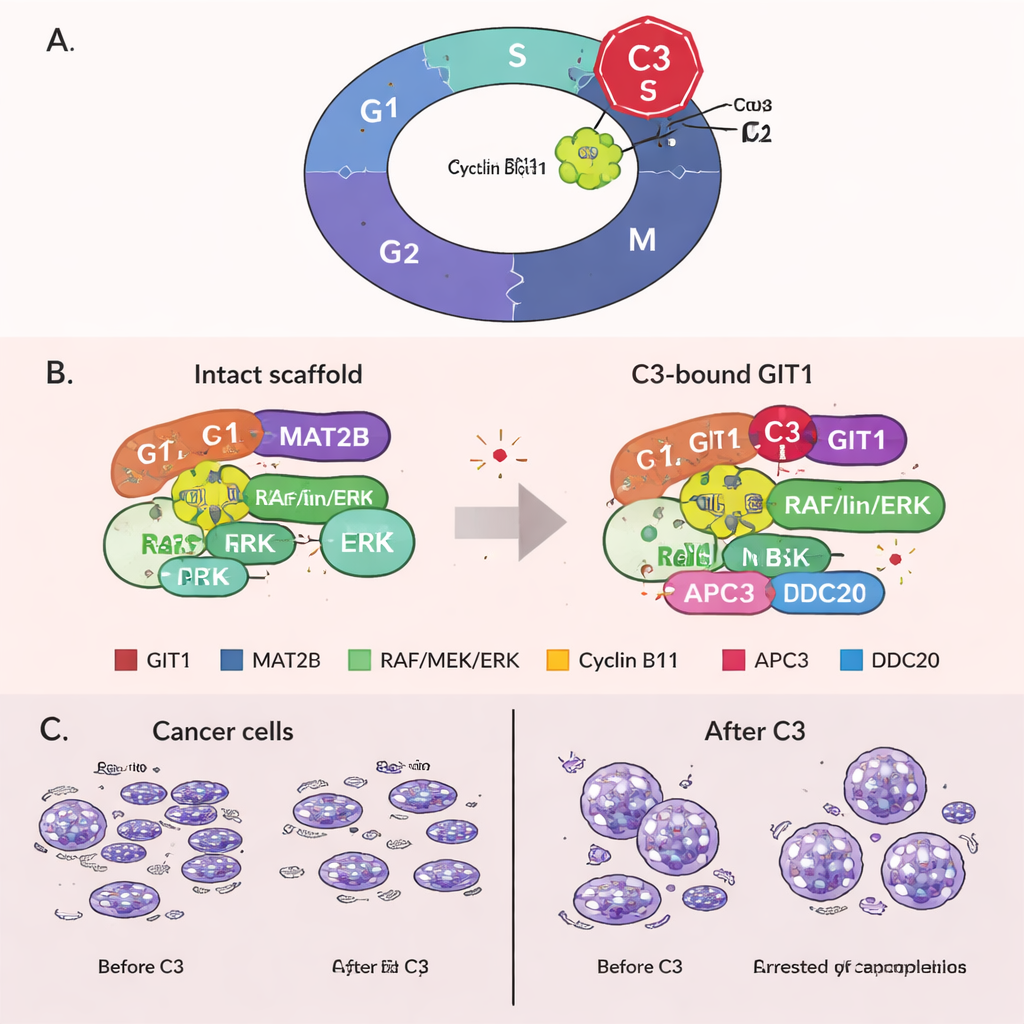
Zellen in der Mitose arretiert durch eine neu entdeckte Rolle von GIT1
Unerwartet entdeckte das Team eine neue Funktion von GIT1 bei den letzten Schritten der Zellteilung. Sie fanden, dass GIT1 an Cyclin B1 bindet, ein Protein, das Zellen in die Mitose treibt, und zudem an Teile einer Proteinanlage namens anaphase‑promoting complex (APC/C), die normalerweise Cyclin B1 markieren und abbauen lässt, damit Zellen die Mitose verlassen können. Die Behandlung mit C3 verstärkte die Bindung zwischen GIT1 und Cyclin B1, schwächte jedoch die Verbindungen zwischen GIT1, Cyclin B1 und APC/C‑Komponenten. Infolgedessen wurde Cyclin B1 nicht mehr effizient abgebaut, sein Spiegel blieb hoch, und die Zellen blieben in der Mitose stecken. Dieser verlängerte Arrest löst bekanntermaßen Zelltod aus und bietet einen zweiten Weg, auf dem C3 Krebszellen abtöten kann. Wichtig ist, dass bei experimenteller Reduktion von GIT1 C3 einen Großteil seiner Fähigkeit verlor, Cyclin B1 zu erhöhen, den Zellzyklus zu blockieren und Wachstum zu unterdrücken, was zeigt, dass seine Wirkungen tatsächlich GIT1‑abhängig sind.
Vielversprechende Ergebnisse in Tiermodellen
Die Forschenden testeten C3 anschließend in Mäusen, um zu prüfen, ob die Verbindung in lebenden Organismen wirkt. In immunkompetenten Mäusen mit implantierten kolorektalen Tumoren verlangsamten intratumorale Injektionen von C3 deutlich das Tumorwachstum, ohne offensichtliche Toxizität in wichtigen Organen. In zwei weiteren Modellen – humane Darmkrebszellen, die in die Leber immundefizienter Mäuse wuchsen, und Mauszellen eines Darmtumors, die sich in immunkompetenten Mäusen auf die Leber ausgebreitet hatten – reduzierte intraperitoneal verabreichtes C3 die Tumorlast und Anzeichen der Ausbreitung. Blutwerte und Gewebeuntersuchungen deuteten darauf hin, dass die Behandlungen gut vertragen wurden, und pharmakokinetische Studien zeigten, dass die Wirkstoffkonzentrationen im Blut mehrere Stunden nach der Gabe ausreichend hoch blieben.
Was das für künftige Krebstherapien bedeuten könnte
Für Nicht‑Spezialisten ist die wesentliche Botschaft, dass die Forschenden eine Möglichkeit gefunden haben, Krebs nicht durch das Anvisieren eines einzelnen mutierten Enzyms zu bekämpfen, sondern durch das Stören einer multi‑proteinen Assemblierung, auf die Krebszellen sowohl für Wachstums‑ als auch für Teilungssignale angewiesen sind. Ihr kleines Molekül C3 bindet spezifisch an GIT1, verändert dessen Netzwerk von Partnern, dämpft einen wichtigen Wachstumsweg und fängt Krebszellen in einem fatalen Stau während der Mitose ein. Obwohl C3 noch ein experimentelles Werkzeug und kein Patientenmedikament ist, zeigt die Arbeit, dass das Anvisieren von Gerüstproteinen wie GIT1 einen neuen Weg für die Behandlung von Leber‑ und Darmkrebs mit größerer Präzision und möglicherweise weniger Nebenwirkungen eröffnen kann.
Zitation: Peng, H., Chhimwal, J., Fan, W. et al. A small molecule inhibitor of ARF GTPase protein 1 limits liver and colon cancer cell growth and metastasis. Cell Death Dis 17, 238 (2026). https://doi.org/10.1038/s41419-026-08477-8
Schlüsselwörter: Leberkrebs, Darmkrebs, zielgerichtete Therapie, Zellzyklusarrest, Gerüstprotein