Clear Sky Science · de
Die Hemmung des Colony‑stimulating factor 1‑Rezeptors ist neuroprotektiv für Photorezeptoren bei Netzhautablösung
Warum diese Forschung für das Sehvermögen wichtig ist
Eine Netzhautablösung ist ein Notfall, der das Sehvermögen auch nach einer erfolgreichen operativen Wiederanlagerung noch beeinträchtigen kann. Ein großer Teil dieses bleibenden Schadens stammt von der körpereigenen Aufräumtruppe aus Immunzellen, die beim Versuch zu helfen lichtempfindliche Zellen schädigen können. Diese Studie an Mäusen untersucht, ob das Herunterregeln eines zentralen Immun‑Schalters, des CSF1R, diese empfindlichen Photorezeptoren schützen und einen neuen Weg eröffnen kann, das Sehvermögen zu erhalten.
Die Aufräumtruppe des Auges und wie sie sich rächen kann
Wenn sich die Netzhaut von ihrer Stützschicht löst, verlieren Photorezeptoren plötzlich den Zugang zu Sauerstoff und Nährstoffen. Viele dieser Zellen sterben, und das Gewebe sendet Alarmzeichen aus. Lokale Immunzellen in der Netzhaut, bekannt als Mikroglia, verändern ihre Gestalt, wandern zur Verletzung und verstärken ihre Phagozytose von Trümmern. Gleichzeitig strömen Immunzellen aus dem Blut, darunter verschiedene Monozyten‑Typen, in die Netzhaut ein. Gemeinsam versuchen sie, tote Zellen zu räumen und die Reparatur einzuleiten. Diese hilfreiche Reaktion kann jedoch über das Ziel hinausschießen und zu zusätzlicher Entzündung führen, die weitere, noch lebensfähige Photorezeptoren tötet und den Sehverlust verschlimmert.
Ein Medikament, das einen gemeinsamen Immun‑Schalter anvisiert
Sowohl die ansässigen Mikroglia als auch die einströmenden Monozyten sind für ihr Überleben und ihre Funktion auf denselben Oberflächenrezeptor CSF1R angewiesen. Die Forschenden setzten PLX5622 ein, eine oral verabreichte Substanz, die CSF1R blockiert, um zu untersuchen, wie das Eingreifen in diesen Schalter das Immunverhalten bei Netzhautablösung verändert. Zunächst kartierten sie die Effekte im Blut und in der Netzhaut. In der Zirkulation veränderte die kurze Behandlung nicht die Gesamtzahl der Monozyten, verschob jedoch deren Untergruppen: proinflammatorische „klassische“ Monozyten nahmen zu, während patrouillierende „nicht‑klassische“ Monozyten abnahmen. Im Auge räumte PLX5622 die retinalen Mikroglia effizient aus und veränderte sowohl die Anzahl der aus dem Blut eingewanderten Immunzellen als auch die Formen und Verhaltensweisen, die diese annahmen.
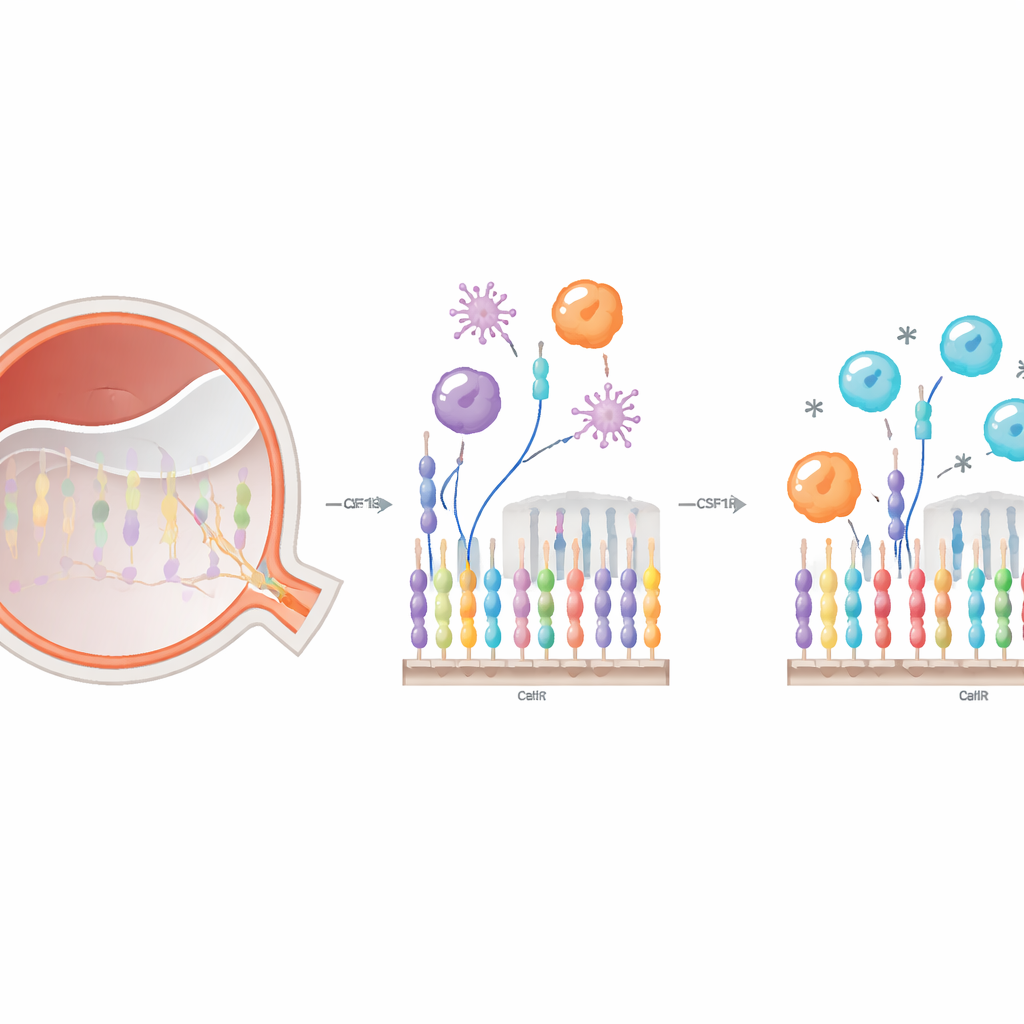
Lokale und eintreffende Zellen mithilfe von Farbmarkern verfolgen
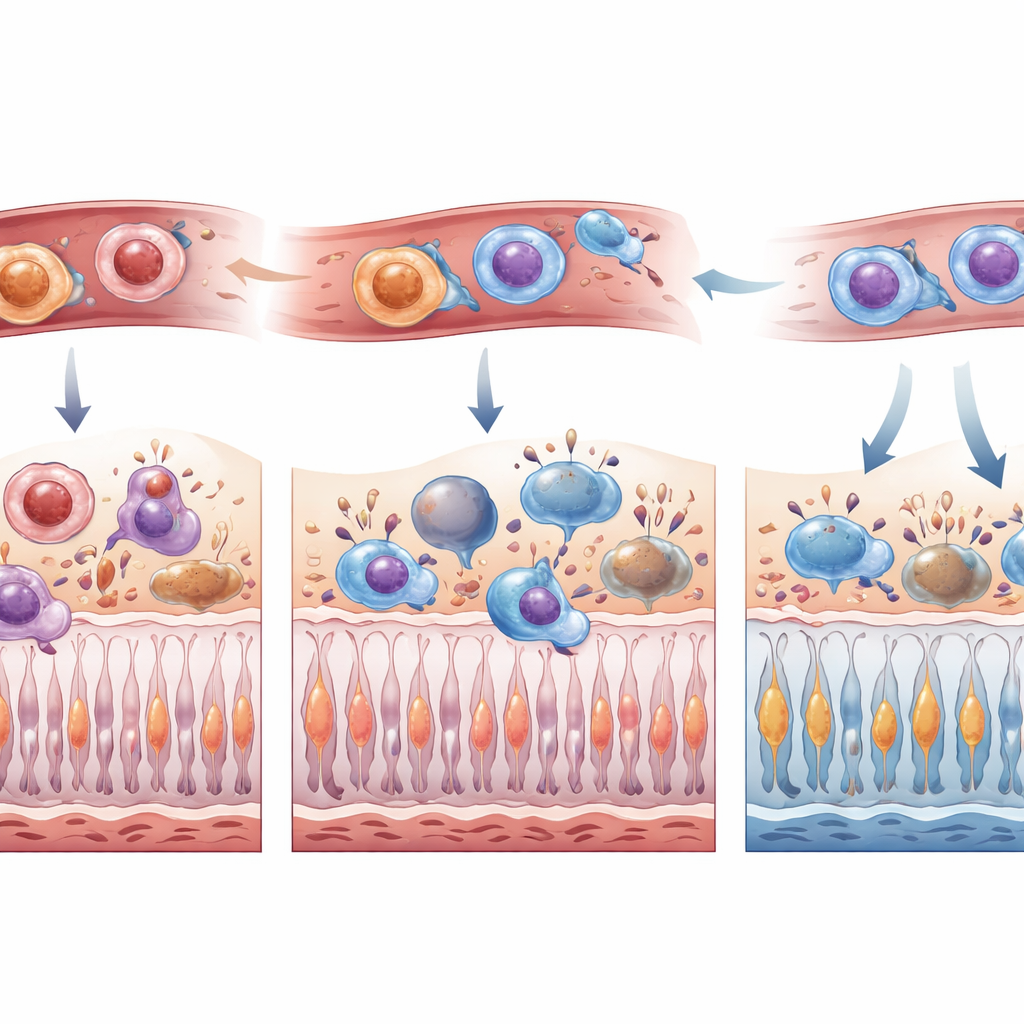
Weil Mikroglia und infiltrierende Monozyten, sobald sie in die Netzhaut eingedrungen sind, sehr ähnlich aussehen können, erzeugte das Team ein zweifarbig markiertes Maussystem: Ansässige Mikroglia leuchteten in einer Farbe, knochenmarkabgeleitete Zellen in einer anderen. Nach Auslösen einer kontrollierten Netzhautablösung verfolgten sie, wohin diese Zellen in der ersten Woche wanderten und wie sie sich veränderten. Ohne Behandlung sammelten sich Mikroglia vor allem in den oberen Netzhautschichten an, während knochenmarkabgeleitete Zellen besonders in den subretinalen Raum eindrangen und häufig eine amöboide, stark phagozytische Gestalt annahmen. Unter CSF1R‑Hemmung waren Mikroglia frühzeitig in allen Schichten deutlich reduziert, und weniger knochenmarkabgeleitete Zellen, insbesondere der amöboide Typ, erreichten die Netzhaut in den ersten Tagen nach der Verletzung. Bis Tag sieben hatte die Welle einströmender Zellen größtenteils aufgeholt, was darauf hindeutet, dass die CSF1R‑Blockade ihre Ankunft verzögert, aber nicht dauerhaft verhindert.
Wie das Verschieben des Immungleichgewichts lichtempfindliche Zellen schützt
Um zu verstehen, was diese Immunverschiebungen für das Sehen bedeuten, zählten die Forschenden sterbende und überlebende Photorezeptoren zu mehreren Zeitpunkten. In den frühen Stunden nach der Ablösung hatten Tiere unter PLX5622 weniger sterbende Photorezeptoren und mehr überlebende Zellen. Nach einer Woche bewahrten sowohl eine kurze Vorbehandlung als auch eine kontinuierliche Behandlung die Dicke der Photorezeptorschicht, ein strukturelles Maß für Zellüberleben, und reduzierten die Präsenz von Immunzellen im subretinalen Raum. Detaillierte immunologische Profilierungen zeigten, dass trotz eines insgesamt geringeren Einstroms infiltrierender Leukozyten diejenigen, die unter CSF1R‑Hemmung in die Netzhaut eintraten, tendenziell ein stärkeres proinflammatorisches Profil trugen. Die Autorinnen und Autoren schlagen vor, dass diese Kombination – weniger Zellen, aber stärker auf schnelle Trümmerbeseitigung ausgerichtet – das sichere Entfernen sterbender Photorezeptoren beschleunigen kann, während noch gesunde Nachbarzellen geschont werden.
Was das für künftige Behandlungen bedeuten könnte
Diese Arbeit zeigt, dass ein systemischer CSF1R‑Inhibitor sowohl lokale als auch zirkulierende Immunantworten bei Netzhautablösung umgestalten kann und, etwas kontraintuitiv, dass eine kleinere, aber stärker entzündungsbereite Aufräumtruppe das Sehvermögen schützen kann. Durch die vorübergehende Dezimierung der Mikroglia, das Verzögern des ersten Ansturms blutabgeleiteter Zellen und die Verschiebung von Monozyten‑Untertypen schuf PLX5622 ein Zeitfenster, in dem frühe immunvermittelte Schäden reduziert wurden und mehr Photorezeptoren überlebten. Da die Studie an Mäusen durchgeführt wurde und das Verhältnis von hilfreicher zu schädlicher Entzündung je nach Augenerkrankung variiert, stützen diese Befunde jedoch die CSF1R‑Hemmung als vielversprechenden Ausgangspunkt für Medikamente, die die Immunantwort feinjustieren und das Sehvermögen nach Netzhautverletzung erhalten sollen.
Zitation: Pastor-Puente, S., Jung, R., Gonzalez-Buendia, L. et al. Colony-stimulating factor 1 receptor inhibition is neuroprotective to photoreceptors in retinal detachment. Cell Death Dis 17, 264 (2026). https://doi.org/10.1038/s41419-026-08470-1
Schlüsselwörter: Netzhautablösung, Mikroglia, Überleben der Photorezeptoren, Neuroinflammation, CSF1R‑Hemmung