Clear Sky Science · de
Umschaltung des Schicksals von Melanomzellen: TRPM8-Modulatoren lösen Apoptose aus und steigern die Zytotoxizität von NK-Zellen
Warum es wichtig ist, einen „Kältesensor“ gegen Hautkrebs einzusetzen
Melanom ist eine gefährliche Form von Hautkrebs, die häufig lernt, sowohl Medikamenten als auch dem Immunsystem auszuweichen. Diese Studie untersucht eine unerwartete Schwachstelle in Melanomzellen: ein Protein namens TRPM8, das vor allem als Sensor bekannt ist, der Nervenzellen Kälte oder Menthol spüren lässt. Die Forschenden zeigen, dass sorgfältig entwickelte Wirkstoffe, die TRPM8 blockieren, Melanomzellen zur Selbstzerstörung treiben und sie gleichzeitig für natürliche Killerzellen (NK-Zellen) leichter angreifbar machen. Diese doppelte Wirkung deutet auf einen neuen Ansatz zur Behandlung hartnäckiger, fortgeschrittener Melanome hin.
Ein verborgener Schalter auf Melanomzellen
Durch Auswertung großer Krebsdatenbanken und Untersuchung patientenabgeleiteter Melanomzellen im Labor stellte das Team fest, dass TRPM8 in metastasierendem Melanom deutlich stärker vorhanden ist als in normaler Haut, einschließlich gesunder Melanozyten und dermaler Fibroblasten. Mit bildgebenden Verfahren zeigten sie, dass TRPM8 sowohl auf der Zelloberfläche als auch auf inneren Membranen sitzt, wodurch es an strategischen Stellen Zellverhalten beeinflussen kann. Als sie eine Reihe neuer TRPM8‑wirksamer Moleküle testeten, stachen zwei Verbindungen (bezeichnet als 4 und 9) konstant hervor: Sie verringerten über die Zeit deutlich das Überleben von Melanomzellen, während normale Hautzellen weitgehend verschont blieben. Genetische Tests bestätigten, dass die Wirkstoffe ihre Tötungswirkung verloren, wenn TRPM8 entfernt wurde, und dass eine Erhöhung von TRPM8 die Melanomzellen noch empfindlicher machte — ein Beleg dafür, dass der Effekt von genau diesem Kanal abhängt. 
Kreieren einer Energiekrise in Krebszellen
Im Gegensatz zu klassischen TRPM8‑Aktivatoren wie Menthol, die einen Kalziumeinstrom in Zellen auslösen, verursachten diese neuen Blocker keine Kalziumveränderungen. Stattdessen lösten sie eine Welle von oxidativem Stress in Melanomzellen aus. Die Verbindungen erhöhten schnell reaktive Sauerstoffspezies, insbesondere in den Mitochondrien, den Energiezentralen der Zelle. Dieser oxidative Ausbruch brachte die Mitochondrien dazu, ihr elektrisches Potenzial zu verlieren, sich zu fragmentieren und Cytochrom c freizusetzen — ein entscheidender Schritt zur Aktivierung des inneren „Selbstmord“-Programms der Zelle. Antioxidantien, die diese reaktiven Moleküle neutralisierten, retteten die Zellen größtenteils, was zeigt, dass das Redox‑Ungleichgewicht nicht nur ein Nebeneffekt, sondern der Motor des Zelltods ist. Weiter downstream bestätigten klassische Todesmarker wie die Aktivierung von Caspase‑3 und PARP‑Spaltung, dass die Zellen programmierte Apoptose und keine zufällige Schädigung durchliefen.
Entwaffnen von Überlebenssignalen und Aktivierung einer Wächterfunktion
Der oxidative Schlag löste eine breitere Stressantwort aus. Die Wirkstoffe aktivierten ATM, einen Sensor für DNA‑Schäden, und führten zum Aufbau und zur Aktivierung von p53, einem bekannten Tumorsuppressorprotein, das entscheidet, ob sich eine geschädigte Zelle repariert oder stirbt. Gleichzeitig schwächten die Verbindungen einen der wichtigsten Überlebenswege des Melanoms: den PI3K–AKT‑Signalweg. Normalerweise interagiert TRPM8 physisch mit PI3K‑Bestandteilen, um AKT in seiner aktiven, wachstumsfördernden Form zu halten. Nach der Behandlung löste sich dieses Zusammenspiel auf und die AKT‑Aktivität sank, wodurch das Gleichgewicht weiter zugunsten des Zelltods kippte. Wichtig ist, dass diese Veränderungen in Melanomzellen ausgeprägt waren, in nicht‑kanzerösen Zellen jedoch kaum, was ein therapeutisches Fenster nahelegt, in dem der Tumor stark getroffen wird, während gesundes Gewebe geschont bleibt.
Tumoren für Immun‑„Einsatztruppen“ sichtbarer machen
Die Gefahr des Melanoms liegt auch in seiner Fähigkeit, der Immunüberwachung zu entkommen. Die Forschenden fragten daher, was mit Tumorzellen passiert, die niedrige Dosen der TRPM8‑Blocker über längere Zeit überleben. Sie entdeckten, dass diese verbliebenen Zellen vermehrt ein Oberflächenmarker namens ULBP1 zeigten, der wie eine Hilfsfahne wirkt und von NKG2D‑Rezeptoren auf NK‑Zellen erkannt wird. Andere verwandte Marker änderten sich nicht, was auf einen selektiven Effekt hinweist. In dreidimensionalen Melanom‑Sphäroiden, die echte Tumoren besser nachahmen, verkleinerte die Vortreatment mit TRPM8‑Blockern nicht nur die Strukturen und erhöhte den Zelltod, sondern machte sie auch deutlich anfälliger für NK‑Zell‑Angriffe. Wurde ULBP1 oder NKG2D mit Antikörpern blockiert, verschwand dieser zusätzliche Zelltod größtenteils, sodass die verbesserte Immun‑Elimination auf diesem spezifischen Zusammenspiel zwischen Tumor und NK‑Zellen beruht. 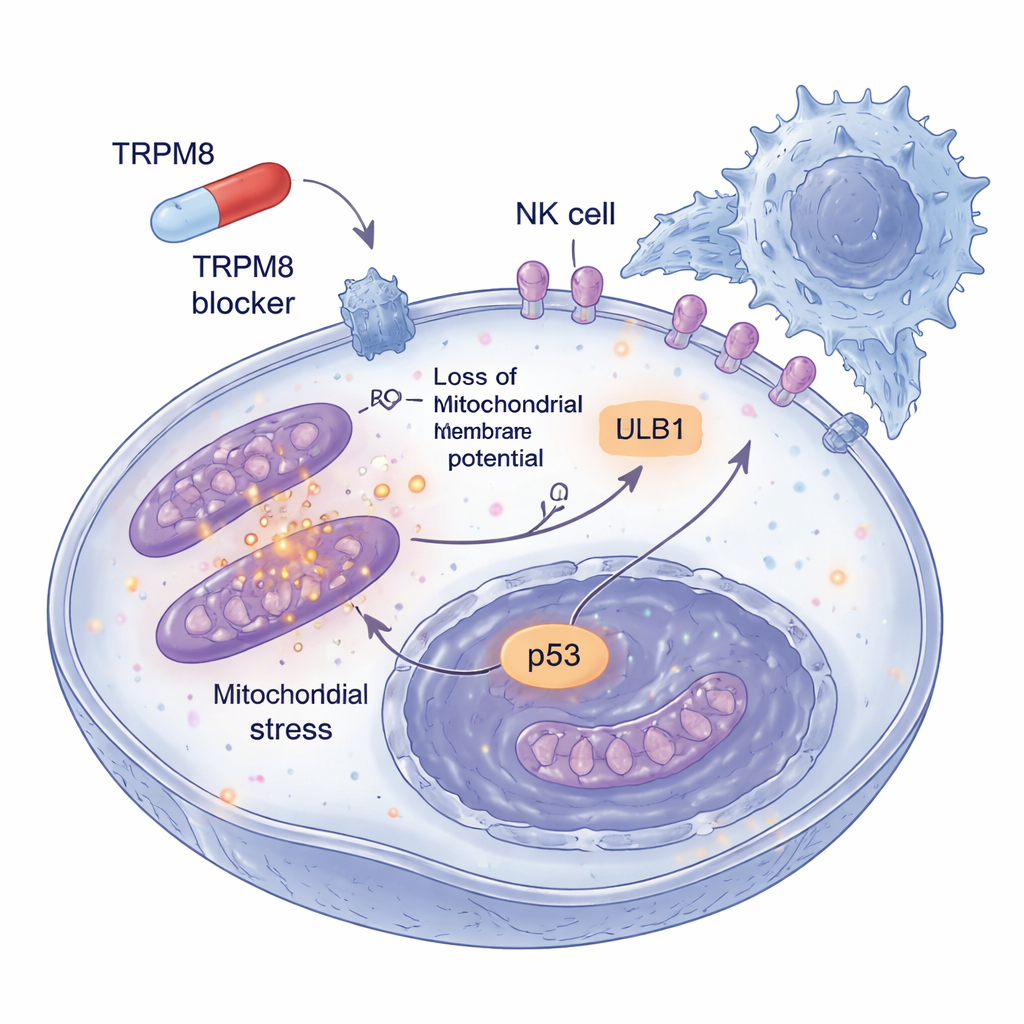
Was das für die künftige Melanomversorgung bedeuten könnte
Einfach gesagt macht die Blockade des TRPM8‑„Kältesensors“ ihn zu einem therapeutischen Hebel: Sie treibt Melanomzellen in eine tödliche mitochondriale und DNA‑Krise und markiert sie gleichzeitig für die Zerstörung durch NK‑Zellen. Da die Wirkstoffe normale Hautzellen verschonen und NK‑Zellen selbst nicht schädigen, bieten sie eine vielversprechende Grundlage für neue Behandlungen. Die Autorinnen und Autoren schlagen vor, TRPM8‑Blocker mit bestehenden Immuntherapien zu kombinieren, um fortgeschrittenes, medikamentenresistentes Melanom zweigleisig anzugehen: direkte Abtötung von Tumorzellen und bessere Auffindbarkeit und Eliminierung der Überlebenden durch das Immunsystem.
Zitation: Sorrentino, C., Lauretta, C., D’Angiolo, R. et al. Rewiring melanoma cell fate: TRPM8 modulators trigger apoptosis and boost NK cell cytotoxicity. Cell Death Dis 17, 223 (2026). https://doi.org/10.1038/s41419-026-08469-8
Schlüsselwörter: Melanom, TRPM8, Mitochondrien, oxidativer Stress, natürliche Killerzellen