Clear Sky Science · de
Lactylierungsgetriebenes TRIM29 fördert invasives Verhalten und Lymphknotenmetastasen beim Magenkrebs über den hnRNPA1-vermittelten Wnt/β-Catenin-Weg
Warum diese Forschung wichtig ist
Magenkrebs gehört zu den tödlichsten Krebsarten weltweit, vor allem weil er früh in nahegelegene Lymphknoten streut und damit eine Heilung durch Operation erschwert. Diese Studie zeigt, wie eine chemische Modifikation, die mit dem Tumormetabolismus verknüpft ist, das Protein TRIM29 auflädt und dadurch Krebszellen dabei unterstützt, in umliegendes Gewebe einzudringen, neue Lymphgefäße zu bilden und Chemotherapie zu widerstehen. Das Verständnis dieser Kausalkette weist auf neue Ansätze hin, das Fortschreiten von Magenkrebs zu verlangsamen oder zu blockieren.
Eine gefährliche Partnerschaft in Magenstumoren
Die Forschenden begannen mit dem Vergleich von Magenkrebsproben und benachbartem gesundem Gewebe von 100 Patient:innen sowie mit großen öffentlichen Gen-Datenbanken. Sie stellten fest, dass TRIM29, ein Protein, das zuvor mit Immunregulation und anderen Krebsarten in Verbindung gebracht wurde, in Tumorzellen durchgängig erhöht war. Patient:innen mit höheren TRIM29-Werten in ihren Tumoren zeigten häufiger Befall von Lymph- und Blutgefäßen und hatten eine schlechtere Gesamtüberlebensrate. Diese Befunde legen nahe, dass TRIM29 nicht nur vorhanden ist, sondern aktiv dazu beiträgt, dass Magenkrebs aggressiver auftritt.
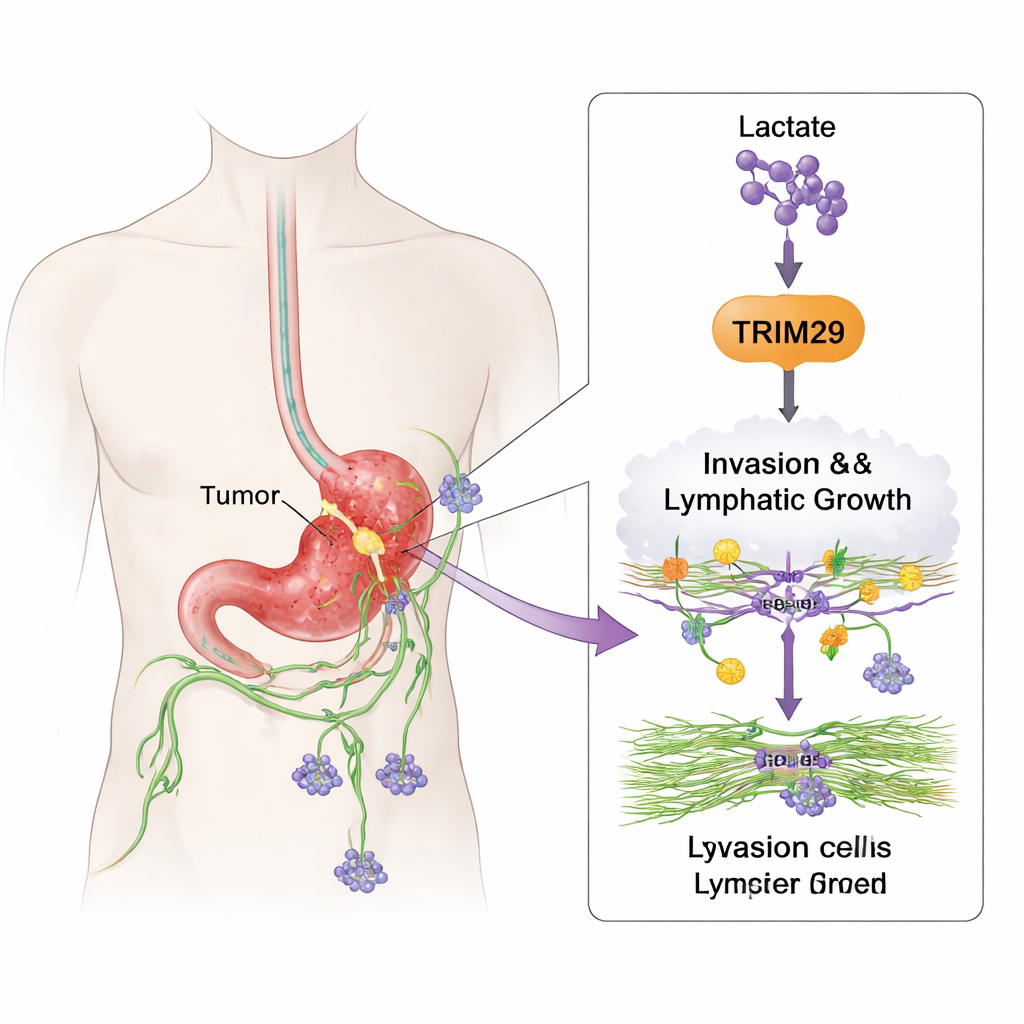
Wie Krebszellen das Reisen lernen
Um die Funktion von TRIM29 zu untersuchen, veränderte das Team dessen Expression in Magenkrebszelllinien. Bei Reduktion von TRIM29 wurden die Zellen deutlich weniger mobil und weniger fähig, sich durch 3D‑Gele zu bewegen, die Körpergewebe nachahmen. Eine Erhöhung von TRIM29 hatte den gegenteiligen Effekt und machte die Zellen invasiver. Die Forschenden untersuchten außerdem lymphatische Endothelzellen, die die Lymphgefäße auskleiden. TRIM29‑reiche Krebszellen förderten das Aussprossen und die Ausbildung röhrenförmiger Strukturen dieser Gefäßzellen, ein Zeichen für Lymphangiogenese. In Mausmodellen bildeten Tumoren mit hohem TRIM29 mehr Leber‑ und Lymphknotenmetastasen, während Tumoren mit reduziertem TRIM29 weniger streuten und weniger lymphatische Gefäße entwickelten.
Molekularer Staffellauf: Schutz eines Schlüsselregulators
Tiefer gehend entdeckten die Wissenschaftler:innen, dass TRIM29 physisch an ein anderes Protein, hnRNPA1, bindet, das die Genverarbeitung beeinflusst und mit Krebsstreuung assoziiert ist. Normalerweise kann hnRNPA1 von einem weiteren Protein, dem Enzym ZFP91, zum Abbau markiert werden, über das zelluläre Recycling‑System. TRIM29 stört diesen Prozess, indem es mit ZFP91 um die Bindung an hnRNPA1 konkurriert. Bei hoher TRIM29‑Konzentration schützt es hnRNPA1 davor, markiert und abgebaut zu werden. Dadurch wird hnRNPA1 stabiler und reichert sich in Krebszellen an, was eine Signalkaskade auslöst, die in der Aktivierung des Wnt/β‑Catenin‑Wegs mündet — ein bekannter Treiber für Tumorwachstum und Zellbewegung. Dies steigert wiederum die Produktion von VEGF‑C, einem Molekül, das neue Lymphgefäße stimuliert und den Krebszellen mehr „Wege“ zum Ausbreiten bietet.
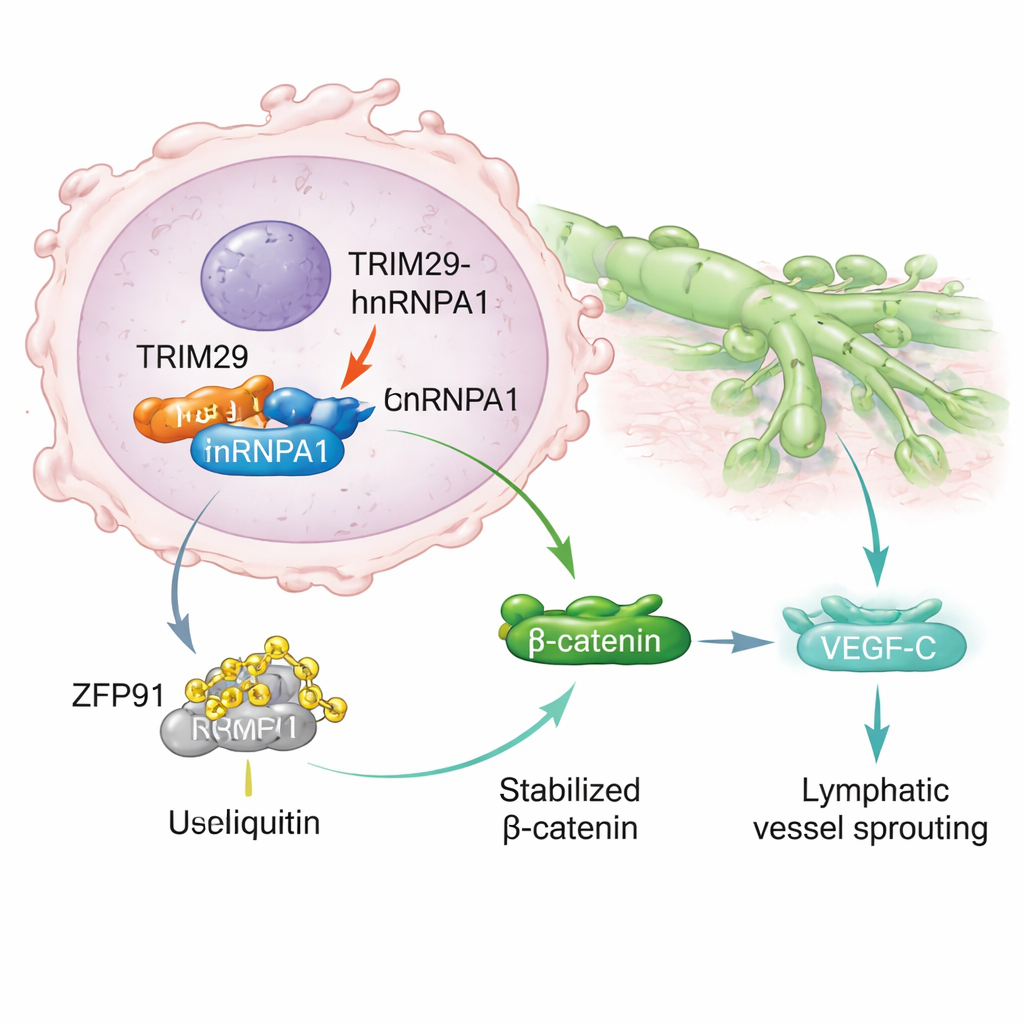
Krebs mit Laktat befeuern
Die Studie verbindet dieses invasive Verhalten zudem mit der Art und Weise, wie Tumoren Zucker verstoffwechseln. Rasch wachsende Tumoren nutzen oft Stoffwechselwege, die große Mengen Laktat produzieren — ein Nebenprodukt, das früher als bloßer Abfall galt. Die Autor:innen zeigen hier, dass Laktat histonische Proteine chemisch modifizieren kann, die die DNA verpacken, insbesondere an der Stelle H3K9. Diese „Lactylierung“ wirkt wie ein Einschalter für das TRIM29‑Gen und erhöht dessen Aktivität. Verringerten sie die Laktatproduktion mit Stoffwechselhemmern, fielen die TRIM29‑Spiegel; erhöhten sie Laktat, stieg TRIM29. Magenkrebsgewebe von Patient:innen wies höhere H3K9‑Lactylierung auf, die mit erhöhtem TRIM29, mehr Lymphknotenbefall und schlechterem Überleben korrelierte. Im Kern hilft der veränderte Tumormetabolismus, ein aggressiveres genetisches Programm zu schreiben.
Neue Wege, die Chemotherapie zu verstärken
Lymphgefäße transportieren nicht nur Krebszellen, sie können auch Chemotherapeutika aus Tumoren abführen. An patient:innenabgeleiteten Tumorimplantaten in Mäusen testeten die Forschenden, ob die Hemmung von TRIM29 und der Lymphgefäßbildung die Wirkung von 5‑Fluorouracil (5‑FU), einem Standardmedikament gegen Magenkrebs, verbessern könnte. Die Inhibition von TRIM29 oder die Blockade der Lymphangiogenese machte jeweils 5‑FU wirksamer beim Schrumpfen der Tumoren und bei der Reduktion der Zellteilung. Die Kombination beider Strategien erzeugte die stärkste Wirkung, was auf einen möglichen Weg hinweist, bestimmte Formen der Arzneimittelresistenz im fortgeschrittenen Stadium zu überwinden.
Was das für Patient:innen bedeutet
Diese Arbeit zeichnet eine schrittweise Abfolge: Magenstumoren erzeugen überschüssiges Laktat, das TRIM29 einschaltet; TRIM29 schützt dann hnRNPA1, stabilisiert einen Wachstumsweg und erhöht die Bildung lymphatischer Gefäße und die Ausbreitung in Lymphknoten. Klinisch identifizieren hohe TRIM29‑Werte und zugehörige Lactylierungsmarker Patient:innen mit höherem Risiko für aggressiven Verlauf. In Zukunft könnten Wirkstoffe, die Laktat‑Signale dämpfen, TRIM29 blockieren oder die Lymphgefäßbildung verhindern, mit bestehender Chemotherapie kombiniert werden, um die Metastasierung von Magenkrebs zu reduzieren und Therapien wirkungsvoller zu machen.
Zitation: Hua, R., Yu, J., Niu, Y. et al. Lactylation-drived TRIM29 induces invasive behavior and lymph node metastasis in gastric cancer via hnRNPA1-mediated Wnt/β-catenin pathway. Cell Death Dis 17, 222 (2026). https://doi.org/10.1038/s41419-026-08468-9
Schlüsselwörter: Metastasierung von Magenkrebs, TRIM29, Laktat und Lactylierung, Lymphangiogenese, Wnt‑Beta‑Catenin‑Signalweg