Clear Sky Science · de
KIF20A hemmt die TRIM21‑abhängige Ubiquitinierung von DHX9, um die Stabilität von SOX2 zu erhöhen, wodurch die Stammzell-Eigenschaften und Ferroptose-Resistenz von OSCC verstärkt werden
Warum diese Forschung für Mundkrebspatienten wichtig ist
Das Plattenepithelkarzinom der Mundhöhle, eine häufige Form von Mundkrebs, tritt oft wieder auf und zeigt Therapieresistenz. Viele Misserfolge von Operation, Chemotherapie und Strahlentherapie lassen sich auf eine kleine, hartnäckige Population von „Krebsstammzellen“ zurückführen, die den Tumor erneut aufbauen und dem Zelltod widerstehen können. Diese Studie enthüllt einen wichtigen molekularen Regelkreis, der diesen Zellen hilft, zu überleben und einer neueren Form des Zelltods, der Ferroptose, zu widerstehen, und weist auf eine Medikamentenstrategie hin, die die Wirksamkeit der Standardchemotherapie verbessern könnte.
Ein verborgener Treiber in Mundtumoren
Die Forschenden begannen mit dem Vergleich von Tumorproben von Mundkrebspatienten mit dem umliegenden gesunden Gewebe. Sie stellten fest, dass ein Protein namens KIF20A in Krebszellen durchgehend deutlich erhöht war. In größeren Patientenkohorten zeigten Menschen mit Tumoren, die mehr KIF20A aufwiesen, tendenziell eine kürzere Überlebenszeit, was darauf hinweist, dass dieses Protein mit aggressiver Krankheit assoziiert ist. 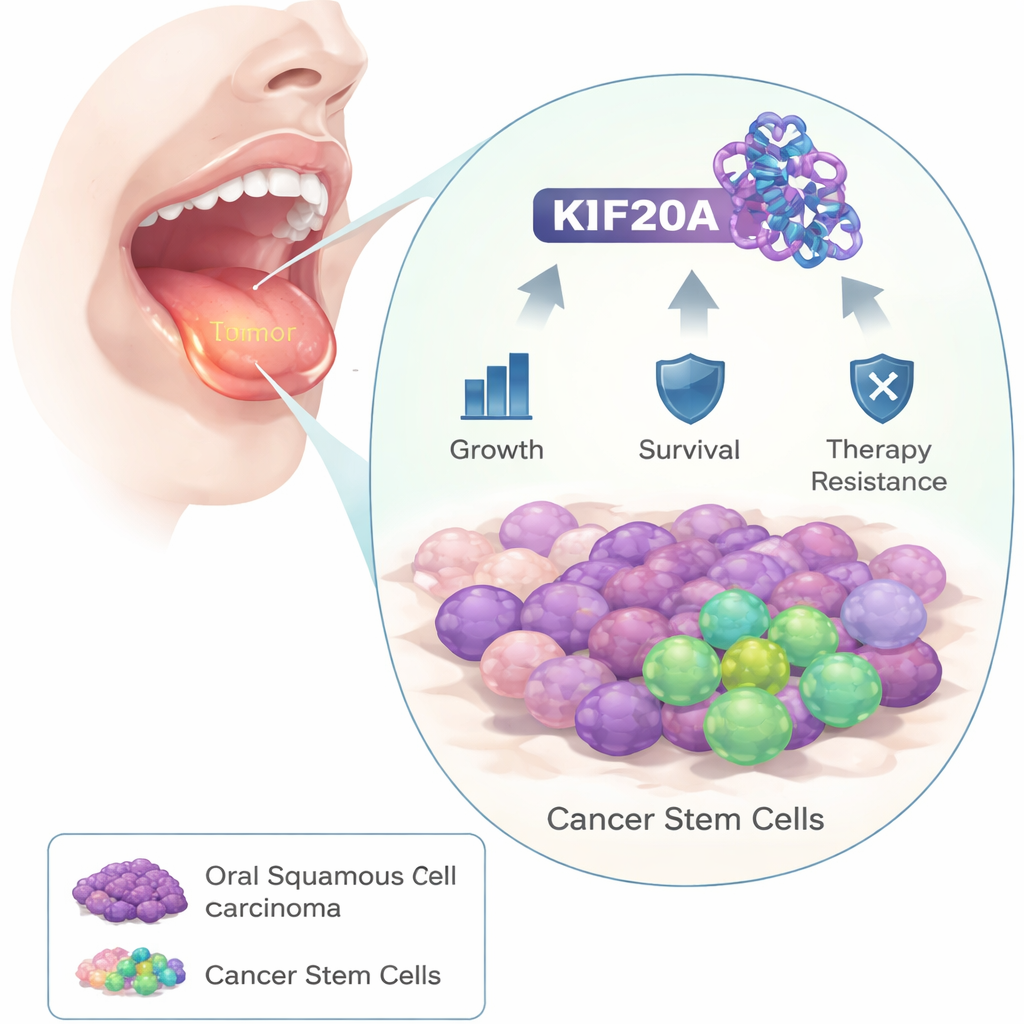
Wie KIF20A einen wichtigen RNA‑Helfer schützt
Um zu verstehen, was KIF20A tatsächlich bewirkt, nutzte das Team Protein‑Mapping‑Methoden, um nach Interaktionspartnern innerhalb der Krebszellen zu suchen. Ein zentraler Partner, der auftauchte, war DHX9, ein Protein, das an der Regulation von RNA‑Molekülen beteiligt ist und beeinflusst, wie lange bestimmte Nachrichten im Zellinneren erhalten bleiben. Die Forschenden entdeckten, dass KIF20A an DHX9 bindet und verhindert, dass es durch das E3‑Ligase‑Protein TRIM21 mit Ubiquitin markiert wird, das normalerweise DHX9 mit Ubiquitin‑Ketten versieht und so seinem Abbau durch das zelluläre Proteasom zuführt. Indem KIF20A dieses Markieren blockiert, verlangsamt es den Abbau von DHX9 und erhöht dessen Menge, insbesondere im Zytoplasma, wo es auf spezifische RNA‑Ziele einwirken kann.
Von RNA‑Stabilität zu Krebsstammzellen und Ferroptose‑Resistenz
Mit stabilerem DHX9 rückt ein weiterer entscheidender Akteur in den Fokus: SOX2, ein Schlüsselfaktor, der Zellen in einem stammzellähnlichen Zustand hält und Therapieresistenz fördert. Die Studie zeigt, dass DHX9 die SOX2‑RNA vor dem Abbau schützt, wodurch mehr SOX2‑Protein produziert werden kann. In Mundkrebzellen führte erhöhtes KIF20A zu höheren DHX9‑ und SOX2‑Spiegeln, verstärkter Tumorsphärenbildung in Kultur und einem größeren Anteil an Zellen, die Stammzellmarker exprimieren — Anzeichen erhöhter „Krebs‑Stammzell‑Eigenschaften“. KIF20A machte die Zellen außerdem weniger anfällig für Ferroptose, eine eisenabhängige, lipidbezogene Form des Zelltods, die als Möglichkeit untersucht wird, resistente Krebszellen zu eliminieren. Wenn KIF20A ausgeschaltet wurde, schrumpften Tumoren bei Mäusen leichter, und Marker der Ferroptose stiegen an, was darauf hindeutet, dass die Tumoren diesen Schutz verloren hatten.
Ein molekularer Schaltkreis mit einer medikamentös angreifbaren Schwachstelle
Setzt man diese Erkenntnisse zusammen, schlagen die Autorinnen und Autoren eine KIF20A–DHX9–SOX2‑Achse vor: KIF20A stabilisiert DHX9, DHX9 stabilisiert die SOX2‑RNA, und SOX2 erhält die Krebsstammzellen und blockiert Ferroptose. Dieser Schaltkreis wirkt sich auch auf den PI3K–AKT‑Signalweg aus, eine zentrale Wachstums‑ und Überlebensachse in vielen Krebsarten. 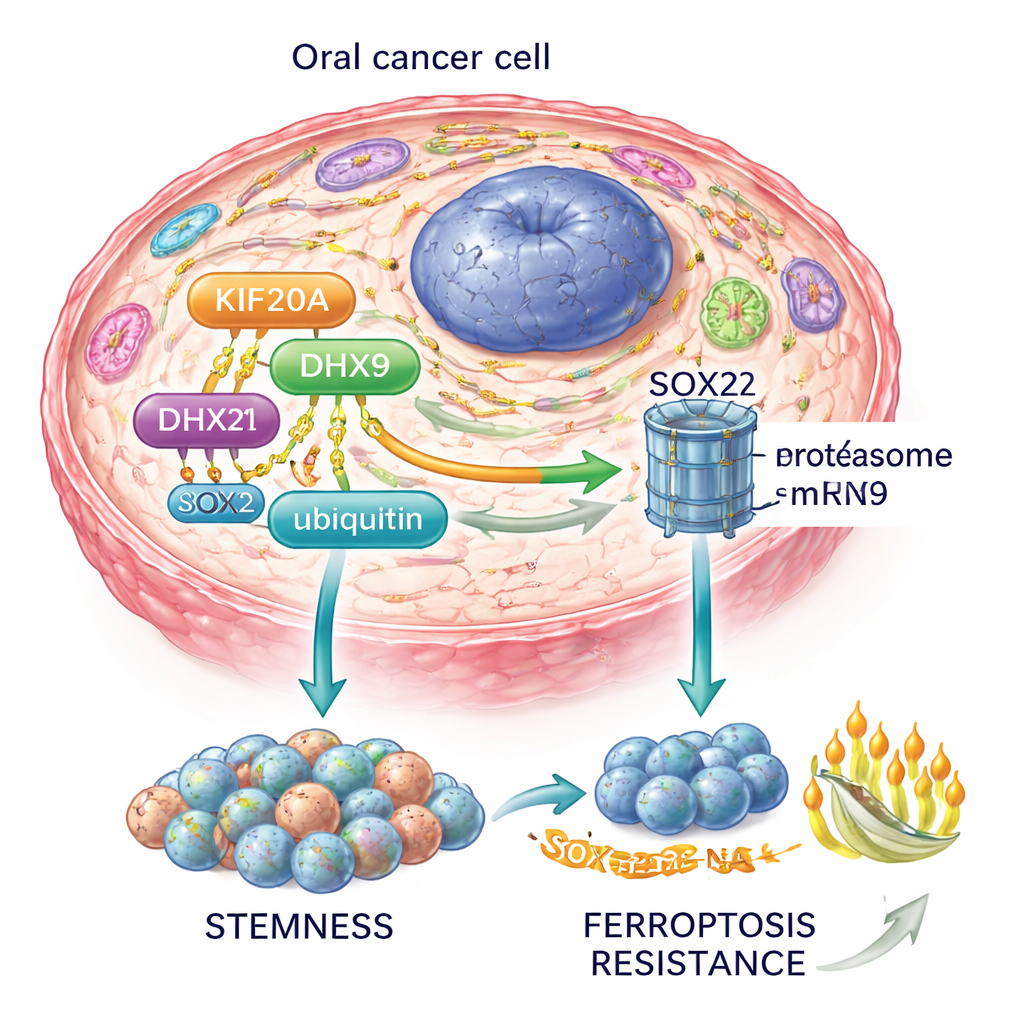
Ein Kandidat‑Medikament zur Schwächung resistenter Tumoren
Auf dem Weg zur Therapie durchsuchte das Team große Wirkstoff‑Gen‑Datenbanken nach Verbindungen, die genmusterbedingt KIF20A‑assoziierte Signaturen entgegenwirken könnten. Sie identifizierten ENMD‑2076, einen oral verfügbaren Multikinase‑Inhibitor, der bereits in anderen Krebsarten getestet wurde. In Mundkrebzellen mit hohem KIF20A senkte ENMD‑2076 die KIF20A‑, DHX9‑ und SOX2‑Spiegel, dämpfte signalgebende Wege, die mit Stammzelligkeit verbunden sind, und verlangsamte das Zellwachstum. In Kombination mit dem Standardchemotherapeutikum Cisplatin zeigte ENMD‑2076 in Zellkulturen und Maus‑Tumoren eine stärkere krebshemmende Wirkung als eines der beiden Mittel allein, ohne offensichtliche zusätzliche Toxizität.
Was das für zukünftige Therapien bedeutet
Für Nicht‑Fachleute lautet die Kernaussage: Diese Studie zeigt, wie ein überaktives Protein, KIF20A, Mundtumoren hilft, einen kleinen Pool von „Saat“‑Zellen am Leben und vor einer vielversprechenden Form des Zelltods geschützt zu halten. Durch die Kartierung dieser Kette — von KIF20A über DHX9 zu SOX2 — heben die Forschenden neue Angriffspunkte für Medikamente hervor und demonstrieren, dass ein vorhandenes experimentelles Mittel, ENMD‑2076, diese Achse schwächen und Cisplatin in Modellen wirksamer machen kann. Obwohl weitere Studien zur Sicherheit und zur Bestätigung des Nutzens beim Menschen notwendig sind, stützen die Befunde die Idee, dass das Blockieren dieses Schaltkreises Rückfälle verhindern und Therapie‑Resistenz beim Mundkrebs überwinden könnte.
Zitation: Zhang, Z., Li, Y., Hu, J. et al. KIF20A inhibits TRIM21-dependent ubiquitination of DHX9 to boost SOX2 stability, enhancing OSCC stemness and ferroptosis resistance. Cell Death Dis 17, 218 (2026). https://doi.org/10.1038/s41419-026-08467-w
Schlüsselwörter: Plattenepithelkarzinom der Mundhöhle, Krebsstammzellen, Ferroptose, KIF20A, SOX2