Clear Sky Science · de
Selenomethionin als Zwei‑Mechanismen‑Inhibitor von Ferroptose: durch Selenzufuhr getriebene GPX4‑Biosynthese jenseits der Transsulfurierung und durch Reduktionskapazität vermittelte ROS‑Entgiftung unabhängig von GPX4‑Aktivität
Warum es wichtig ist, unsere Zellen vor einem „rostähnlichen“ Tod zu schützen
Zellen im Körper können auf viele Arten zugrunde gehen; eine der jüngsten und faszinierendsten Formen ist die Ferroptose — eine eisengetriebene, „rostähnliche“ Schädigung von Zellmembranen. Dieser Prozess steht inzwischen im Zusammenhang mit Erkrankungen von Nierenschäden bis zur Neurodegeneration. Das Spurenelement Selen, das vielen aus Nahrungsergänzungsmitteln bekannt ist, spielt eine zentrale Rolle dabei, diese gefährliche Form des Zelltods zu verhindern. Diese Studie untersucht, wie eine verbreitete selenhaltige Aminosäure, Selenomethionin, Zellen vor Ferroptose schützen kann — und zwar nicht durch nur eine, sondern durch zwei verschiedene Schutzstrategien.
Ein neuer Verteidiger aus einer großangelegten Wirkstoffsuche
Um kleine Moleküle zu finden, die Ferroptose blockieren können, screente das Forscherteam Tausende von Verbindungen aus zugelassenen Arzneimitteln und Naturstoffen. Sie verwendeten die Chemikalie RSL3, um Ferroptose in humanen Krebszelllinien auszulösen, und verfolgten dann Zelltod und die Anhäufung beschädigter, oxidierter Lipide in Zellmembranen. Unter allen Kandidaten erwies sich Selenomethionin als starker Schutzfaktor: Es verringerte sowohl Lipid‑Schäden als auch Zelltod über verschiedene Zelltypen hinweg und in zwei wichtigen Ferroptose‑Modellen — einem von direkter GPX4‑Hemmung (mit RSL3) und einem anderen durch Cystin‑Entzug, einem Baustein für das Antioxidans Glutathion. Diese Ergebnisse positionierten Selenomethionin als einen breit wirksamen und robusten Ferroptose‑Inhibitor. 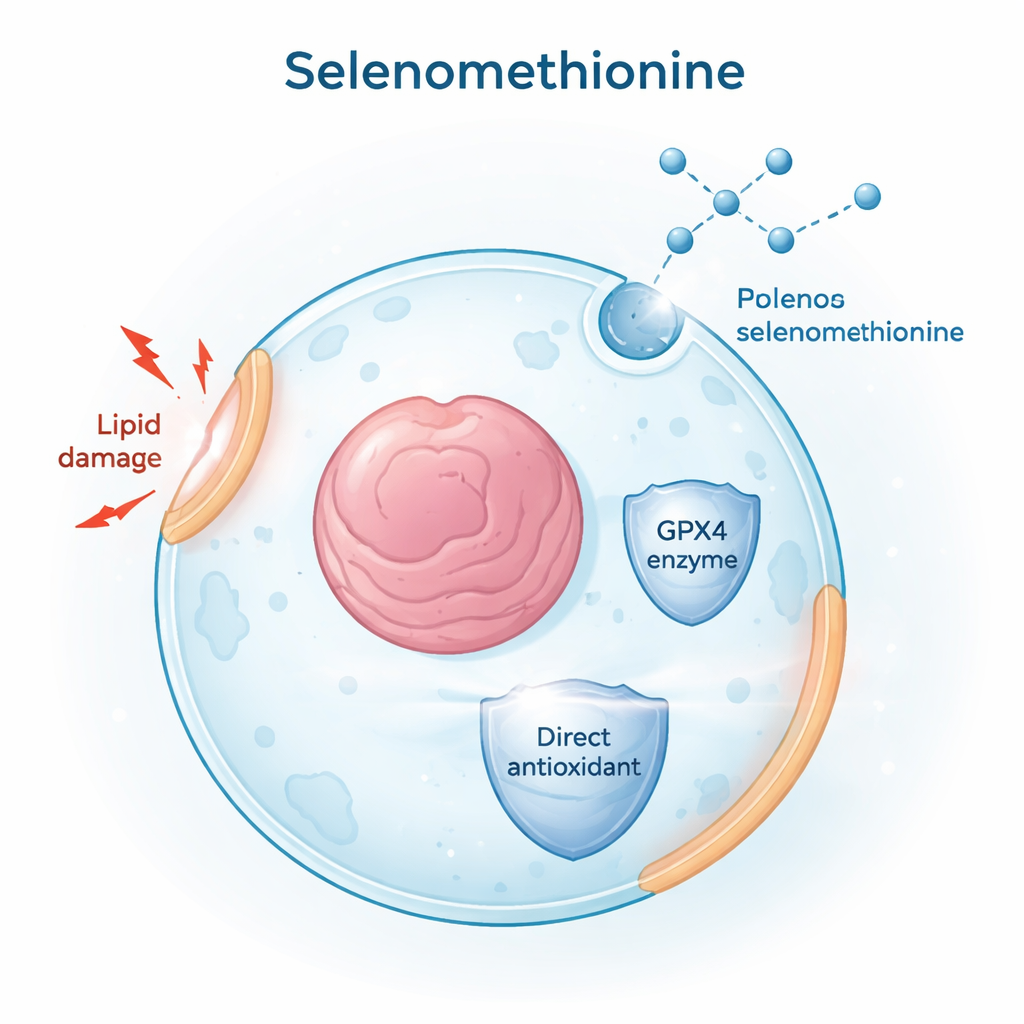
Selenzufuhr für ein zentrales Schutzenzym
Ein zentrales anti‑Ferroptose‑Element in Zellen ist das Enzym GPX4, das für seine Funktion auf Selen angewiesen ist. Das Team wollte klären, ob Selenomethionin diesen Weg lediglich speist oder darüber hinaus wirkt. Sie verfolgten, wie Selen aus Selenomethionin in Formen umgewandelt werden kann, die für den Aufbau von GPX4 geeignet sind — selbst wenn eine übliche Route, die Transsulfurierungs‑Stoffwechselbahn, beeinträchtigt oder blockiert ist. Mithilfe genetischer Herunterregulierungen und chemischer Inhibitoren von Enzymen in diesen Schwefel‑Selen‑Stoffwechselwegen fand man, dass Selenomethionin trotzdem die GPX4‑Spiegel erhöhte und Zellen schützte. Das zeigte, dass Zellen mehrere metabolische Wege anzapfen können, um Selen aus Selenomethionin zu gewinnen und die GPX4‑Produktion aufrechtzuerhalten, selbst in Geweben, in denen der klassische Weg schwach ist.
Schutz, der nicht vom üblichen Enzym abhängt
Überraschenderweise bewahrte Selenomethionin Zellen weiterhin vor Ferroptose, selbst nachdem die Forscher GPX4 mittels CRISPR‑Geneditierung vollständig entfernt hatten. Es reduzierte weiterhin Membranlipid‑Schäden und Zelltod, was zeigt, dass GPX4 nicht die ganze Erklärung ist. Weitere Experimente deuteten darauf hin, dass ein Teil dieses Schutzes darauf beruht, dass Selenomethionin in neu synthetisierte Proteine eingebaut wird, dies aber nur einen Teil der Wirkung ausmacht. Die Autor:innen richteten ihren Fokus dann auf die chemische Reaktivität von Selenomethionin selbst. Sie fanden, dass es reaktive Sauerstoffspezies (ROS), einschließlich Wasserstoffperoxid, direkt neutralisieren kann und dabei in eine oxidierte „Sulfoxid“-Form übergeht. Massenspektrometrie bestätigte dieses Produkt, und die Gabe der Sulfoxid‑Form an Zellen verringerte ebenfalls Ferroptose, was darauf hindeutet, dass Zellen sie in einem Redoxzyklus wieder zu aktivem Selenomethionin zurückverwandeln können.
Von Zellkultur bis hin zum Schutz der Nieren in lebenden Tieren
Um zu prüfen, ob diese Mechanismen in einem ganzen Organismus relevant sind, nutzte das Team ein Mausmodell für akutes Nierenschädigung durch das Krebsmedikament Cisplatin, eine Erkrankung, bei der Ferroptose eine Rolle spielt. Mäuse, die mit Cisplatin behandelt wurden, zeigten Gewichtsverlust, geschwollene Nieren, eingeschränkte Nierenfunktion und erhöhte Ferroptose‑Marker. Wenn die Tiere Selenomethionin erhielten, besserten sich viele dieser Probleme: Körpergewicht erholte sich, Nierenschwellungen nahmen ab, Blutwerte der Nierenfunktion normalisierten sich, Entzündungszeichen fielen und chemische Marker für Lipid‑Schäden gingen zurück. Das Nierengewebe zeigte außerdem höhere GPX4‑Spiegel und weniger strukturelle Schäden. Diese Vorteile waren vergleichbar mit denen, die durch Ferrostatin‑1 erzielt wurden, einen bekannten experimentellen Ferroptose‑Hemmstoff. 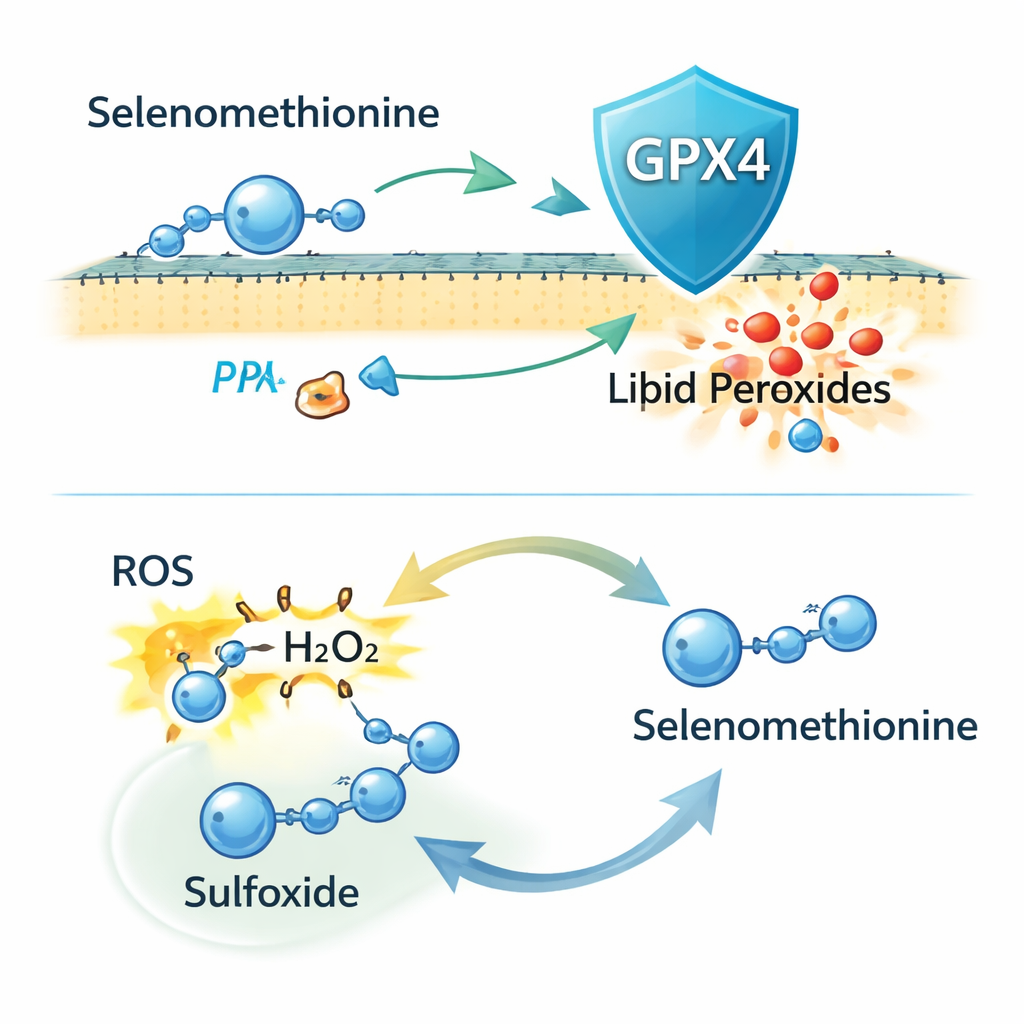
Was das für künftige Therapien bedeutet
Vereinfacht gesagt legt diese Arbeit nahe, dass Selenomethionin wie ein zweckmäßiger Feuerlöscher gegen ein eisengetriebenes „Rosten“ von Zellmembranen wirkt. Einerseits liefert es Selen, sodass Zellen mehr des Enzyms GPX4 bauen können, das als innere Aufräumcrew für beschädigte Lipide fungiert. Andererseits kann Selenomethionin selbst schädliche Oxidantien auffangen und in einem redox‑fähigen Zyklus recycelt werden, wodurch eine GPX4‑unabhängige Backup‑Schutzfunktion entsteht. Zusammengenommen machen diese Eigenschaften Selenomethionin zu einem vielversprechenden Kandidaten zur Prävention oder Behandlung von Erkrankungen, bei denen Ferroptose eine zentrale Rolle spielt — etwa medikamenteninduzierte Nierenschäden und möglicherweise andere Zustände, die von unkontrolliertem oxidativem Stress getrieben werden.
Zitation: Xia, C., Sun, X., Shao, J. et al. Selenomethionine as a dual-mechanism ferroptosis inhibitor: selenium-supply-driven GPX4 biosynthesis beyond transsulfuration and reductive-capacity-mediated ROS scavenging independent of GPX4 activity. Cell Death Dis 17, 224 (2026). https://doi.org/10.1038/s41419-026-08466-x
Schlüsselwörter: Ferroptose, Selen, Selenomethionin, oxidativer Stress, akutes Nierenversagen