Clear Sky Science · de
Die Chaperonin-TRiC-Komponente Cct3 ist für axonalen Transport, Myelinisierung und die Ausreifung neuromuskulärer Synapsen erforderlich
Wenn die Nervenverdrahtung schiefläuft
Unser Gehirn und unser Körper sind auf lange, kabelartige Nervenfasern angewiesen, die Signale schnell und zuverlässig leiten. Dazu sind viele Nerven von isolierendem Myelin umgeben, und ihre Enden müssen präzise Kontakte zu Muskeln ausbilden. Diese Arbeit untersucht, was passiert, wenn ein wichtiger zellulärer „Helfer“ beim Proteinfolding, genannt Cct3, ausfällt. Anhand von Zebrafischen und menschlichem Gewebe zeigen die Autoren, wie diese einzelne Komponente einer großen Chaperon-Maschine Myelin, Nerven–Muskel-Verbindungen und das interne Transportsystem, das Nervenzellen am Leben und funktionsfähig hält, stören kann.
Ein zellulärer Schneider fürs Nervenbauen
In jeder Zelle müssen neu gebildete Proteine in die richtigen Formen gefaltet werden, ähnlich wie ein sorgfältig geschneiderter Anzug. Der TRiC-Komplex, zu dem die Untereinheit Cct3 gehört, ist einer der wichtigsten „Schneider“ und hilft etwa 10 % aller zellulären Proteine — insbesondere den Strukturproteinen Aktin und Tubulin — korrekt zu falten. Diese Bausteine bilden das innere Gerüst der Zelle und die Schienen, entlang derer wichtige Fracht transportiert wird. Bei Patienten mit fehlerhaften Versionen von CCT3 und verwandten Genen zeigen Hirnscans verringerte weiße Substanz (die myelinhaltigen Leitungsbahnen des Gehirns) sowie Probleme in peripheren Nerven und Muskeln. Die Autoren wollten verstehen, wie der Verlust von Cct3 die Nervenentwicklung und -funktion entgleisen lässt.
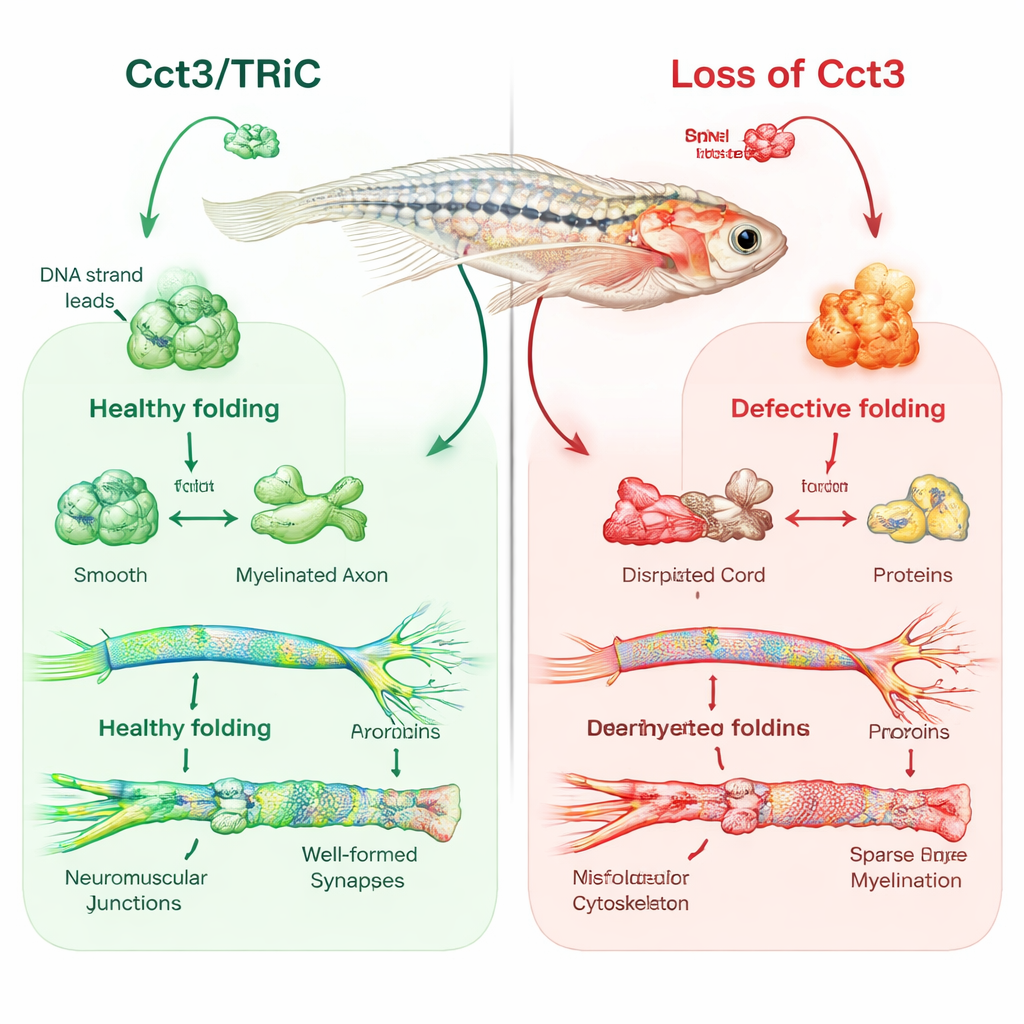
Zebrafische als Fenster zur Nervenisolierung
Das Team nutzte CRISPR/Cas9-Geneditierung, um Zebrafische zu erzeugen, denen funktionelles cct3 fehlt. Diese kleinen Fische zeigten kleinere Gehirne und Augen, Flüssigkeitsansammlungen um das Herz, schwache Berührungsreaktionen und starben innerhalb weniger Tage. Als die Forscher normales cct3 durch Injektion seiner Boten-RNA wiederherstellten, verbesserten sich viele dieser Defekte, was bestätigte, dass der Verlust von Cct3 die Ursache war. Mit Blick auf Myelin verwendeten sie Fluoreszenzmarker und Elektronenmikroskopie, um die Isolationsschichten um Nerven sichtbar zu machen. Bei normalen Fischen wickelten Myelin-bildende Zellen im Gehirn und den peripheren Nerven Axone bis zum vierten Entwicklungstag in ordentliche, geschichtete Hüllen. Im Gegensatz dazu hatten cct3-Mutanten deutlich weniger myelinisierende Zellen und praktisch kein richtiges Myelin um viele Axone, obwohl diese Axone an der Oberfläche normal geformt erschienen.
Verletzliche Stützzellen und belastete Nerven–Muskel-Verbindungen
Um herauszufinden, warum Myelin fehlte, untersuchten die Autoren Schwann-Zellen und verwandte Neuralleistenzellen — die Stützzellen, die periphere Nerven umgeben. Bei normalen Fischen streckten diese Zellen lange, schlanke Fortsätze aus und verfeinerten dann ihre Form, während sie Myelinsegmente bildeten. In Mutanten wurden sie rundlicher, verkürzten ihre Fortsätze und zerfielen in Fragmente. Ihre Zellkerne zerfielen in einem Muster, das für programmierten Zelltod typisch ist, und ein wichtiger Todesmarker (aktiviertes Caspase-3) trat auf, was zeigt, dass viele dieser Zellen frühzeitig starben. Unterdessen fehlte an den neuromuskulären Synapsen, wo Nerven auf Muskeln treffen, die Verfeinerung des Musters von Rezeptor-„Hotspots“ auf den Muskeln. Anstatt vieler kleiner, präziser Cluster wiesen die Mutanten weniger, größere Rezeptorflächen auf, was den vereinfachten synaptischen Falten ähnelt, die bei einem menschlichen Patienten mit einer CCT3-Mutation beobachtet wurden.
Beschädigte innere Schienen und verlangsamter Frachtverkehr
Da TRiC beim Falten von Aktin und Tubulin hilft, betrachteten die Autoren das innere Gerüst der motorischen Axone genauer. Sie fanden, dass die Gesamtniveaus von Tubulin in Mutanten stark reduziert waren und die Anzahl normaler Mikrotubuli — der hohlen Röhren, die als Transportspuren dienen — in zentralen und peripheren Nerven dramatisch abnahm. Chemische „Markierungen“ auf Tubulin, die für stabile, transportfähige Mikrotubuli wichtig sind, waren ebenfalls stark verändert. Mithilfe von Live-Bildgebung leuchtender Mitochondrien und Endosomen in motorischen Axonen verfolgten sie, wie diese Frachtstücke sich bewegten. Bei gesunden Fischen reisten Organellen schnell und gerichtet entlang des Axons. In Mutanten blieben viele Organellen stehen oder schwankten nur hin und her, was mit beschädigten Schienen und gestörtem Transport übereinstimmt.
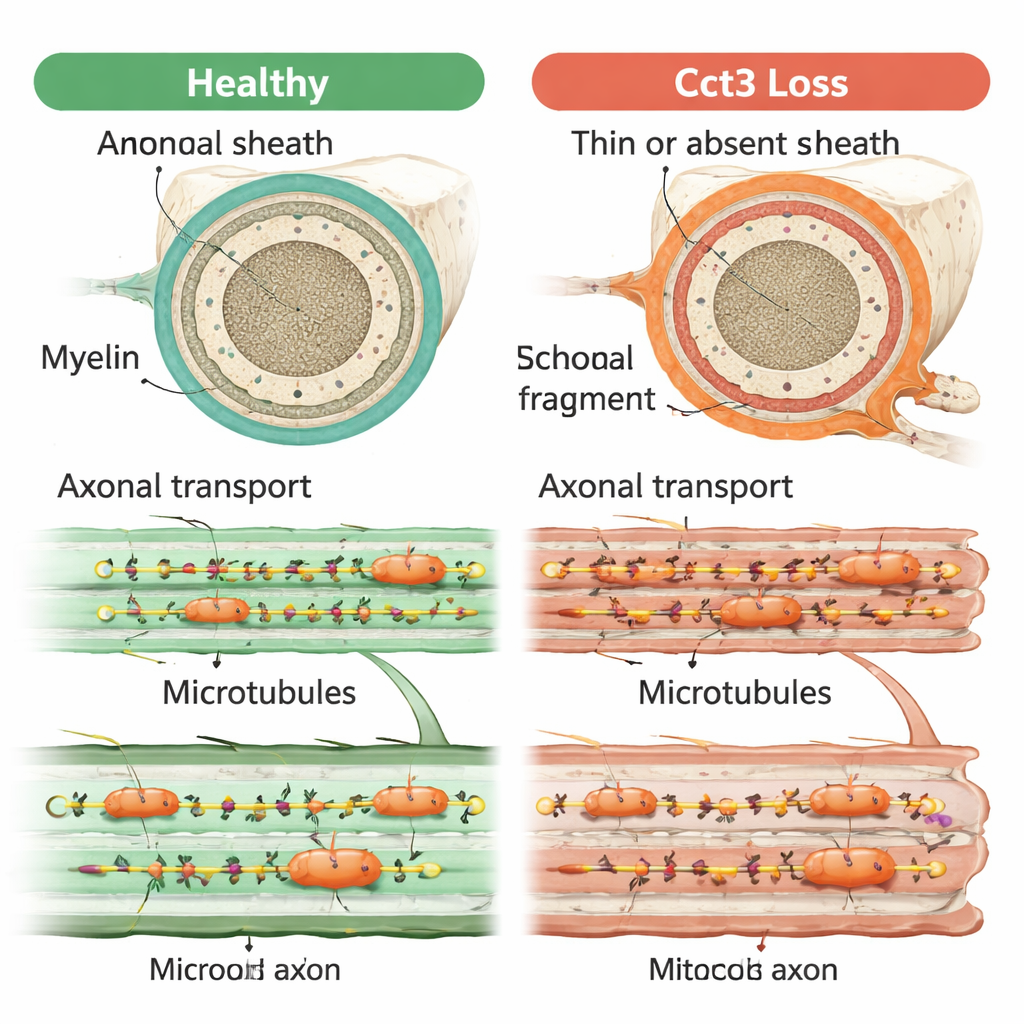
Ein zentraler Defekt hinter vielen Symptomen
Insgesamt zeigen die Ergebnisse, dass Cct3 für mehrere miteinander verbundene Aspekte der Nervengesundheit unerlässlich ist: Es unterstützt das Überleben myelinbildender Stützzellen, ermöglicht korrektes Myelinwickeln und erlaubt die Feinabstimmung reifender neuromuskulärer Synapsen. All diese Rollen lassen sich auf seine Aufgabe beim Falten und Erhalt der Proteine zurückführen, die das Zytoskelett und die Mikrotubuli-Schienen für den axonalen Transport bilden. Wenn diese Schienen versagen, können wichtige Signale und Materialien nicht die richtigen Stellen entlang des Nervs erreichen, was wahrscheinlich sowohl die Kommunikation mit myelinbildenden Zellen als auch die Ausbildung präziser Nerven–Muskel-Kontakte beeinträchtigt. Diese Arbeit legt nahe, dass gestörter axonaler Transport der gemeinsame Faden ist, der die vielfältigen Gehirn- und Nervenprobleme bei TRiC-assoziierten Erkrankungen verbindet.
Zitation: Zhang, X., Zajt, K.K., Palaz, T. et al. The chaperonin TRiC component Cct3 is required for axonal transport, myelination, and neuromuscular junction refinement. Cell Death Dis 17, 221 (2026). https://doi.org/10.1038/s41419-026-08465-y
Schlüsselwörter: Myelinisierung, axonaler Transport, neuromuskuläre Verbindung, molekulare Chaperone, Zebrafisch-Modell