Clear Sky Science · de
Beeinträchtigte BDNF‑TrkB‑Trafficking und Signalübertragung in Basalvorhofneuronen bei Down‑Syndrom
Warum diese Hirnstudie wichtig ist
Menschen mit Down‑Syndrom leben länger als je zuvor, haben aber auch ein sehr hohes Risiko, im mittleren Lebensalter eine Alzheimer‑ähnliche Demenz zu entwickeln. Diese Studie blickt tief in einzelne Gehirnzellen, um zu verstehen, warum bestimmte Neurone besonders anfällig sind. Indem die Forschenden nachverfolgen, wie diese Zellen ein wichtiges „Gehirndünger“-Molekül transportieren und darauf reagieren, decken sie einen Stau innerhalb der Neurone auf, der helfen könnte, Gedächtnisverlust zu erklären und auf neue Behandlungsansätze hinweist.
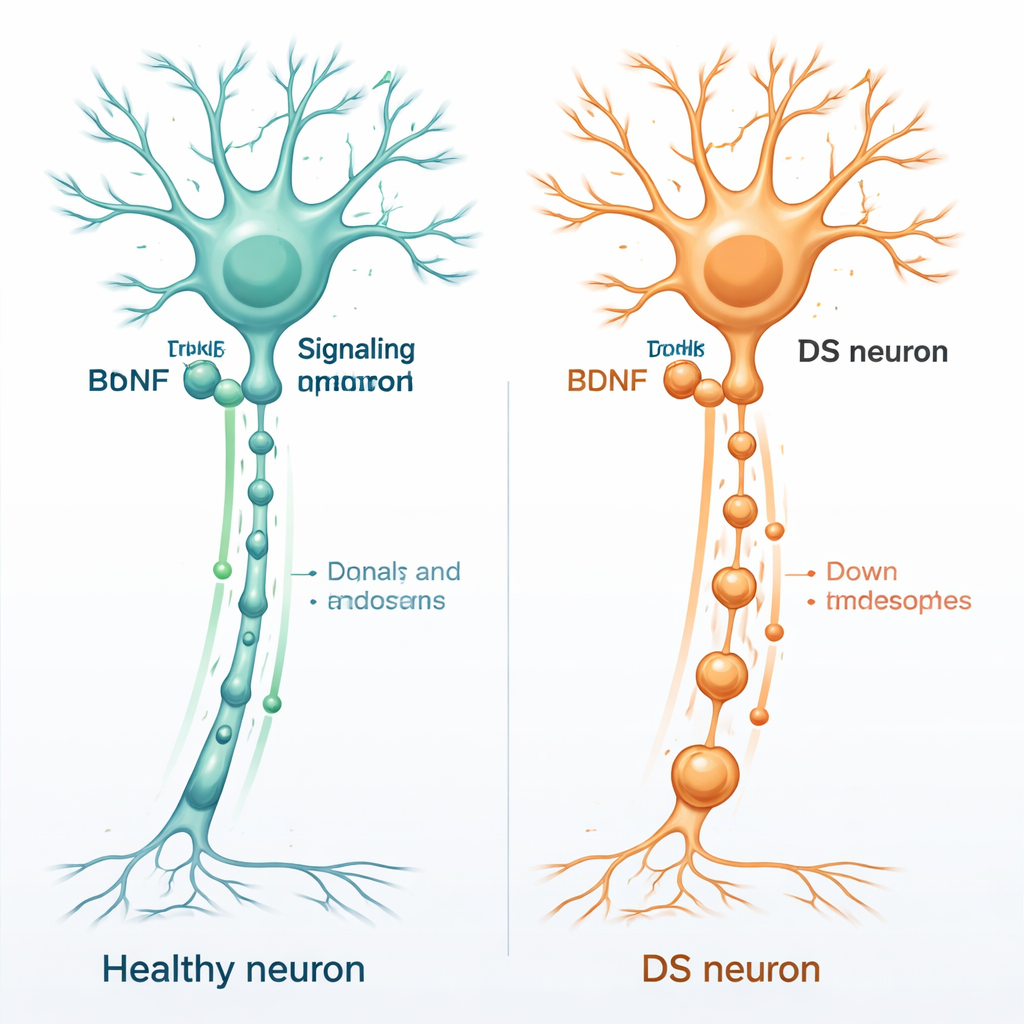
Gehirndünger und die Gesundheit von Nervenzellen
Gesunde Gehirnzellen sind auf eine Reihe von Stützmolekülen angewiesen, die als Neurotrophine bezeichnet werden und für Neurone wie Dünger wirken. Eines der wichtigsten ist das brain‑derived neurotrophic factor, kurz BDNF. BDNF bindet an ein Andockprotein auf Neuronen namens TrkB, gewöhnlich an den weit außen liegenden Enden der Nervenfasern. Sobald BDNF anhaftet, wird der gesamte BDNF–TrkB‑Komplex in kleine Membranschläuche aufgenommen und entlang der langen Nervenfaser zurück zum Zellkörper transportiert. Diese bewegten Bläschen, bekannt als Signalendosomen, signalisieren dem Zellkern, welche Gene eingeschaltet werden müssen, um das Neuron am Leben, verbunden und anpassungsfähig zu halten.
Wenn zelluläre Versandbehälter zu groß werden
Das Team konzentrierte sich auf Basalvorhofneurone, eine Zellgruppe, die Gedächtnis und Aufmerksamkeit stark unterstützt und zu den ersten gehört, die sowohl bei Down‑Syndrom als auch bei Alzheimer‑Krankheit degenerieren. Mit einem Mausmodell des Down‑Syndroms namens Dp1Tyb färbten sie Neurone für einen frühen Endosomenmarker und verglichen sie mit normalen Neuronen. Die Down‑Syndrom‑Neurone enthielten deutlich mehr frühe Endosomen, die mehr als 50 Prozent größer waren als üblich. Diese Strukturen werden von Rab5 gesteuert, einem molekularen Schalter, der hilft, diese internen „Versandbehälter“ zu bilden und zu sortieren. Die Forschenden fanden, dass Rab5 in Down‑Syndrom‑Neuronen bereits in einem überaktiven Zustand verharrte, selbst vor einer BDNF‑Stimulation, was darauf hindeutet, dass das endosomale System bereits auf Hochtouren lief.
Staus entlang der Nervenfaser
Als Nächstes fragten die Wissenschaftler, ob diese verzerrte interne Landschaft die Bewegung von BDNF‑Signalen beeinträchtigte. Sie züchteten Neurone in mikrofluidischen Geräten, die Zellkörper von ihren Axonendigungen trennen, sodass nur die Axonspitzen stimuliert werden können. Durch Verfolgung harmloser fluoreszenter Tracer, die die gleiche Transportstrecke wie BDNF–TrkB‑Komplexe nutzen, maßen sie, wie schnell die Signalendosomen zurück zum Zellkörper unterwegs waren. In normalen Neuronen beschleunigte die Zugabe von BDNF die Endosomen um etwa 30 Prozent und verringerte Pausen, was eine robuste Reaktion auf Wachstumssignale widerspiegelt. In Down‑Syndrom‑Neuronen hingegen gelang es BDNF nicht, den Transport zu beschleunigen oder Pausen zu reduzieren. Ein separates Experiment, das echte TrkB‑Rezeptoren verfolgte, bestätigte, dass weniger von ihnen erfolgreich den Zellkörper in Down‑Syndrom‑Zellen erreichten.
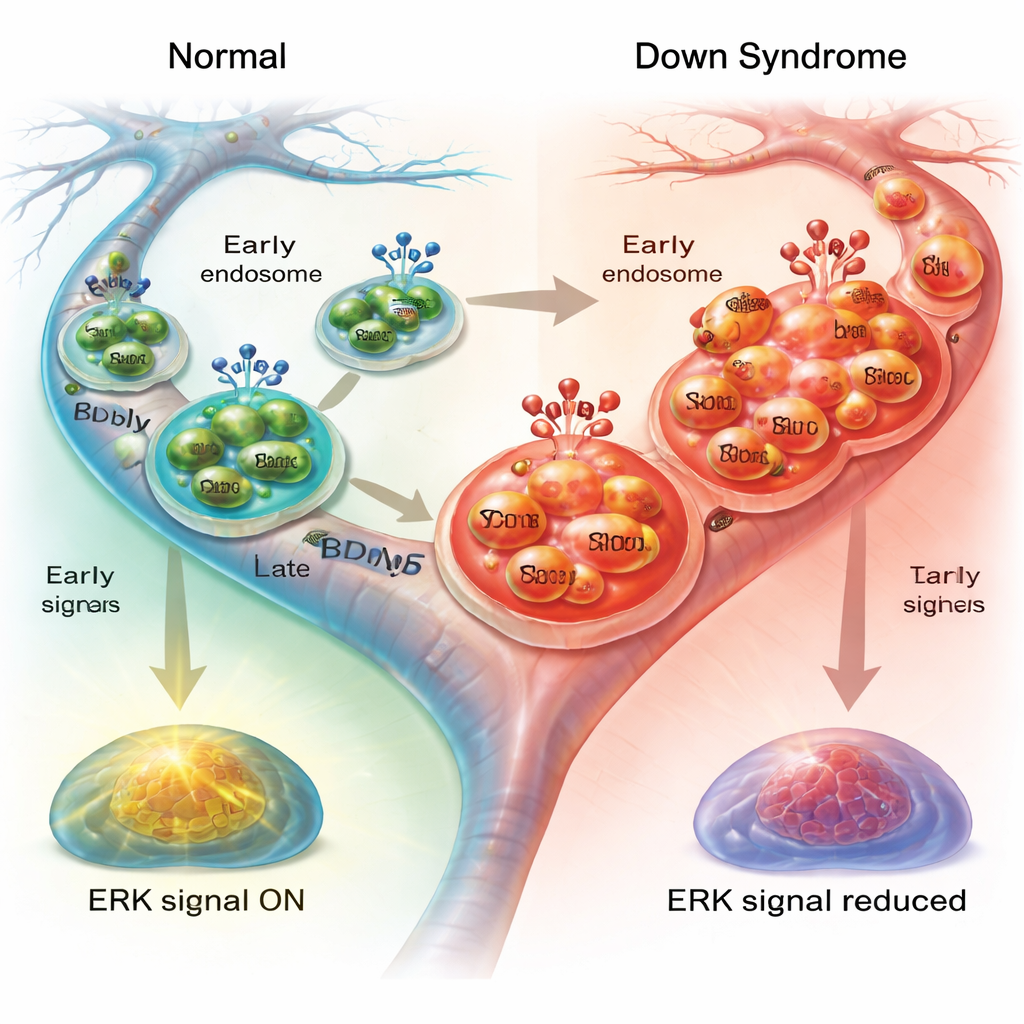
Abgeschwächte nachgeschaltete Signale innerhalb der Zelle
Damit diese reisenden Bläschen die Gesundheit der Neurone unterstützen, müssen sie nach Erreichen ihres Ziels interne Signalwege aktivieren. Ein wichtiger Pfad involviert ERK1/2, ein Enzympaar, das die Nachricht von BDNF an den Zellkern weiterleitet und hilft, das Zellskelett und die Transportmaschinerie zu regulieren. Als die Forschenden aktiviertes ERK1/2 nach BDNF‑Behandlung maßen, stellten sie in normalen Neuronen einen klaren Anstieg fest, in Down‑Syndrom‑Neuronen hingegen eine deutlich schwächere Reaktion, besonders in den Axonen. Das Blockieren von ERK1/2 in gesunden Neuronen reproduzierte teilweise den trägen Transport, wie er in Down‑Syndrom‑Zellen zu sehen war: Endosomen wurden langsamer und pausierten häufiger. Im Gegensatz dazu hatte die ERK1/2‑Blockade in Down‑Syndrom‑Neuronen kaum einen zusätzlichen Effekt, was mit bereits gedämpfter Signalübertragung übereinstimmt.
Was das für das Altern des Gehirns bei Down‑Syndrom bedeutet
Zusammen genommen deuten die Ergebnisse auf ein sich selbst verstärkendes Problem in anfälligen Neuronen hin: Rab5 ist überaktiv, frühe Endosomen schwellen an und BDNF–TrkB‑Komplexe werden in Kompartimenten gefangen, die sich nicht effizient bewegen. Infolgedessen erreichen weniger Wachstumssignale den Zellkörper, die ERK1/2‑Signalübertragung ist geschwächt und die Maschinerie, die den Ferntransport antreibt, wird weiter beeinträchtigt. Im Laufe von Jahren kann dieses fehlerhafte Kommunikationssystem zum frühen und schweren Verlust von Basalvorhofneuronen beitragen, wie er bei Alzheimer‑Erkrankungen im Zusammenhang mit Down‑Syndrom beobachtet wird. Indem die Studie diese Verbindung zwischen endosomalem „Verkehrsmanagement“ und Wachstumsfaktorsignalen beleuchtet, weist sie auf neue therapeutische Ansätze hin, die darauf abzielen, Rab5‑Aktivität zu normalisieren, Endosomenfunktionen wiederherzustellen und BDNF‑Antworten zu stärken, um diese wichtigen Neurone zu schützen.
Zitation: Blackburn, E., Birsa, N., Lopes, A.T. et al. Impaired BDNF-TrkB trafficking and signalling in Down syndrome basal forebrain neurons. Cell Death Dis 17, 214 (2026). https://doi.org/10.1038/s41419-026-08464-z
Schlüsselwörter: Down‑Syndrom, Alzheimer‑Krankheit, BDNF, Axonentransport, Endosomen