Clear Sky Science · de
Endotheliales IRE1-Signal erhält die Integrität der Blut‑Hirn‑Schranke und begrenzt Neuroinflammation nach traumatischer Hirnverletzung
Warum der Schutz der inneren Gehirnwand wichtig ist
Nach einem Schlag auf den Kopf ist der unmittelbare Schaden nur ein Teil der Geschichte. In den Stunden und Tagen danach startet das Gehirn eine starke Stress‑ und Immunantwort, die die Verletzung still und leise weiter ausdehnen kann. Diese Studie untersucht, wie ein kleines, stresswahrnehmendes System in den Zellen, die die Gehirngefäße auskleiden, dazu beiträgt, die innere Gehirnwand — die Blut‑Hirn‑Schranke — nach traumatischer Hirnverletzung verschlossen und ruhig zu halten. Das Verständnis dieser verborgenen Abwehr könnte auf neue Behandlungen hinweisen, die bleibende Behinderungen nach Kopfverletzungen begrenzen.
Die Torwächter des Gehirns unter Stress
Das Gehirn ist auf eine spezialisierte Schranke angewiesen, die von Endothelzellen gebildet wird; sie kleiden das Innere der Blutgefäße aus und kontrollieren streng, was aus dem Blut in das Hirngewebe gelangt. Traumatische Hirnverletzungen (TBI) können diese Blut‑Hirn‑Schranke stören, wodurch entzündliche Moleküle und Immunzellen eindringen und den Schaden verschlimmern können. In diesen Endothelzellen existiert ein Qualitätskontrollsystem, die sogenannte Antwort auf fehlgefaltete Proteine (unfolded protein response), die Zellen hilft, mit Stress im endoplasmatischen Retikulum umzugehen. Ein zentraler Bestandteil davon, IRE1, fungiert als Sensor und Regulator, wenn Zellen unter Druck stehen. Die Forschenden fragten: Trägt dieser endotheliale Stresssensor dazu bei, die Schranke nach einer TBI zu schützen, oder verschlechtert er die Lage?
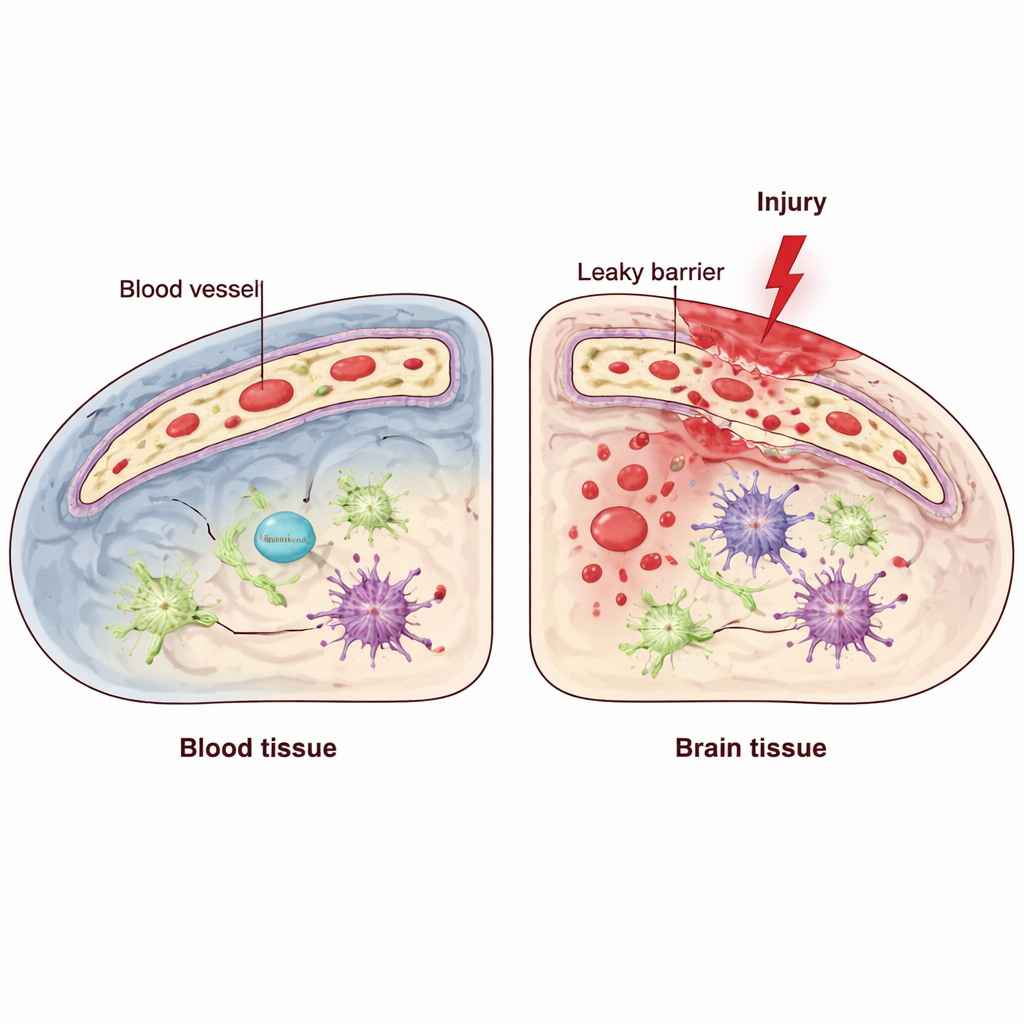
Ein zellulärer Sensor in Gefäßzellen abschalten
Um das herauszufinden, verwendete das Team genetisch veränderte Mäuse, bei denen IRE1 selektiv nur in Endothelzellen ausgeschaltet werden konnte. Anschließend erzeugten sie eine kontrollierte Verletzung im motorischen Kortex, die Aspekte menschlicher TBI nachbildet, und verglichen diese Mäuse mit normalen Wurfgeschwistern. Sie testeten die Bewegung mit Aufgaben, die Gleichgewicht und präzise Pfotenplatzierung messen, und untersuchten das Hirngewebe mit hochauflösender Mikroskopie und molekularen Techniken. Bei normalen Mäusen stieg die IRE1‑Aktivität in Gefäßzellen nahe der Verletzung kurz nach dem Trauma an, was darauf hindeutet, dass Endothelzellen Stress schnell wahrnehmen und darauf reagieren. Fehlt IRE1 spezifisch in diesen Zellen, schnitten die Tiere in den Motortests schlechter ab, was auf eine schlechtere funktionelle Erholung hinweist.
Undichte Gefäße, mehr Immunzellen und sterbende Neurone
Die Forschenden untersuchten als Nächstes, wie gut die Blut‑Hirn‑Schranke den Belastungen standhielt. Normalerweise verbleiben große Blutproteine wie Antikörper innerhalb der Gefäße. Nach einer TBI ist in der Nähe der Läsion ein gewisses Austreten zu erwarten, doch Mäuse ohne endotheliales IRE1 zeigten ein deutlich weiter verbreitetes Eindringen dieser Proteine ins Gehirn. Die Mikroskopie zeigte, dass ein wichtiges Verbindungsprotein, VE‑Cadherin, das Endothelzellen zusammen abdichtet, im verletzten Bereich reduziert war, wenn IRE1 fehlte, obwohl die Gesamtzahl der Gefäße ähnlich erschien. Diese Undichtigkeit ging einher mit einem massiven Zustrom von Immunzellen in die Nähe der Läsion und erhöhten Entzündungssignalen. In denselben Bereichen zeigten Neurone häufiger Zeichen von Degeneration und programmierter Zellsterblichkeit, und die Zone des geschädigten Gewebes um den Kerndefekt war deutlich größer.
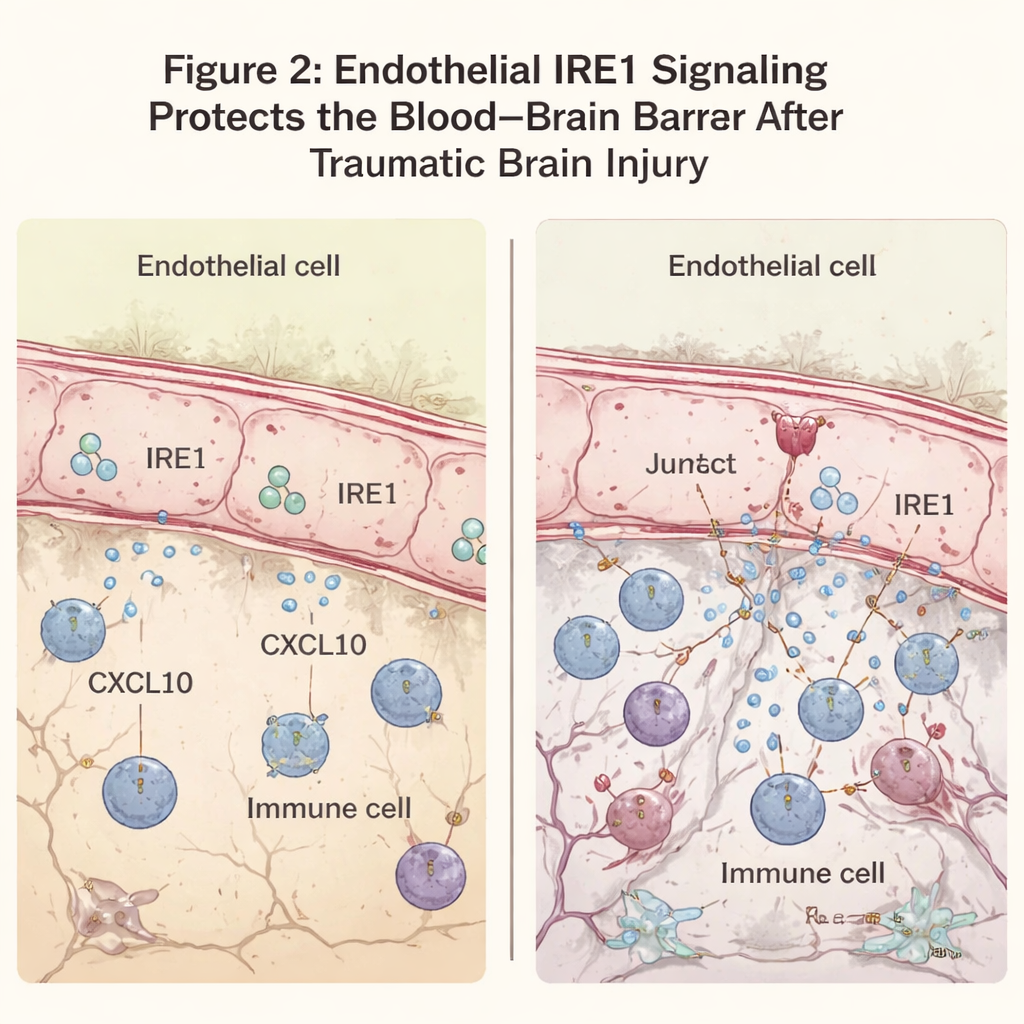
Ein Stressmedikament dämpft den Signalsturm
Um die molekularen Grundlagen zu verstehen, analysierte das Team, welche Gene nach der Verletzung hochreguliert wurden. Bei Mäusen ohne endotheliales IRE1 waren Gene, die an antiviralen und entzündlichen Reaktionen beteiligt sind, stark erhöht. Besonders auffällig war CXCL10, eine Chemokinart — eine Art molekularer Signalstoff —, die Immunzellen anlockt und die Schranke weiter schwächen kann. CXCL10 war in Endothelzellen nahe der Läsion besonders erhöht, wenn IRE1 fehlte. In kultivierten Gehirn‑Endothelzellen, die einem entzündlichen Auslöser ausgesetzt wurden, senkte die Verringerung des ER‑Stresses mit einem Wirkstoff namens TUDCA sowohl die IRE1‑Aktivität als auch die CXCL10‑Produktion. Wurde TUDCA verletzten Mäusen verabreicht, reduzierte es CXCL10 und Immunzellmarker im geschädigten Kortex und verbesserte die motorische Leistung, was darauf hindeutet, dass das Abklingen dieses Stresswegs sekundäre Schäden abschwächen kann.
Was das für Menschen mit Kopfverletzungen bedeutet
Kurz gesagt deuten diese Ergebnisse darauf hin, dass der Stresssensor IRE1 in den Zellen, die die Gehirngefäße auskleiden, nach einer traumatischen Hirnverletzung als Wächter wirkt. Wenn er vorhanden und funktionsfähig ist, trägt er dazu bei, die Blut‑Hirn‑Schranke dicht zu halten, reduziert die Freisetzung chemischer Signale, die Immunzellen herbeirufen, und begrenzt die Ausbreitung von Entzündung und Neuronverlust um die Läsion. Ist er deaktiviert, wird die Schranke durchlässiger, Immunzellen strömen ein und mehr Hirngewebe wird beschädigt. Da Gefäßzellen für im Blut zirkulierende Medikamente vergleichsweise gut zugänglich sind, könnte das Anvisieren ihrer Stressantworten — mit Verbindungen wie TUDCA oder künftig präziseren Therapien — eine praktikable Strategie werden, um langfristigen Schaden nach Kopfverletzungen zu reduzieren.
Zitation: Fan, Q., Takarada-Iemata, M., Tanaka, T. et al. Endothelial IRE1 signaling maintains blood–brain barrier integrity and limits neuroinflammation after traumatic brain injury. Cell Death Dis 17, 210 (2026). https://doi.org/10.1038/s41419-026-08461-2
Schlüsselwörter: traumatische Hirnverletzung, Blut‑Hirn‑Schranke, Endothelzellen, Neuroinflammation, zellulärer Stress