Clear Sky Science · de
CD36 erhöht die Empfindlichkeit von triple-negativen Brustkrebszellen gegenüber palmitatinduzierter Ferroptose
Warum Fett rund um Tumoren sowohl Freund als auch Feind sein kann
Brusttumoren wachsen in Gewebe, das natürlicherweise fettreich ist, und Krebszellen „ernähren“ sich bekanntermaßen von in der Nähe verfügbaren Fettsäuren. Diese Studie untersucht eine überraschende Wendung: Unter den richtigen Bedingungen kann eine der häufigsten Fette im Körper, Palmitinsäure, tatsächlich helfen, eine besonders aggressive Form von Brustkrebs zu töten, indem sie eine bestimmte Art des Zelltods auslöst. Zu verstehen, wie das geschieht, könnte auf neue Behandlungen für Patientinnen hinweisen, die derzeit nur wenige Optionen haben.
Ein schwer zu behandelnder Brustkrebs unter dem Mikroskop
Der triple-negative Brustkrebs (TNBC) fehlt die Hormon- und Wachstumsfaktorrezeptoren, auf die viele moderne Medikamente abzielen, wodurch er zu einer der schwierigsten Brustkrebsarten in der Behandlung zählt. Diese Tumoren stehen in engem Kontakt mit Fettzellen, die große Mengen an Fettsäuren freisetzen, darunter die gesättigte Fettsäure Palmitinsäure. Die Forschenden wollten wissen, ob Palmitinsäure das Tumorwachstum einfach nur antreibt oder ob sie auch eine Schwachstelle schafft, die zum Abtöten von Krebszellen ausgenutzt werden könnte.
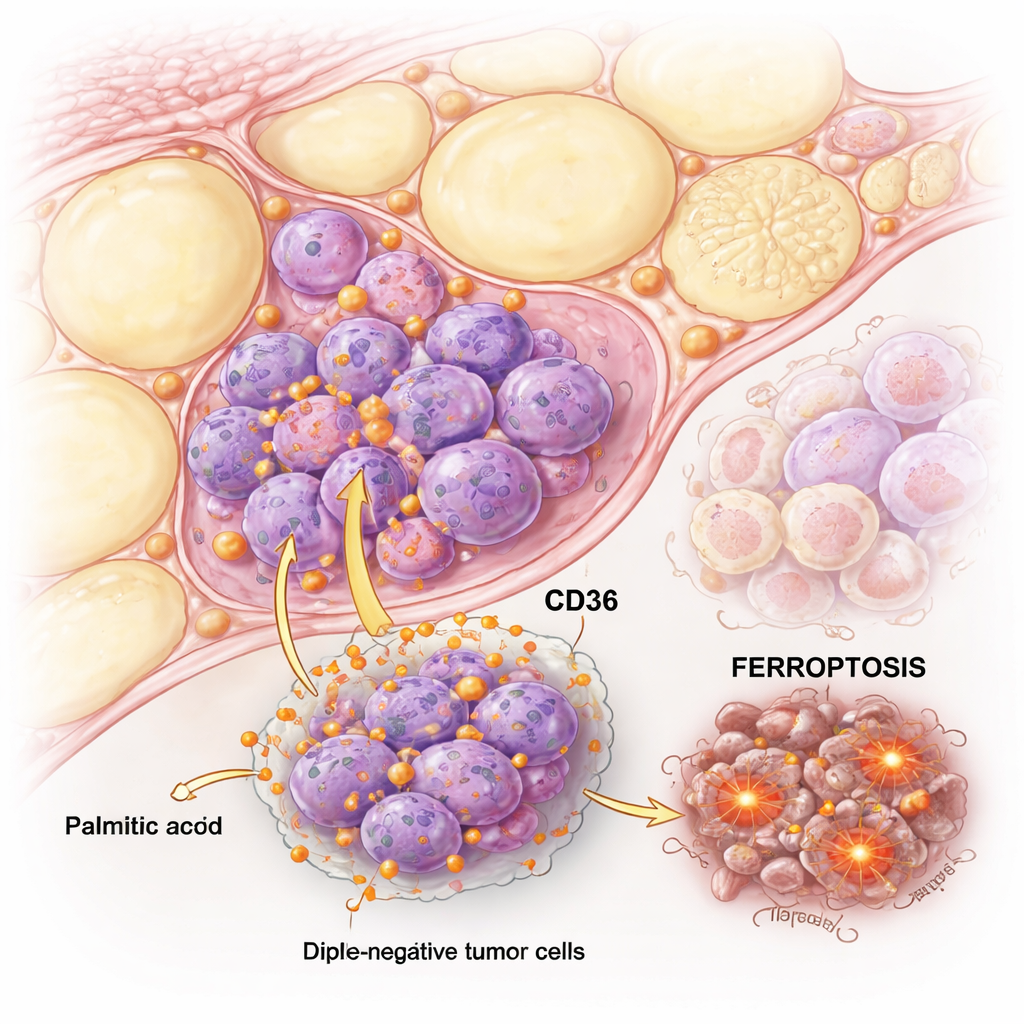
Wenn Palmitinsäure Krebszellen über die Kante treibt
Das Team verglich TNBC-Zellen mit hormonempfindlichen „luminalen“ Brustkrebszellen und setzte sie steigenden Mengen an Palmitinsäure aus. Beide Zelltypen konnten durch hohe Dosen geschädigt werden, doch TNBC-Zellen waren deutlich empfindlicher. Detaillierte Tests zeigten, dass in luminalen Zellen Palmitinsäure vornehmlich klassische Apoptose auslöste, eine ordentliche Form des Zelltods. In TNBC-Zellen jedoch löste Palmitinsäure sowohl Apoptose als auch einen anderen, weniger bekannten Weg namens Ferroptose aus, der von Eisen und der Zerstörung von Membranlipiden abhängt.
Eine Fettsäurepforte namens CD36
Um zu verstehen, warum TNBC-Zellen so anders reagierten, konzentrierten sich die Forschenden auf CD36, ein Protein an der Zelloberfläche, das wie eine Pforte für langkettige Fettsäuren wirkt. TNBC-Zellen wiesen natürlicherweise deutlich mehr CD36 auf als luminale Zellen, und die Exposition gegenüber Palmitinsäure erhöhte die CD36-Spiegel weiter. Das bedeutete, dass TNBC-Zellen mehr Palmitinsäure aufnahmen, mehr beschädigte Lipide anhäuften, mehr reaktive Sauerstoffspezies in ihren Mitochondrien produzierten und mehr freies Eisen innerhalb der Zelle ansammelten — alles Schlüsselzeichen der Ferroptose. Wenn CD36 mit einem Wirkstoff blockiert oder genetisch reduziert wurde, nahm die palmitinsäureinduzierte Ferroptose stark ab.
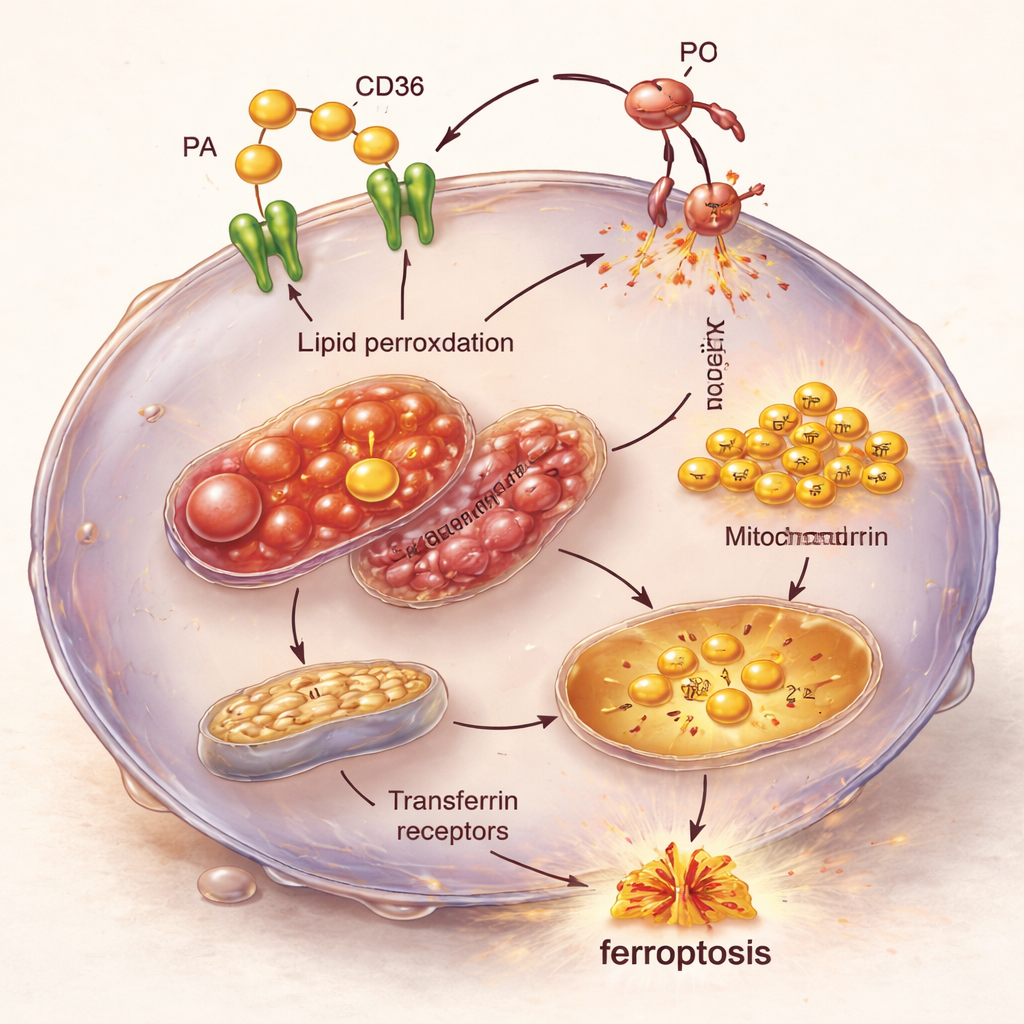
Ein Blick auf die Kettenreaktion im Zellinneren
Mikroskopie und Analysen der Genaktivität enthüllten die interne Kettenreaktion hinter dieser Verwundbarkeit. Mit Palmitinsäure und hohem CD36 belastete TNBC-Zellen zeigten geschwollene, strukturell geschädigte Mitochondrien und steigende Eisenwerte, die über Transferrinrezeptoren hereingebracht wurden. Gleichzeitig wurden Gene, die Ferroptose fördern, hochreguliert, während Gene, die normalerweise gegen diese Form des Zelltods schützen, heruntergefahren wurden. Das Ergebnis ist ein perfekter Sturm: einströmendes Fett im Übermaß, mehr verfügbares Eisen, das chemische Reaktionen antreibt, und geschwächte Verteidigungsmechanismen gegen Lipid-Schäden — zusammen treiben sie TNBC-Zellen in die Ferroptose.
Welche Patientinnen könnten am meisten profitieren?
Krebs ist nicht einheitlich, selbst innerhalb von TNBC. Anhand von in Mäusen gezüchteten Tumorproben und großen Patientendatenbanken fanden die Autorinnen und Autoren heraus, dass CD36 besonders hoch in einem bestimmten TNBC-Subtyp namens luminal androgen receptor (LAR) war, der bereits als empfindlicher gegenüber Ferroptose aufgefallen war. Andere TNBC-Subtypen mit hoher Eisenaufnahme zeigten ebenfalls tendenziell erhöhte CD36-Werte. Dieses Muster legt nahe, dass CD36 als Marker dienen könnte, um Patientinnen zu identifizieren, deren Tumoren natürlicherweise für Ferroptose-basierte Therapien prädisponiert sind.
Eine gängige Fettsäure in eine therapeutische Hilfe verwandeln
Einfach gesagt zeigt diese Arbeit, dass eine weit verbreitete Nahrungs- und Körperfettart, Palmitinsäure, bestimmte triple-negative Brustkrebszellen töten kann, wenn diese hohe Mengen des Fetttransporters CD36 exprimieren. Indem CD36 Fettüberladung, Eisenansammlung und Schäden an Zellmembranen fördert, macht es diese Krebszellen anfälliger für Ferroptose — ein zerstörerisches Schicksal, dem sie nicht entkommen können. Wenn künftige Behandlungen diesen Weg sicher verstärken oder ihn mit Wirkstoffen kombinieren können, die die Abwehrmechanismen der Zellen weiter schwächen, könnten Klinikerinnen und Kliniker diese metabolische Schwäche in eine neue, präzisere Methode verwandeln, einige der aggressivsten Brusttumoren anzugreifen.
Zitation: Closset, L., Foy, JP., Louadj, L. et al. CD36 enhances sensitivity of triple negative breast cancer cells to palmitate-induced ferroptosis. Cell Death Dis 17, 219 (2026). https://doi.org/10.1038/s41419-026-08460-3
Schlüsselwörter: triple-negativer Brustkrebs, Ferroptose, CD36, Palmitinsäure, Tumorstoffwechsel