Clear Sky Science · de
USP30-vermittelte Deubiquitinierung von Hexokinase 2 steuert das stoffwechsel- und Tumorwachstums-Schicksal von Glukose
Wie Krebszellen ihre Zucker‑Nutzung umverdrahten
Krebszellen sind bekannt für ihren „süßen Zahn“: sie verwerten Zucker auf ungewöhnliche Weise, um schnelles Wachstum zu ermöglichen. Diese Studie legt einen neuen Schalter frei, ein Protein namens USP30, das Tumorzellen dabei hilft zu entscheiden, wie Glukose genutzt wird. Durch die Feinabstimmung eines anderen Proteins, der Hexokinase 2 (HK2), kann USP30 Krebszellen dazu bringen, mehr Zucker zu verbrauchen und schneller zu wachsen — ein Hinweis auf ein neues Ziel für künftige Krebstherapien. 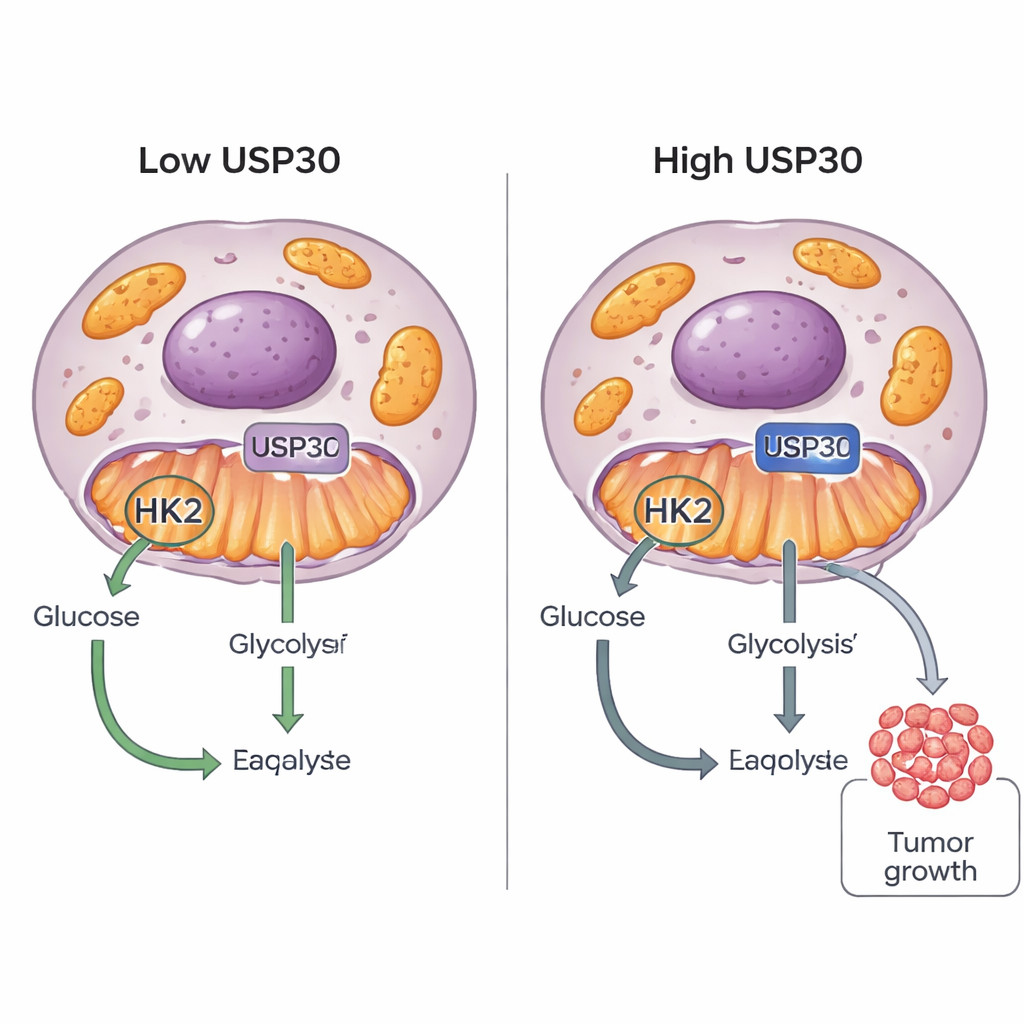
Ein zuckerhungriger Lebensstil in Tumoren
Die meisten gesunden Zellen gewinnen Energie effizient aus Nährstoffen, aber viele Krebszellen bevorzugen einen schnellen, weniger effizienten Weg, die aerobe Glykolyse, auch bekannt als Warburg‑Effekt. Sie nehmen große Mengen Glukose auf und wandeln sie schnell in Laktat um, selbst wenn ausreichend Sauerstoff vorhanden ist. Diese Strategie dient nicht nur der Energiegewinnung: sie liefert Bausteine für DNA, Fette und Proteine, hilft Tumoren, Stress zu überstehen, und kann sogar Immunangriffe schwächen. An der Schwelle zu diesem Stoffwechselweg steht die Hexokinase, ein Enzym, das eintreffende Glukose mit einer Phosphatgruppe markiert und sie so für den weiteren Abbau und wachstumsfördernde Reaktionen verpflichtet.
Ein mitochondriales Enzym rückt ins Rampenlicht
USP30 ist ein Enzym auf der Außenseite der Mitochondrien, den Kraftwerken der Zelle. Es gehört zur Familie der Deubiquitinasen, die kleine Proteinmarken namens Ubiquitin von anderen Proteinen entfernen und dadurch oft deren Stabilität, Ort oder Aktivität verändern. USP30 war bereits für Funktionen in Nervenzellen und für die Kontrolle der mitochondrialen Qualität bekannt, sein Einfluss auf Krebs war jedoch unklar. Durch die Auswertung großer Krebs‑Gen‑Datenbanken stellten die Forscher fest, dass Tumoren mit erhöhten USP30‑Spiegeln tendenziell stärkere Glukose‑Verbrennungs‑Signaturen und schwächere Fettverbrennungs‑Signaturen zeigten, was darauf hindeutet, dass USP30 Krebszellen beim Umschalten auf einen zuckerbetriebenen Stoffwechsel unterstützen könnte.
Verbindung von USP30 zu den Zucker‑Torwächtern der Zelle
Um diese Verbindung zu untersuchen, reduzierten oder entfernten die Forscher USP30 in mehreren Krebszelllinien und maßen, wie die Zellen Energie verarbeiteten. Mit Messgeräten, die Säureproduktion und Sauerstoffverbrauch in Echtzeit verfolgen, fanden sie, dass der Verlust von USP30 sowohl die Glykolyse als auch die mitochondriale Atmung deutlich reduzierte. Laktatproduktion und Glukoseverbrauch sanken, was zeigt, dass der Zuckerstoffwechsel der Zellen langsamer lief. Eine Reihe von Massenspektrometrie‑Experimenten zeigte dann, dass USP30 physisch mit mehreren Enzymen der Glukoseverwertung interagiert, insbesondere mit den Hexokinasen HK1 und HK2. Nachfolgende Tests ergaben, dass diese Interaktion von der katalytischen Aktivität von USP30 abhängt und direkt erfolgt, nicht nur über indirekte Partner.
Ein präziser molekularer Griff an Hexokinase 2
Bei näherer Untersuchung stellten die Forscher fest, dass USP30 bestimmte Arten von Ubiquitin‑Ketten — sogenannte atypische Verknüpfungen — von HK1 und HK2 entfernt. Bei HK2 erfolgt diese Bearbeitung an einer einzelnen entscheidenden Aminosäure, der Lysin‑144 (K144). Wenn K144 so verändert wird, dass es kein Ubiquitin mehr tragen kann, wird HK2 stabiler, bindet stärker an ein Kanalprotein namens VDAC1 auf Mitochondrien und zeigt eine höhere Enzymaktivität. Zellen, die mit dieser K144‑Veränderung konstruiert wurden, sendeten mehr HK2 zu den Mitochondrien, verbrauchten mehr Glukose, setzten mehr Laktat frei und zeigten im Labor schnelleres Wachstum und verstärkte Beweglichkeit. In Mäusen wuchsen Tumore aus Zellen mit der K144‑Mutante größer und schneller als solche mit normaler HK2, was die Wirkung dieses winzigen molekularen Schalters unterstreicht. 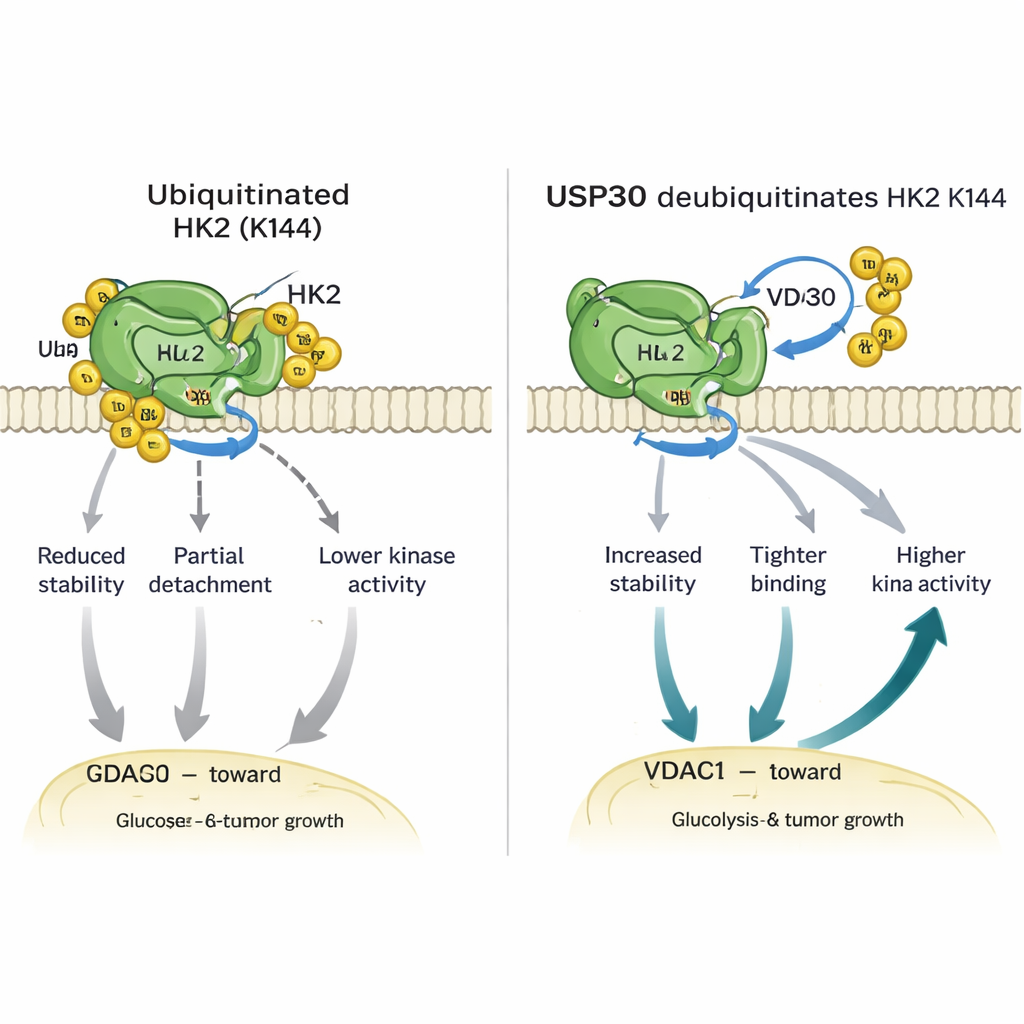
Aus einem metabolischen Schalter einen Wachstumsvorteil machen
Diese Ergebnisse zeichnen eine klare Ereigniskette nach: USP30 bindet an HK2, entfernt Ubiquitin‑Marken von K144 und hält dadurch HK2 aktiv und an den Mitochondrien verankert. Das steigert die Glykolyse, fördert Zellteilung und Migration von Tumorzellen und beschleunigt letztlich das Tumorwachstum. Fehlt USP30 oder ist es inaktiv, wird HK2 weniger stabil und weniger wirksam, und Krebszellen verlieren einen Teil ihres metabolischen Vorteils. Für Laien wirkt USP30 wie ein Mechaniker, der den Zucker‑Motor der Krebszelle gewartet und fest verankert hält — entfernt man den Mechaniker, stottert der Motor.
Was das für künftige Krebstherapien bedeutet
Für Nicht‑Fachleute ist die zentrale Erkenntnis: Krebszellen sind auf eine fein abgestimmte Kontrolle ihrer Zuckerverbrennung angewiesen, und USP30 ist ein neu entdeckter Drehknopf an diesem Steuerpult. Indem USP30 HK2 an einer spezifischen Stelle stabilisiert, unterstützt es den zuckerhungrigen Stoffwechsel von Tumoren und fördert aggressiveres Wachstum. Wirkstoffe, die USP30 blockieren oder seine Bindung an HK2 an Lysin‑144 stören, könnten Tumoren schwächen, indem sie ihren Zucker‑Motor ausbremsen, ohne normale Zellen in gleichem Maße zu schädigen. Diese Arbeit fügt damit ein wichtiges Puzzleteil zum Verständnis hinzu, wie Krebs den Stoffwechsel umprogrammiert, und schlägt einen vielversprechenden Ansatz für gezielte Therapien vor.
Zitation: Haowei, Z., Li, X., Liao, W. et al. USP30-mediated Deubiquitination of Hexokinase 2 controls the metabolic fate of glucose and tumor progression. Cell Death Dis 17, 225 (2026). https://doi.org/10.1038/s41419-026-08459-w
Schlüsselwörter: Krebsstoffwechsel, Glykolyse, Hexokinase 2, USP30, Warburg‑Effekt