Clear Sky Science · de
M5C-vermittelte Stabilisierung von SERPINB5 fördert das Fortschreiten von Gebärmutterhalskrebs und die Chemoresistenz
Warum diese Forschung für Patientinnen wichtig ist
Gebärmutterhalskrebs ist weltweit weiterhin für viele Frauen tödlich, insbesondere wenn er nicht mehr auf standardmäßige Chemotherapeutika wie Paclitaxel und Vincristin anspricht. Diese Studie deckt einen verborgenen molekularen Signalweg in den Tumorzellen auf, der ihr Wachstum, ihre Ausbreitung und ihre Fähigkeit, gängige Behandlungen zu überstehen, fördert. Durch die Aufklärung dieses Weges eröffnet die Arbeit neue Möglichkeiten, vorherzusagen, welche Tumoren therapieresistent sein könnten, und Ziele für Medikamente zu identifizieren, die die Sensitivität wiederherstellen könnten.
Ein chemischer RNA-Aufkleber, der Krebs antreibt
Die meisten Menschen kennen DNA als Träger der genetischen Information, aber Zellen nutzen auch RNA als Arbeitskopie dieser Anweisungen. Die Autoren konzentrierten sich auf einen kleinen chemischen Aufkleber auf RNA namens 5‑Methylcytosin (m5C). Mittels hochauflösender Kartierung in Patientenproben fanden sie heraus, dass Gebärmutterhalskarzinome deutlich mehr dieser m5C‑Markierungen auf ihrer RNA tragen als normales Zervixgewebe. Diese Markierungen kamen besonders häufig in kodierenden Abschnitten der RNA vor und traten gehäuft an Genen auf, die mit Zellwachstum, Invasion und der Fähigkeit der Krebszellen, dem Immunsystem zu entkommen, verbunden sind. Dieses Muster spricht dafür, dass die Tumorzellen ihre RNA‑Chemie umgestalten, um Programme zu verstärken, die die Bösartigkeit fördern.
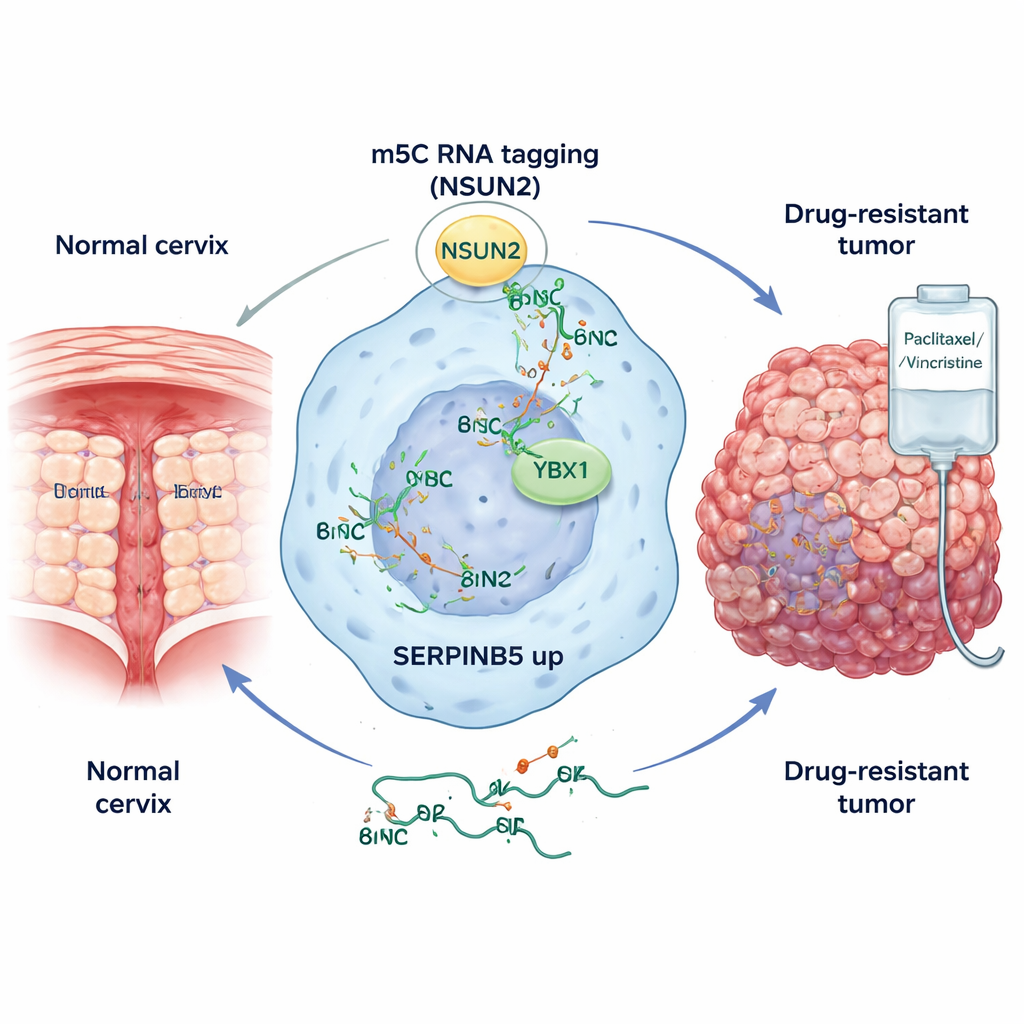
Im Rampenlicht: ein entscheidender Übeltäter — SERPINB5
Um herauszufinden, welche m5C‑markierten RNAs tatsächlich das Tumorverhalten steuern, kombinierte das Team mehrere fortschrittliche Methoden: Bulk‑RNA‑Sequenzierung, räumliche Transkriptomik, die zeigt, wo Gene in einer Tumorscheibe aktiv sind, und Einzelzellsequenzierung, die einzelne Zellen charakterisiert. Anschließend entwickelten sie ein maßgeschneidertes Computermodell, MORGAN, um Kandidatengene zu priorisieren, deren Aktivität mit m5C‑Marken zunimmt. Unter mehreren krebsrelevanten Genen stach eines hervor: SERPINB5, auch Maspin genannt. In Gebärmutterhalskarzinomen wurde SERPINB5 in einer klar abgegrenzten Untergruppe von Tumorzellen stark exprimiert, während es im normalen Gewebe selten vorkam. Diese SERPINB5‑positiven Zellen gruppierten sich in Tumorregionen mit hoher Teilungsaktivität und zeigten Genprofile, die mit DNA‑Replikation, Veränderungen der Zellgestalt und der Fähigkeit zur Umgestaltung des umliegenden Gewebes verbunden sind.
Wie ein Methylierungs‑Schaltkreis SERPINB5 stabilisiert
Die Forscher fragten dann, wie SERPINB5 in Gebärmutterhalskrebs so stark angereichert wird. Sie entdeckten, dass ein Enzym namens NSUN2 maßgeblich dafür verantwortlich ist, m5C‑Marken auf die SERPINB5‑RNA zu schreiben. In Tumorproben und Zelllinien waren die NSUN2‑Spiegel erhöht, und das bevorzugte Sequenzmotiv von NSUN2 stimmte mit den m5C‑Stellen auf SERPINB5‑Transkripten überein. Wurde NSUN2 reduziert oder genetisch ausgeschaltet, wurde die SERPINB5‑RNA weniger stabil und die Proteinspiegel sanken — aber nur, wenn NSUN2 seine katalytische Aktivität verlor. Ein zweites Protein, YBX1, fungierte als molekularer Leser: Es band selektiv an die m5C‑markierte SERPINB5‑RNA und schützte sie zusätzlich vor Abbau. Zusammen bilden NSUN2 und YBX1 einen RNA‑Methylierungs‑Schaltkreis, der SERPINB5‑Spiegel in Tumorzellen hochhält.
Ein Treiber für aggressives Wachstum und Medikamentenresistenz
Funktionelle Tests zeigten, wie entscheidend SERPINB5 für das Tumorverhalten ist. Wenn das Team SERPINB5 in Gebärmutterhalskrebszelllinien reduzierte, teilten sich die Zellen langsamer, migrierten und invasierten weniger und bildeten in Mäusen deutlich kleinere Tumoren. Genanalysen zeigten, dass SERPINB5 Stammzell‑ähnliche Eigenschaften aufrechterhält, die Gefäßbildung unterstützt und Zellen in mobilere, invasivere Zustände überführt. Entscheidend ist, dass SERPINB5 auch die Art und Weise umgestaltet, wie Zellen die Teilung steuern: Es erhöhte die Produktion von Mitose‑Regulatoren und Mikrotubuli‑Motorproteinen wie CENPE, CDK1 und CCNB1, die die Spindelmaschinerie beaufsichtigen, welche die Chromosomen während der Zellteilung auseinanderzieht.
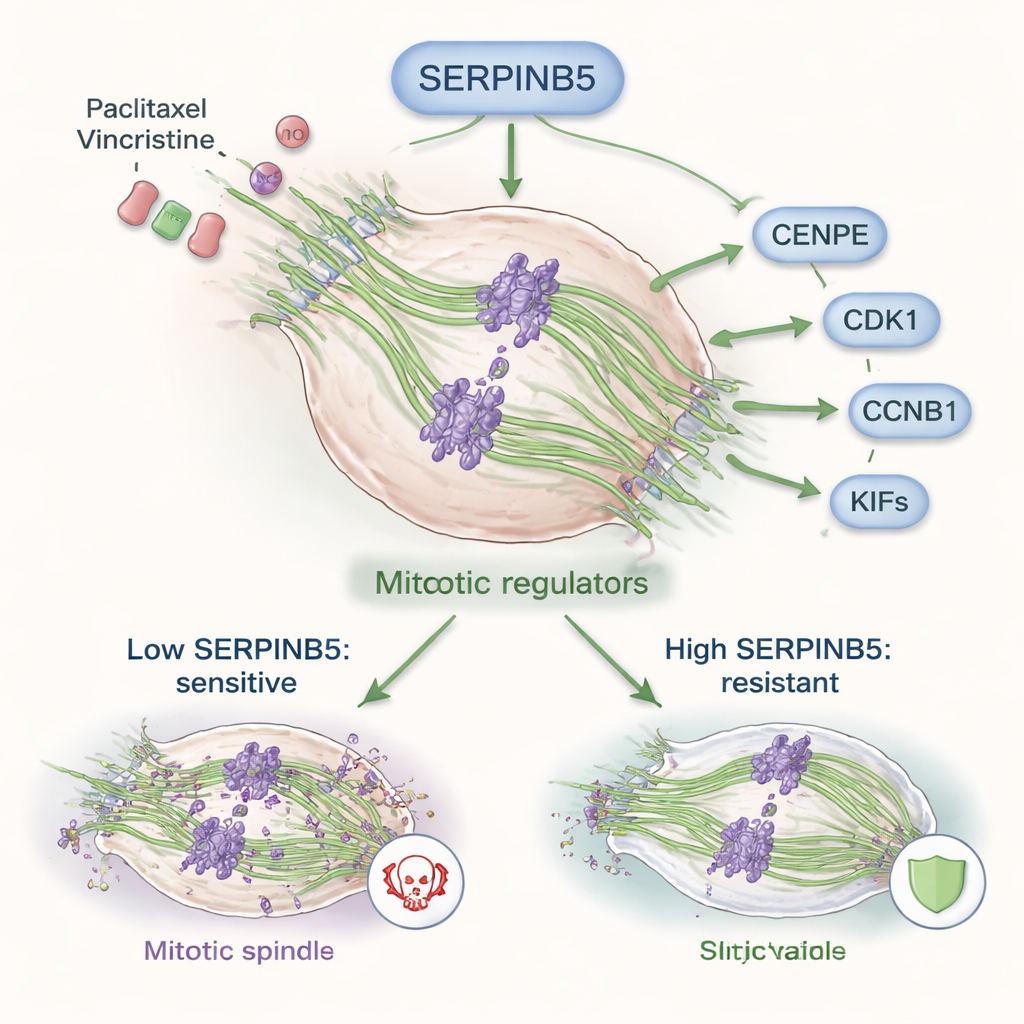
Wie Chemotherapie weniger wirksam wird
Paclitaxel und Vincristin töten Krebszellen hauptsächlich, indem sie Mikrotubuli stören — die strukturellen Fasern, die die Mitose‑Spindel bilden. Durch das Blockieren dieser Maschinerie zwingen die Medikamente die Zellen in einen verlängerten, tödlichen Teilungsstillstand. Die Studie zeigt, dass hohe SERPINB5‑Spiegel den Tumorzellen helfen, diesen Block zu überwinden. Bei Herunterregulierung von SERPINB5 wurden die Zellen empfindlicher gegenüber beiden Wirkstoffen, sodass niedrigere Dosen ausreichten, um die Lebensfähigkeit zu verringern. Derselbe Effekt ergab sich bei Eliminierung von NSUN2, und die Wiedereinführung von SERPINB5 in NSUN2‑defiziente Zellen stellte einen Großteil der Medikamentenresistenz wieder her. Patientenproben von Tumoren, die auf Paclitaxel‑basierte Therapien versagten, zeigten ebenfalls höhere SERPINB5‑Proteinspiegel als medikamentensensitive Tumoren, was die klinische Relevanz unterstreicht.
Was das für zukünftige Therapien bedeutet
Für eine allgemeine Leserschaft lautet die Kernbotschaft: Manche Gebärmutterhalskarzinome überleben und wachsen, indem sie eine einzelne, einflussreiche RNA und ihr Proteinprodukt, SERPINB5, mithilfe eines chemischen Markierungssystems auf RNA schützen. Diese NSUN2–YBX1–SERPINB5‑Achse wirkt wie ein molekularer Schild, der Tumoren hilft, sich rasch zu teilen und gegen Standard‑Chemotherapien, die Mikrotubuli angreifen, resistent zu sein. Das Anvisieren dieser Achse — durch Hemmung von NSUN2, Blockierung der YBX1‑Bindung, direkte Senkung von SERPINB5 oder die Nutzung von SERPINB5 als Biomarker — könnte Standardmedikamente wirksamer machen und dabei helfen, Patientinnen zu identifizieren, die am ehesten von spezifischen Behandlungen profitieren.
Zitation: Liu, J., Zhou, L., Yao, P. et al. M5C-driven stabilization of SERPINB5 promotes cervical cancer progression and chemotherapy resistance. Cell Death Dis 17, 215 (2026). https://doi.org/10.1038/s41419-026-08453-2
Schlüsselwörter: Gebärmutterhalskrebs, Chemoresistenz, RNA-Methylierung, SERPINB5, NSUN2