Clear Sky Science · de
Ringförmige RNAs in der metabolischen Gesundheit: die Lücke zwischen Molekularbiologie und Therapie überbrücken
Warum winzige RNA‑Schleifen für Gewicht und Gesundheit wichtig sein könnten
Adipositas wird oft als ein einfaches Problem von Willenskraft und Kalorien dargestellt, doch viele Menschen kämpfen trotz Diät und Bewegung. Dieser Artikel erklärt, wie eine neu erkannte Klasse genetischer Moleküle — ringförmige RNAs oder circRNAs — mitbestimmt, ob unsere Fettzellen Energie speichern oder verbrennen. Indem sie weißes „Speicher“fett in braunes, wärmeproduzierendes Fett verwandeln, könnten diese RNA‑Schleifen eines Tages präzisionsmedizinische Behandlungen für Adipositas und damit verbundene Erkrankungen wie Typ‑2‑Diabetes oder Fettleber anregen.
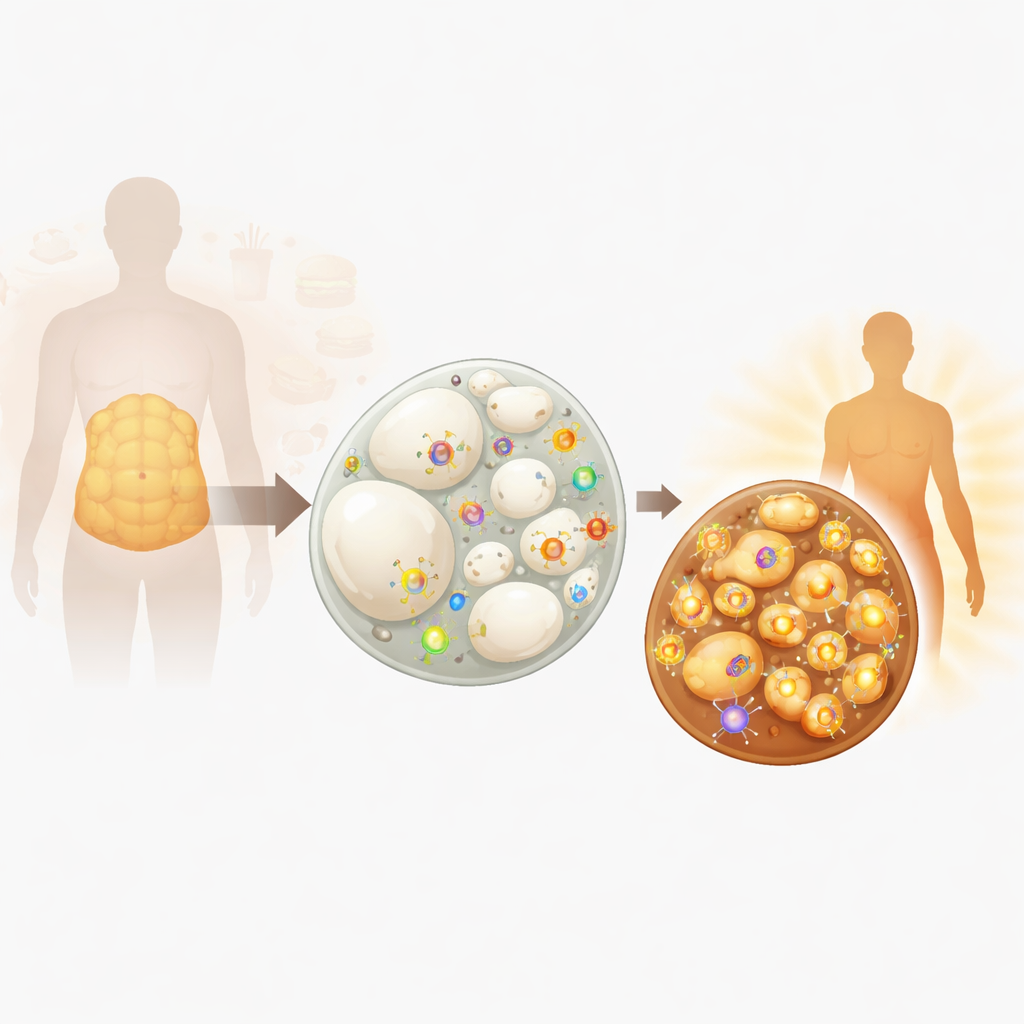
Die zwei Gesichter des Körperfetts
Nicht jedes Körperfett verhält sich gleich. Weißes Fett, das Organe polstert und sich vor allem am Bauch anlagert, dient hauptsächlich als Energiespeicher: Seine Zellen enthalten einen großen Fetttropfen und relativ wenige Mitochondrien, die Kraftwerke der Zelle. Braunes Fett, konzentriert im oberen Rücken und Nacken, ist reich an Mitochondrien, die Brennstoff verbrennen, um Wärme zu erzeugen — das hilft uns warm zu halten und begrenzt Gewichtszunahme. Unter bestimmten Bedingungen — etwa Kälteeinwirkung, Überessen oder durch Trainingssignale — kann weißes Fett in „beiges“ Fett umbauen, einen Zwischenzustand, der die Fähigkeit des braunen Fetts erwirbt, Kalorien zu verbrennen. Dieses Umbauprogramm, genannt Fettbräunung, gilt inzwischen als vielversprechender Ansatz zur Bekämpfung metabolischer Erkrankungen.
Was ringförmige RNAs besonders macht
RNA wird normalerweise als gerader Strang verstanden, der genetische Anweisungen von der DNA zu Proteinen trägt. CircRNAs widersprechen diesem Lehrbuchbild: Ihre Enden sind verbunden und bilden Schleifen. Diese geschlossene Ringstruktur macht sie ungewöhnlich stabil, sodass sie in Zellen und sogar im Blut und anderen Körperflüssigkeiten überdauern können. Weit davon entfernt, genetischer „Müll“ zu sein, können circRNAs MikroRNAs binden (kleine Regulatoren, die Gene stilllegen), bestimmte Proteine andocken, beeinflussen, wie Gene ein- oder ausgeschaltet werden, und in einigen Fällen sogar die Produktion kurzer Peptide steuern. Da bestimmte circRNAs in Fettgewebe angereichert sind und auf Ernährung und Hormone reagieren, treten sie als Schlüsselkoordinatoren dafür hervor, wie Fettzellen Energie nutzen und speichern.
Wie ringförmige RNAs weißes Fett in braunes lenken
In braunem und beigem Fett ändern viele circRNAs ihre Aktivität im Vergleich zu weißem Fett. Einige wirken wie molekulare Schwämme und binden MikroRNAs, die ansonsten Gene blockieren würden, die für den Fettabbau oder den Aufbau von Mitochondrien notwendig sind. Beispielsweise befreien bestimmte circRNAs Gene, die Lipolyse (Fettabbau) antreiben oder Signalwege wie AMPK und mTOR aktivieren, die umprogrammieren, wie Zellen mit Zucker und Fetten umgehen. Andere binden direkt Proteine, die die Fettsynthese, -oxidation oder Wärmeerzeugung steuern, stabilisieren hilfreiche Enzyme oder lenken sie zu neuen Aufgaben. Eine wachsende Zahl von circRNAs kodiert sogar kleine Peptide, die die Mitochondrienfunktion feinjustieren oder den Stoffwechsel so verändern, dass weiße Fettzellen zu einem bräuneren, energiehungrigeren Zustand tendieren.
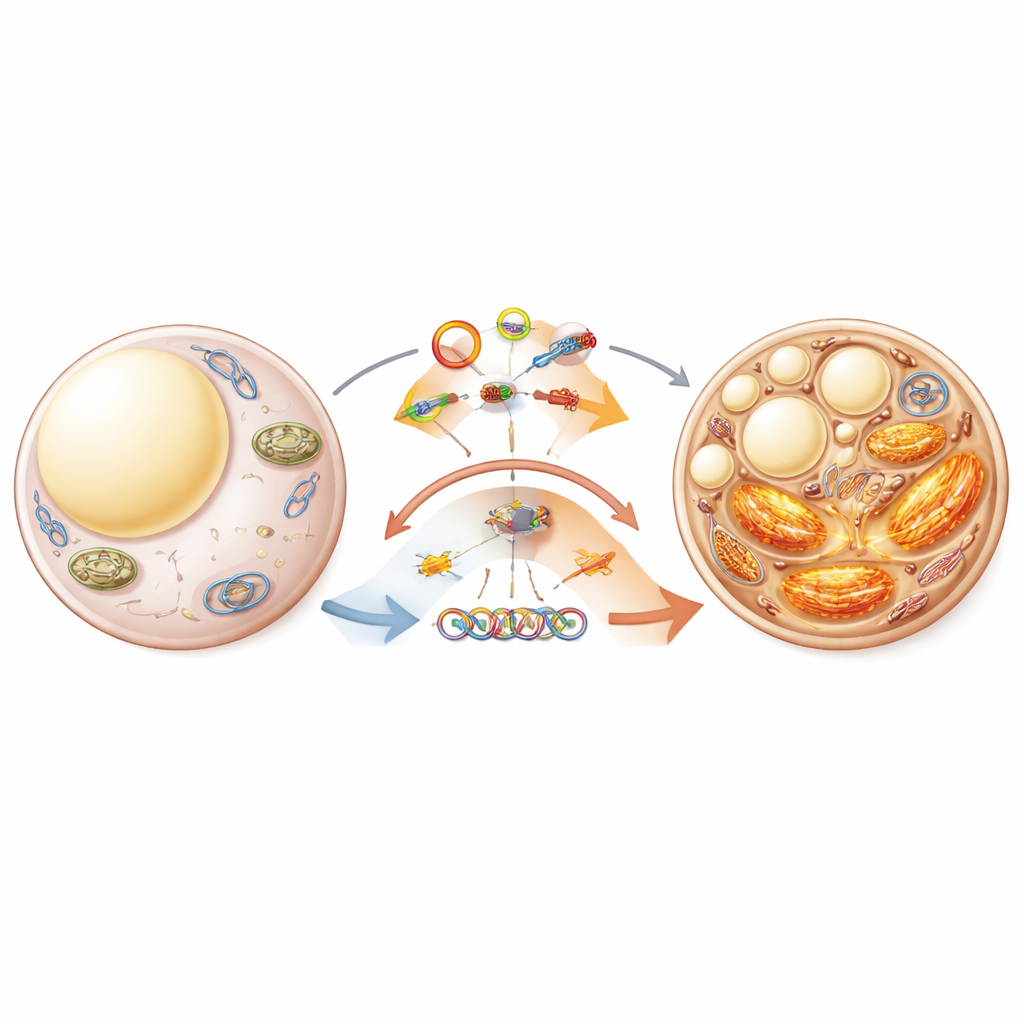
Die Kraftwerke der Zelle und Stresssysteme justieren
Die Fettbräunung hängt stark von Mitochondrien und dem endoplasmatischen Retikulum ab, einem Membrannetzwerk, das hilft, Stress in Zellen zu bewältigen. Der Übersichtsartikel hebt hervor, wie circRNAs diese inneren Strukturen beeinflussen. Einige circRNAs schützen Mitochondrien, indem sie die geordnete Entfernung beschädigter Organellen fördern, während andere dieses Aufräumen hoch- oder herunterregulieren, indem sie mit Proteinen an der mitochondrialen Oberfläche interagieren. CircRNAs prägen auch, wie das endoplasmatische Retikulum auf Überlast reagiert, was das Bräunungsprogramm entweder blockieren oder unterstützen kann. Da Mitochondrien und das endoplasmatische Retikulum physisch und funktionell zusammenarbeiten, könnten circRNAs, die an diesem Schnittpunkt wirken, als Schaltstellen dienen, ob Fettzellen Energie anhäufen oder als Wärme verbrennen.
Von der Laborentdeckung zu künftigen Therapien
Dank ihrer Haltbarkeit und Präzision gewinnen circRNAs Aufmerksamkeit als diagnostische Marker, Wirkstoffziele und sogar als therapeutische Moleküle selbst. Ingenieurmäßig hergestellte circRNAs können so konstruiert werden, dass sie nützliche Peptide produzieren, die Genaktivität anpassen oder als langanhaltende Impfstoffe dienen, und es werden Nanopartikel‑ oder Exosomträger entwickelt, um sie in Gewebe wie Fett und Leber zu bringen. Der Artikel mahnt jedoch, dass viele circRNAs zwischen Arten unterschiedlich sind, Liefermethoden noch grob sind und die Langzeitsicherheit unbekannt ist. Insgesamt argumentieren die Autoren, dass das Verstehen und Nutzen von circRNAs einen Weg eröffnet, über rein kalorienbasierte Sichtweisen auf Adipositas hinauszukommen und Behandlungen zu entwickeln, die unsere Fettzellen dazu „umschulen“, mehr wie braunes Fett zu funktionieren und das metabolische Gleichgewicht wiederherzustellen.
Zitation: Huang, Y., He, T., Zheng, J. et al. Circular RNAs in metabolic health: bridging the gap between molecular biology and therapy. Cell Death Dis 17, 258 (2026). https://doi.org/10.1038/s41419-026-08450-5
Schlüsselwörter: ringförmige RNA, Fettbräunung, Adipositas, metabolische Erkrankung, braunes Fettgewebe