Clear Sky Science · de
Oozytenspezifischer Knockout von eIF2-Untereinheiten verursacht Apoptose von Maus-Oozyten in frühen wachsenden Follikeln durch mitochondriale Dysfunktionen und DNA-Schäden
Warum das Leben der Eizellen wichtig ist
Frauen werden mit allen Eizellen geboren, die sie jemals haben werden, gespeichert in winzigen Strukturen im Eierstock, den sogenannten Follikeln. Gehen diese Follikel zu schnell verloren, kann sich eine vorzeitige Ovarialinsuffizienz (POI) entwickeln — ein Zustand, der zu früher Unfruchtbarkeit und oft zu menopausenähnlichen Symptomen in jungem Alter führt. Diese Studie an Mäusen stellt eine grundlegende, aber zentrale Frage: Was geschieht in Eizellen, wenn ein wichtiger Schritt bei der Proteinsynthese gestört ist, und wie kann das zum vorzeitigen Verlust der Fruchtbarkeit führen?
Der Schalter für den Start der Proteinproduktion
Damit Eizellen gesund bleiben, müssen sie ständig die richtigen Proteine zur richtigen Zeit herstellen. Ein zentraler Bestandteil dieses Prozesses ist eine dreiteilige molekulare Maschine namens eIF2, die den Start der Proteinproduktion aus genetischen Botschaften unterstützt. Die Forschenden schalteten gezielt zwei Untereinheiten von eIF2 aus, genannt eIF2α und eIF2β, und zwar ausschließlich in Maus-Oozyten in frühen Stadien des Follikelwachstums. Fehlte eine dieser Untereinheiten, wurden die weiblichen Mäuse vollständig unfruchtbar. Ihre Eierstöcke waren verkleinert, und der normale Übergang von frühen Follikeln zu reifen, ovulationsbereiten Follikeln blieb weitgehend stehen; in allen späteren Stadien gab es deutlich weniger Follikel. Mit der Zeit waren praktisch alle Follikel aufgebraucht, was einen schweren, früh einsetzenden POI-ähnlichen Zustand nachahmte.
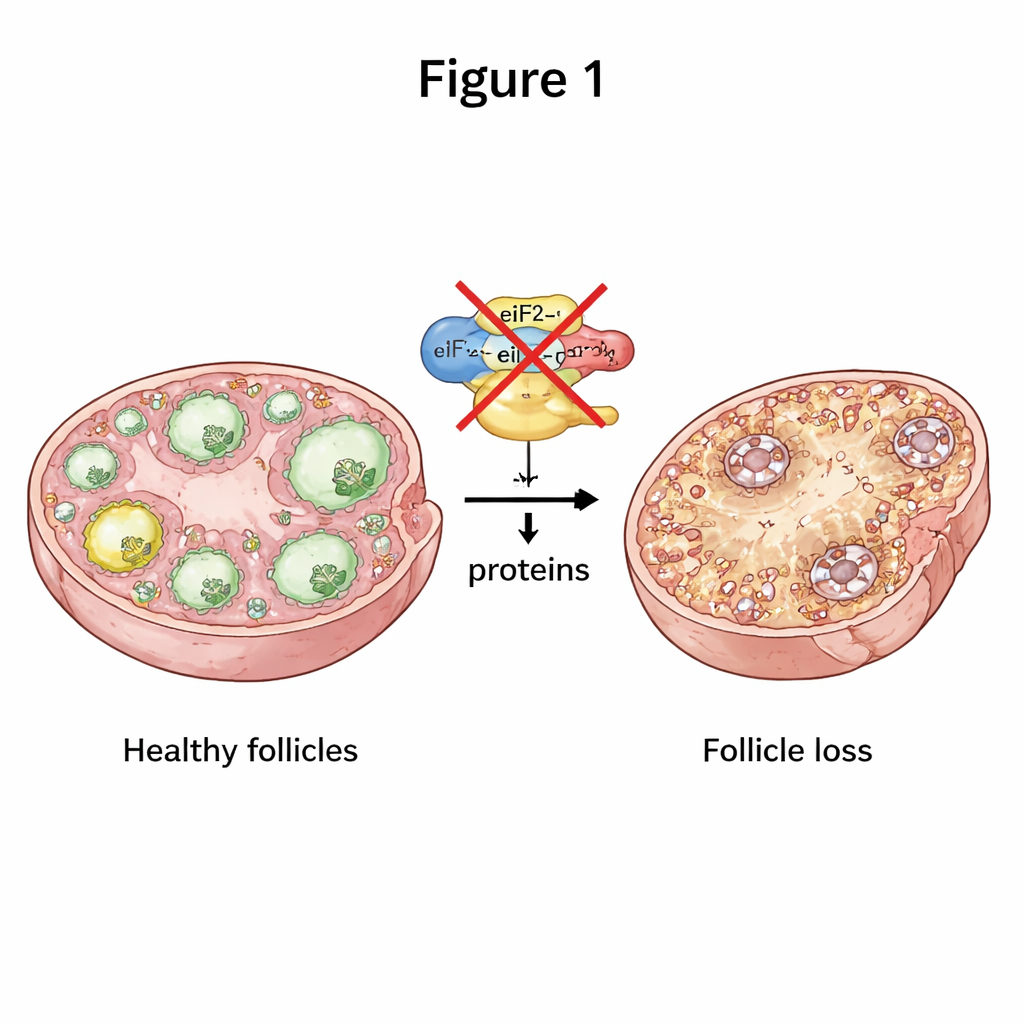
Wenn die Kommunikation im Eierstock zusammenbricht
Follikel sind nicht einfach einzelne Eizellen; sie sind enge Partnerschaften zwischen einer Eizelle und den sie umgebenden „Hilfs“-Zellen, den Granulosazellen. Das Team stellte fest, dass Oozyten ohne eIF2β deutlich weniger von mehreren wichtigen Signalproteinen produzierten, die normalerweise das Wachstum der Granulosazellen und die Nährstoffversorgung unterstützen. Die physischen Brücken zwischen Oozyten und Granulosazellen waren desorganisiert und verkürzt, und die Mikrovilli auf der Eizelloberfläche wirkten unter dem Elektronenmikroskop gestutzt und beschädigt. Granulosazellen in diesen Follikeln teilten sich weniger und starben häufiger. Dieser Zusammenbruch der bidirektionalen Kommunikation verhinderte das richtige Wachstum der Follikel und trieb den Eierstock in Richtung Follikelverlust.
Stromausfall in den Batterien der Eizelle
Mitochondrien, oft als Kraftwerke der Zelle bezeichnet, sind für Eizellen besonders wichtig, weil sie die Energie liefern, die für Wachstum und später für die Embryonalentwicklung benötigt wird. In eIF2β-defizienten Oozyten sank die allgemeine Rate der Neuproteinproduktion, und viele mitochondrienbezogene Proteine waren vermindert. Mitochondrien wurden ungewöhnlich lang, klumpten an der Zelloberfläche und zeigten ein geschwächtes Membranpotenzial, niedrigere Energiewerte (ATP) und weniger Kopien der mitochondrialen DNA. Gleichzeitig sammelten die Zellen hohe Mengen reaktiver Sauerstoffspezies (ROS) an — aggressive sauerstoffbasierte Moleküle, die zelluläre Komponenten schädigen können. Zusammengenommen zeigen diese Veränderungen einen tiefgreifenden Zusammenbruch der mitochondrialen Dynamik und Funktion.
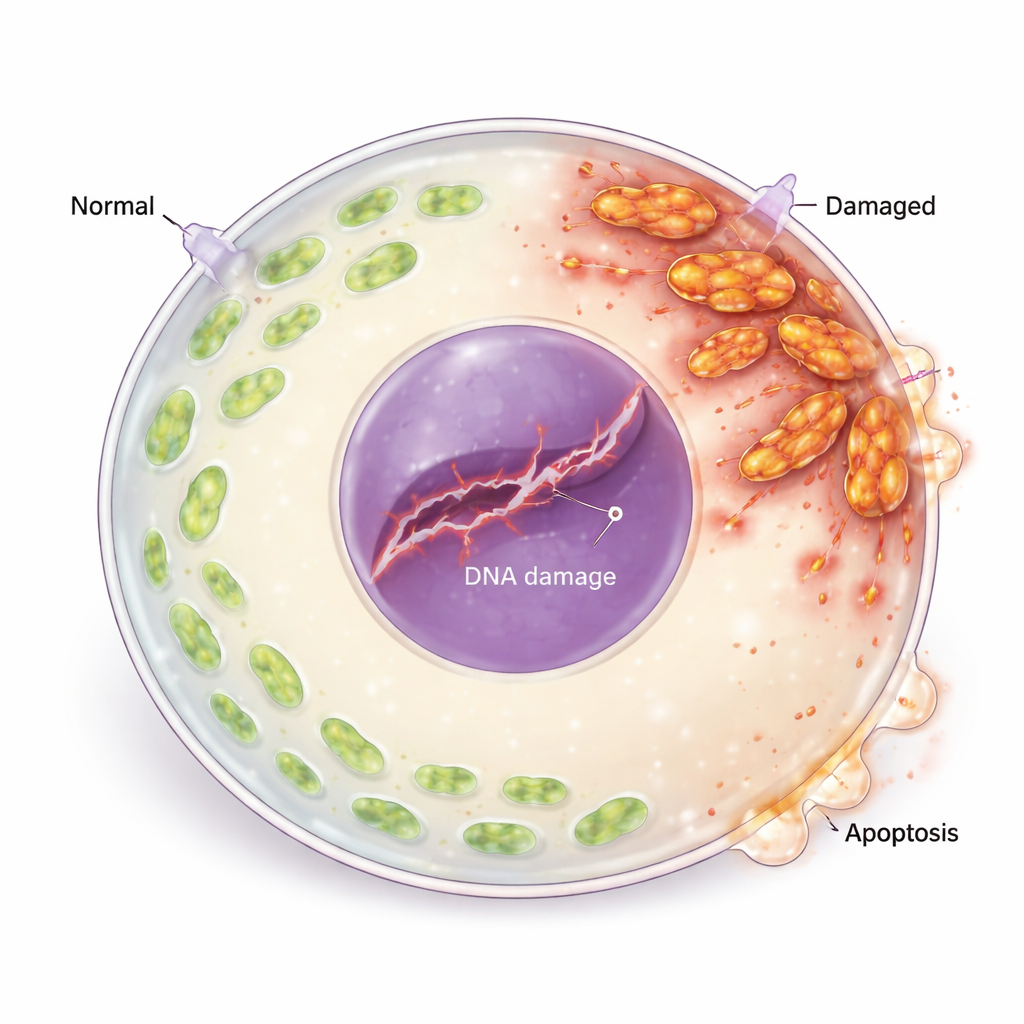
Von oxidativem Stress zu DNA-Schäden und Zelltod
Überschüssige ROS schadeten nicht nur den Mitochondrien; sie verletzten auch das genetische Material der Eizelle. Die Forschenden beobachteten vermehrte Marker für gebrochene DNA-Stränge und die Aktivierung der DNA-Schadensantwort der Zelle, einschließlich Proteinen, die genetische Verletzungen erkennen und signalisieren. Ein wichtiges Reparaturprotein war vermindert, was darauf hindeutet, dass die Schäden nicht effizient behoben wurden. Im weiteren Verlauf verschob sich das Gleichgewicht der Lebens‑und‑Tods‑Regulatoren: pro‑apoptotische Proteine stiegen, während schützende anti‑apoptotische Proteine fielen, und die Oozyten zeigten klare Anzeichen programmierter Zelltods (Apoptose). Behandelten die Forschenden die Oozyten mit einem Antioxidans (N‑Acetylcystein), sanken ROS‑Werte, DNA‑Schäden und Apoptosemarker nahmen ab, und die Eizellreifung verbesserte sich — ein direkter Zusammenhang zwischen oxidativem Stress und Eizellverlust.
Was das für den vorzeitigen Eierstocksversagen bedeutet
Indem die Studie den Weg von einem einzelnen molekularen Komplex (eIF2) über fehlerhafte Proteinsynthese, mitochondrialen Zusammenbruch, oxidativen Stress und DNA‑Schäden bis hin zum Untergang der Eizellen nachzeichnet, liefert sie eine detaillierte Kausalkette, die das ovarielle Reservevermögen zerstören kann. Die Arbeit stützt die Idee, dass Mutationen in Faktoren, die den Start der Translation steuern — wie sie bereits bei einigen Frauen mit POI gefunden wurden — direkt Oozyten über diesen Mechanismus schädigen können. Sie weist auch auf mögliche therapeutische Ansätze hin: Antioxidanzien, Modulatoren der Stressantwort oder Behandlungen, die frühe Follikel schützen (wie das anti‑Müller‑Hormon, das in diesen Mäusen teilweise ruhende Follikel bewahrte), könnten eines Tages die Fruchtbarkeit von Patientinnen unterstützen, deren Eierstöcke für ähnliche Belastungen anfällig sind.
Zitation: Liu, H., Wang, W., Li, B. et al. Oocyte-specific knockout of eIF2 subunits causes apoptosis of mouse oocytes within the early growing follicles via mitochondrial dysfunctions and DNA damage. Cell Death Dis 17, 196 (2026). https://doi.org/10.1038/s41419-026-08449-y
Schlüsselwörter: vorzeitige Ovarialinsuffizienz, Oozytenapoptose, mitochondriale Dysfunktion, Proteinsynthese, reaktive Sauerstoffspezies