Clear Sky Science · de
Transglutaminase 2 verschlechtert das Überleben bei Eierstockkrebs, indem es GSK3β direkt inaktiviert
Warum diese Forschung für die Gesundheit von Frauen wichtig ist
Eierstockkrebs zählt zu den tödlichsten Krebserkrankungen bei Frauen, weil er meist erst spät entdeckt wird und häufig selbst nach intensiver Chemotherapie zurückkehrt. Diese Studie deckt auf, wie ein wenig bekanntes Protein, Transglutaminase 2 (TGase 2), Eierstockkrebszellen hilft, Behandlungen zu überstehen und sich im Körper auszubreiten. Indem sie diesen verborgenen Helfer des Tumors offenlegt, weist die Arbeit auf neue Wege hin, bestehende Medikamente wirksamer zu machen und tödliche Metastasen zu verlangsamen oder zu stoppen.
Ein verborgener Treiber in aggressiven Tumoren
Ärztinnen und Ärzte beobachten seit langem, dass viele Eierstocktumoren chemoresistent werden und sich weit im Bauchraum ausbreiten. Ein wichtiger Verursacher ist die sogenannte epithelial–mesenchymale Transition (EMT): Dabei lösen Tumorzellen ihre Verbindungen, werden beweglicher und verhalten sich eher wie invasive „Wanderer“ als wie geordnete Gewebezellen. Die Autoren zeigen, dass TGase 2, das im normalen Eierstock sehr niedrig exprimiert wird, in Tumoren deutlich erhöht ist und eng mit diesem Wechsel verbunden ist. In einer großen Anzahl menschlicher Gewebeproben stiegen die TGase-2-Spiegel kontinuierlich von Frühstadien zu fortgeschrittenen und metastasierten Erkrankungen an, und ihre Menge korrelierte eng mit der Aktivität zahlreicher EMT-bezogener Gene, die Zellbewegung, Wachstum und Gefäßbildung steuern. 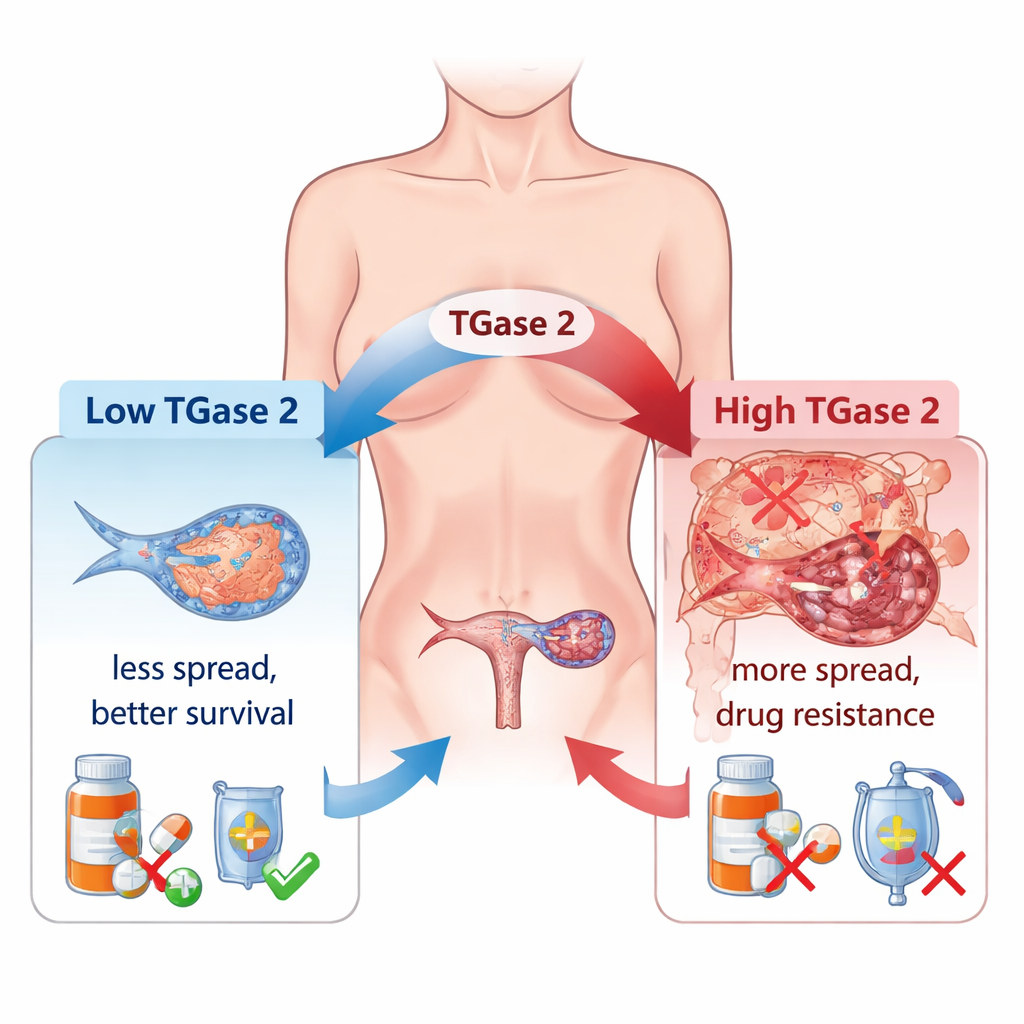
Wie TGase 2 einen wichtigen Sicherheitsmechanismus umlegt
Um zu verstehen, was TGase 2 in Tumorzellen tatsächlich bewirkt, konzentrierten sich die Forschenden auf seine Beziehung zu einem anderen Protein, GSK3β. Unter gesunden Bedingungen wirkt GSK3β wie eine Bremse gegen Invasion: Es hält die Konzentration des Signalmoleküls β‑Catenin niedrig, wodurch Gene, die EMT antreiben, zurückgehalten werden. Das Team entdeckte, dass TGase 2 physisch an GSK3β bindet, dessen Aktivität abschwächt und dessen Abbau über das zelluläre Recycling-System, die Autophagie, fördert. Bei hoher TGase‑2‑Expression wanderten Eierstockkrebszellen leichter und zeigten höhere Werte klassischer EMT‑Marker wie Fibronectin, Vimentin und β‑Catenin. Wurde TGase 2 mithilfe genetischer Werkzeuge reduziert, nahmen diese invasiven Eigenschaften ab und die β‑Catenin‑Signalgebung wurde gedämpft, was zeigt, dass TGase 2 einen entscheidenden Sicherheitsmechanismus gegen Metastasen außer Kraft setzt.
Von Tumorzellen zu lebenden Tieren
Als Nächstes prüfte das Team, ob die Blockade von TGase 2 das Krebswachstum in Tieren verlangsamen kann. Sie erzeugten Eierstockkrebszellen ohne TGase‑2‑Gen und transplantierten diese in Mäuse. Im Vergleich zu Mäusen, die normale Tumorzellen erhielten, entwickelten Tiere mit TGase‑2‑defizienten Zellen geringere Tumorlasten und lebten länger. In einem separaten Modell, das die Blutbahn‑vermittelte Ausbreitung des Tumors simuliert, entwickelten Mäuse, die mit TGase‑2‑defizienten Zellen injiziert wurden, deutlich weniger und kleinere Lungenmetastasen. Wichtig: Diese metastatischen Herde wiesen höhere GSK3β‑Spiegel auf, was zur Idee passt, dass das Entfernen von TGase 2 die natürliche Bremse gegen Invasion wiederherstellt und dazu beiträgt, die Erkrankung einzudämmen.
Aus einem Laborhinweis eine Arzneistrategie machen
Da das Entfernen eines Gens bei Patientinnen nicht praktikabel ist, testeten die Autoren ein kleines Molekül namens Streptonigrin, das dafür bekannt ist, an dasselbe Ende von TGase 2 zu binden, mit dem es andere Proteine greift. Sie fanden, dass Streptonigrin die TGase‑2–GSK3β‑Interaktion in Zellen stören, ihre Ko- Lokalisierung verringern und die Wanderung von Krebszellen einschränken kann. In Mausmodellen des Eierstockkrebses verlangsamte orale Behandlung mit Streptonigrin das Tumorwachstum, verkleinerte metastatische Herde und verlängerte das Überleben. Am eindrücklichsten war, dass Mäuse, die Streptonigrin zusammen mit Standard-Chemotherapeutika wie Cisplatin oder Paclitaxel erhielten, deutlich länger lebten als bei alleiniger Chemotherapie. Alleinige Chemotherapie erhöhte tendenziell die TGase‑2‑Spiegel und senkte GSK3β, was die Zellen indirekt in Richtung EMT drängte; die Zugabe des TGase‑2‑Blockers kehrte diesen Trend jedoch um und bremste die neu gewonnene Mobilität der Zellen. 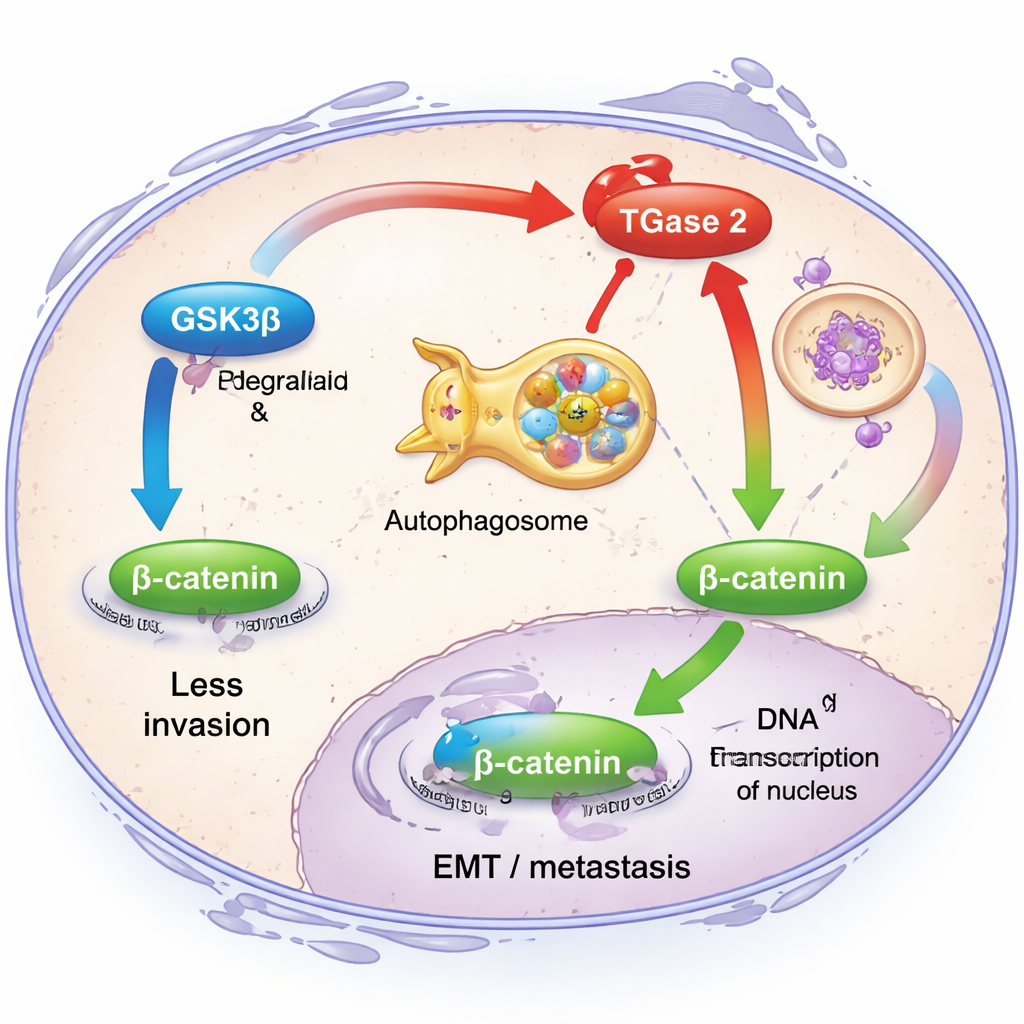
Was das für zukünftige Behandlungen bedeuten könnte
Für Nicht-Fachleute lautet die Kernaussage: Eierstockkrebszellen nutzen TGase 2, um eine eingebaute Anti‑Metastasen‑Bremse auszuschalten und die Stürme einer Chemotherapie zu überstehen. Indem TGase 2 GSK3β direkt inaktiviert und β‑Catenin stabilisiert, fördert es die Invasivität und Medikamentenresistenz von Tumoren. Die Arbeit legt nahe, dass Wirkstoffe, die an die N‑terminale Region von TGase 2 gerichtet sind – wie Streptonigrin oder künftig sicherere, darauf basierende Verbindungen – bestehende Chemotherapien wirksamer machen, Rückfälle seltener und das Überleben verbessern könnten. Einfach gesagt: TGase‑2‑Hemmung könnte eine „Fluchtroute“ des Krebses abschneiden und Eierstocktumoren empfindlicher gegenüber Therapien und weniger ausbreitungsfreudig halten.
Zitation: Lee, H., Kang, J.H., Kim, H.J. et al. Transglutaminase 2 exacerbates ovarian cancer survival by directly inactivating GSK3β. Cell Death Dis 17, 199 (2026). https://doi.org/10.1038/s41419-026-08447-0
Schlüsselwörter: Eierstockkrebs, Medikamentenresistenz, Metastasierung, epithelial-mesenchymale Transition, gezielte Therapie