Clear Sky Science · de
Hemmung der autoantigeninduzierten Internalisierung des B‑Zell‑Rezeptors (BCR) als therapeutische Strategie beim diffus großzelligen B‑Zell‑Lymphom (DLBCL)
Warum das für Patientinnen und Patienten wichtig ist
Das diffuse großzellige B‑Zell‑Lymphom (DLBCL) ist die häufigste schnell wachsende Blutkrebserkrankung bei Erwachsenen, und viele Patientinnen und Patienten erleiden trotz standardmäßiger Chemo‑Immuntherapie ein Rezidiv. Diese Studie untersucht eine überraschende Verwundbarkeit in einer wichtigen Untergruppe dieser Tumoren: ihre Abhängigkeit von einer zelloberflächengetragenen Antenne, dem B‑Zell‑Rezeptor (BCR). Indem gezeigt wird, dass das Blockieren der Aufnahme dieser Antenne in die Zelle das Überleben der Krebszellen stark beeinträchtigen kann, eröffnet die Arbeit die Möglichkeit, langjährig eingesetzte Anti‑Übelkeits‑ und Antipsychotika als zielgerichtete Unterstützer gegen Lymphome umzunutzen.
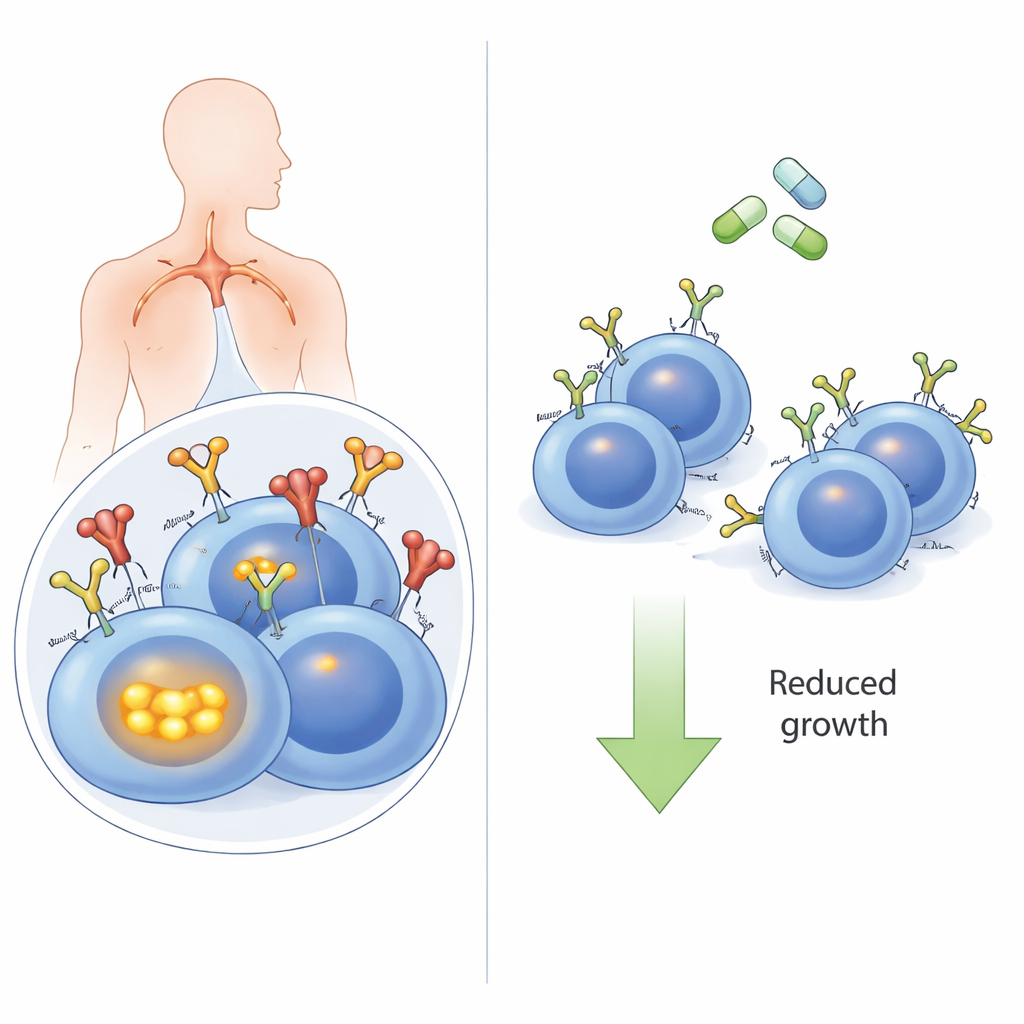
Die Antenne der Krebszelle
B‑Zellen, eine Art weißer Blutkörperchen, nutzen den B‑Zell‑Rezeptor auf ihrer Oberfläche zur Erkennung von Bedrohungen. In vielen DLBCLs, insbesondere im risikoreichen „activated B‑cell“ (ABC) Subtyp, wird dieser Rezeptor missbraucht, um dauerhafte „bleib am Leben und wachse“-Signale zu senden. Häufig erkennen diese BCRs körpereigene Moleküle (Autoantigene), die wie eine klemmende Türklingel wirken. Bindet ein Autoantigen, tut der BCR mehr, als nur an der Oberfläche zu signalisieren: er wird in die Zelle hinein gezogen und schließt sich einem internen Proteinverbund mit Sensoren wie TLR9 und MYD88 an. Dieser Superkomplex schaltet dann NFκB ein, einen starken wachstumsfördernden Signalweg. Bislang war unklar, ob diese nach innen gerichtete Reise des Rezeptors tatsächlich für die krebsfördernden Signale erforderlich ist.
Die Antenne umbauen, um ihre Grenzen zu testen
Um diese Frage zu klären, setzten die Forschenden CRISPR‑Geneditierung ein, um die „Spitzen“ des BCR in Lymphomzelllinien präzise zu verändern. Sie ersetzten die natürlichen, selbstreaktiven Erkennungsregionen durch Versionen, die Ovalbumin erkennen, ein harmloses Hühnereiweiß, das als Laborwerkzeug dient. Diese modifizierten Rezeptoren fassten nicht mehr ihre üblichen Autoantigene an, konnten aber weiterhin in einer kontrollierten Weise durch zugegebenes Ovalbumin ausgelöst werden. In ABC‑Lymphomzellen, die normalerweise von Selbstantigenbindung abhängig sind, reduzierte dieser Wechsel die Aktivität vieler wichtiger Signalkinasen deutlich und dämpfte NFκB‑abhängige Gene. Die Zellen wuchsen langsamer, obwohl tatsächlich mehr BCR an ihrer Oberfläche vorhanden war, was zeigt, dass anhaltende Engagements durch Autoantigene und die anschließende interne Signalgebung für ihr Überleben kritisch sind.
Rezeptoren hineinzuziehen: ein entscheidender Schritt
Das Team untersuchte anschließend direkt, was mit dem BCR geschieht, nachdem es sein Antigen trifft. In ihren konstruierten Modellen verschwanden sowohl durch Antikörper ausgelöste als auch durch Ovalbumin induzierte Rezeptoren innerhalb von Minuten von der Zelloberfläche, was eine schnelle Internalisierung bestätigte. Dies geschah nicht nur, wenn das Antigen außerhalb der Zelle vorlag, sondern auch, wenn es künstlich auf der Membran derselben Zelle dargestellt wurde, was bestimmte reale Tumorsituationen nachahmt. Blockierte man diesen nach innen gerichteten Verkehr genetisch, etwa durch eine dominant‑negative Form des Proteins Dynamin‑2, das für die clathrinvermittelte Endozytose essenziell ist, verblieben BCR an der Oberfläche, die internen BCR–TLR9–NFκB‑Komplexe schrumpften, NFκB‑Zielgene wurden reduziert und das Zellwachstum verlangsamte sich. Interessanterweise stiegen bei blockierter Endozytose einige „Hintergrund“‑BCR‑Signale an der Oberfläche, was darauf hindeutet, dass Krebszellen versuchen könnten, durch Hochregulierung eines schwächeren, tonischen Signalmodus zu kompensieren.
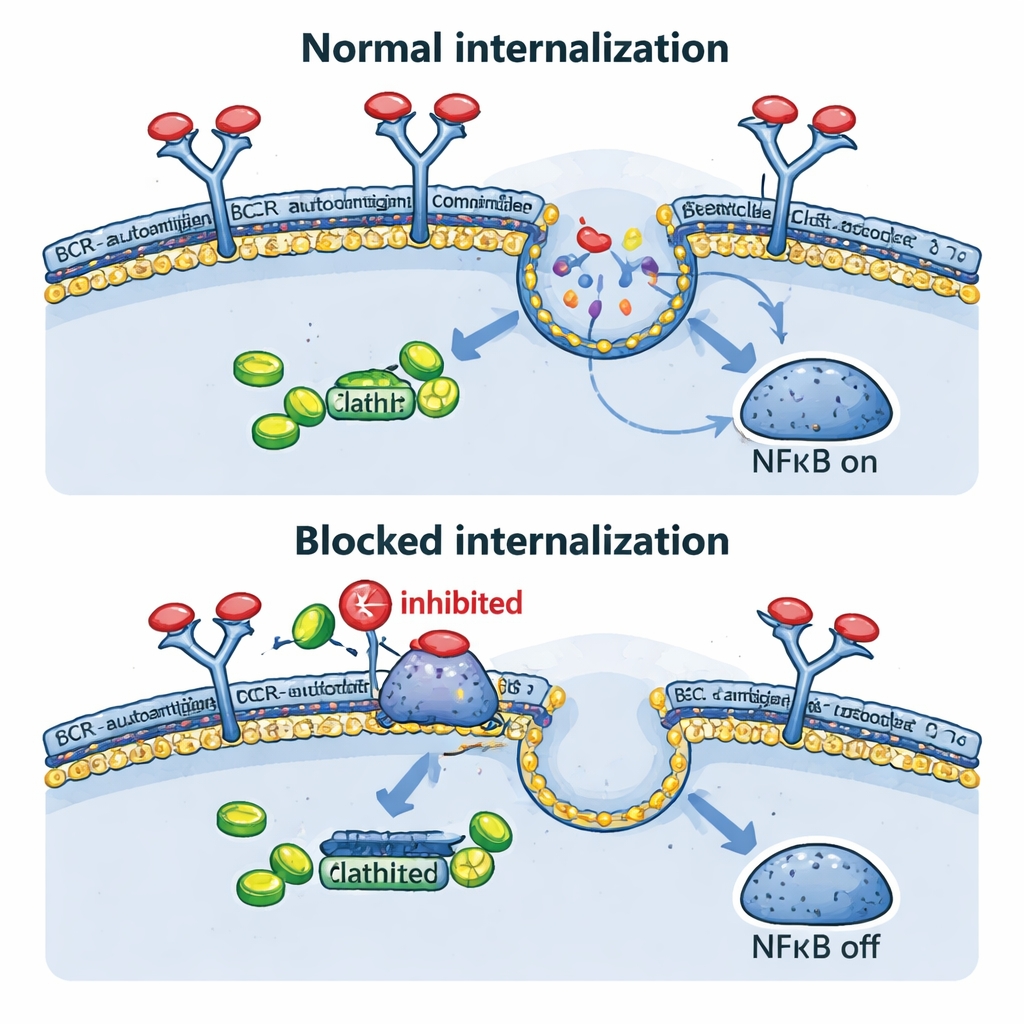
Alte Medikamente, neue Tricks
Da die Entwicklung neuer Medikamente langsam und teuer ist, fragten die Autorinnen und Autoren als Nächstes, ob bestehende Medikamente, die die Endozytose blockieren, die genetischen Experimente nachahmen könnten. Phenothiazine, eine Gruppe von Antipsychotika und Anti‑Übelkeitsmitteln, sind dafür bekannt, Dynamin‑2 und clathrinabhängige Aufnahme von Rezeptoren zu hemmen. In Lymphomzellen führten Verbindungen wie Prochlorperazin und Chlorpromazin zu erhöhten BCR‑Spiegeln an der Oberfläche und reduzierten die antigengetriebene Internalisierung deutlich. Dies führte zu verringerter NFκB‑getriebener Genaktivität und verminderter Lebensfähigkeit von ABC‑Typ DLBCL‑Zellen, insbesondere bei Zellen mit intakten BCR‑Komponenten. In Mäusen mit humanen Lymphomtransplantaten verlangsamte Prochlorperazin in klinisch erreichbaren Dosen das Tumorwachstum signifikant. Zudem erzeugte die Kombination von Phenothiazinen mit Wirkstoffen, die andere BCR‑verknüpfte Enzyme wie SYK und PI3Kδ blockieren, stärkere krebszerstörende Effekte als jede Einzeltherapie.
Was das für die Behandlung bedeuten könnte
Insgesamt zeigt die Studie, dass bei einer beträchtlichen Untergruppe von DLBCLs die krebsfördernden Signale nicht einfach nur von Rezeptoren an der Zelloberfläche ausgehen; sie hängen entscheidend davon ab, dass das BCR–Antigen‑Komplex über einen spezifischen Endozytoseweg ins Zellinnere gezogen wird. Das Unterbrechen dieses Schrittes — sei es durch genetische Eingriffe oder durch Phenothiazine — schwächt die NFκB‑Signalgebung und beeinträchtigt das Überleben der Tumorzellen, während es möglicherweise die Empfindlichkeit gegenüber bestehenden Inhibitoren des BCR‑Signalwegs erhöht. Da Phenothiazine bereits als Anti‑Übelkeitsmittel hinsichtlich Dosierung und Sicherheit gut charakterisiert sind, liefert diese Arbeit einen realistischen Fahrplan für klinische Studien, die deren Einsatz, allein oder in Kombination, bei Patientinnen und Patienten testen, deren Lymphome autoantigenabhängige BCR‑Aktivität zeigen.
Zitation: Górniak, P., Polak, A., Rams, A. et al. Inhibition of autoantigen-induced B-cell receptor (BCR) internalization as a therapeutic strategy in diffuse large B cell lymphoma (DLBCL). Cell Death Dis 17, 216 (2026). https://doi.org/10.1038/s41419-026-08446-1
Schlüsselwörter: diffuses großzelliges B‑Zell‑Lymphom, B‑Zell‑Rezeptor, Endozytose, Phenothiazine, NFkB‑Signalgebung