Clear Sky Science · de
Zeitaufgelöste Multi-Omik-Analyse der Paclitaxel-Exposition in aus menschlichen iPS-Zellen abgeleiteten sensorischen Neuronen deckt Mechanismen der chemotherapieinduzierten peripheren Neuropathie auf
Warum manche Krebsmedikamente Nerven schädigen
Chemotherapie hat Millionen von Menschen das Überleben von Krebs ermöglicht, doch viele Patientinnen und Patienten zahlen einen versteckten Preis: monatelange oder jahrelange brennende Schmerzen, Kribbeln und Taubheitsgefühle in Händen und Füßen. Diese Studie stellt eine einfache, aber wichtige Frage: Was genau bewirkt das weit verbreitete Krebsmedikament Paclitaxel in menschlichen sensorischen Nervenzellen, und kann das Verständnis dieser Veränderungen Wege zu besserer Prävention und Behandlung dieser Nervenschädigung weisen?
Von Patientenproben zu im Labor gezüchteten schmerzleitenden Nerven
Anstatt sich auf Tierexperimente zu stützen, begannen die Forschenden mit Zellen aus fünf menschlichen Spendern, darunter Brustkrebspatientinnen, die Paclitaxel erhalten hatten. Sie reprogrammierten diese Zellen zu induzierten pluripotenten Stammzellen und leiteten sie dann zur Differenzierung in sensorische Neuronen an — genau den Zelltyp, der Berührungs- und Schmerzsignale von der Haut zum Rückenmark überträgt. Diese im Labor gezüchteten Neuronen bildeten lange, feine Fasern und zeigten elektrische Aktivität, die echten schmerzleitenden Nerven im Körper sehr ähnelte. Das Team setzte sie dann steigenden Paclitaxel-Dosen aus, die den im Patienten beobachteten Konzentrationen nachempfunden waren, und verfolgte den Zellzustand über mehrere Tage. Bei niedrigen Konzentrationen kamen die Neuronen gut zurecht, doch bei einer klinisch relevanten Dosis (100 nM) begann ihre Überlebensrate nach etwa zwei Tagen zu sinken, ein Zeichen für beginnende toxische Nervenschädigung.
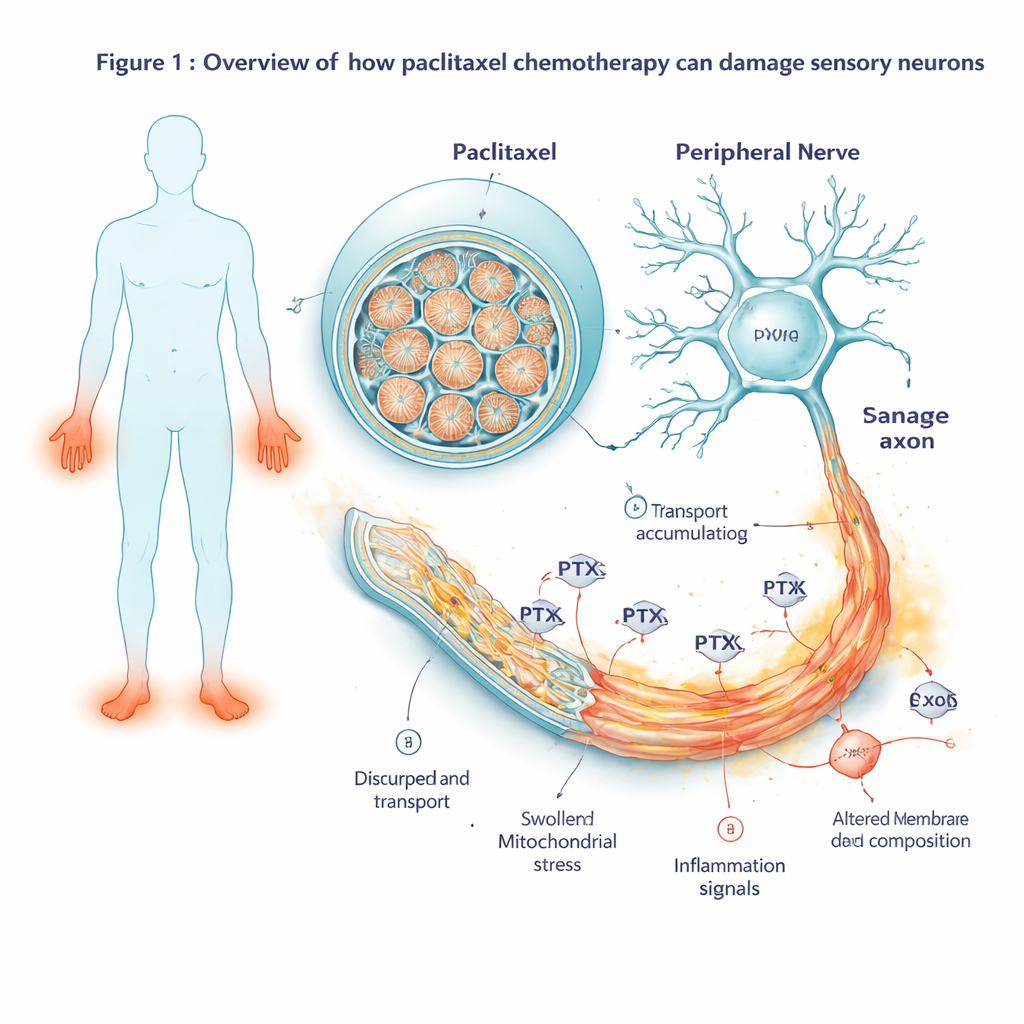
Beobachtung zeitlicher Veränderungen der Genaktivität
Um zu sehen, wie die Zellen reagierten, bevor sie sichtbar degenerierten, maßen die Wissenschaftler, welche Gene zu verschiedenen Zeitpunkten an- oder ausgeschaltet wurden – von zwei Stunden nach der Exposition bis mehrere Tage, nachdem das Medikament ausgespült worden war. Früh zeigte sich die Aktivierung eines klassischen zellulären Stressprogramms, zentriert um das Gen JUN. Mit anhaltender Exposition weitete sich dieses Stresssignal zu einer vollständigen Selbstzerstörungs-Kaskade aus: Gene, die Zellen in Richtung programmierter Zelltod treiben, wurden stark hochreguliert, während schützende Partner überrollt wurden. Gleichzeitig wurden Gene, die mit Entzündung und Schmerzsignalgebung verbunden sind, aktiver. Die Neuronen begannen, mehr entzündliche Botenstoffe, schmerzbezogene Peptide und Rezeptoren zu produzieren, die Zellen empfindlicher für schädliche Reize machen — Veränderungen, die denen in schmerzhaften Nervenerkrankungen entsprechen.
Tiefer Blick auf Proteine und Lipide in Neuronen
Da Gene nur Baupläne sind, untersuchte das Team auch die tatsächlich in den Neuronen vorhandenen Proteine sowie deren Lipidzusammensetzung. Nach 48 Stunden Paclitaxel-Exposition traten viele der auf RNA-Ebene detektierten Stress- und Entzündungssignale auch als erhöhte Proteinmengen auf, was bestätigte, dass die Neuronen diese schädlichen Programme ausführten. Auffällig war ein starker Rückgang von Proteinen, die für den axonalen Transport notwendig sind — die molekularen Motoren und Gerüstproteine, die Fracht entlang der langen Nervenfasern bewegen. Dazu gehörten Kinesine und regulatorische Proteine, die Mikrotubulus-Spuren stabil halten. Auf Lipidebene zeigten die Neuronen einen Rückgang wichtiger Bausteine für Cholesterin- und Membranlipide, parallel zu einem Anstieg gespeicherter Fette, sogenannter Triacylglycerole. Zusammengenommen deuten diese Verschiebungen darauf hin, dass Paclitaxel nicht nur Zelltodwege auslöst, sondern auch die physische Struktur und das Energiegleichgewicht der Nervenfasern schwächt.
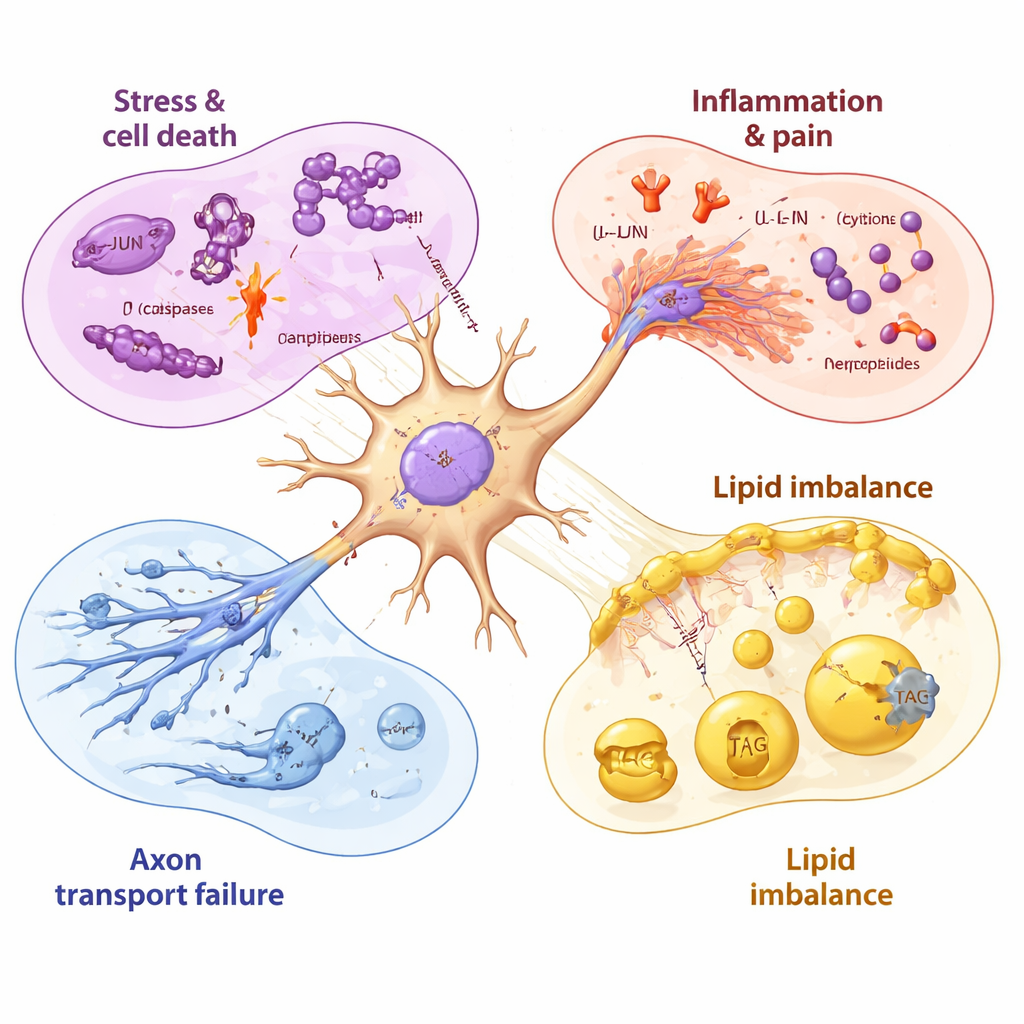
Eine Zeitachse der Nervenschädigung und unvollständigen Erholung
Indem die Forschenden die Neuronen vor, während und nach der Medikamentenexposition beprobten, konnten sie diese Ereignisse zeitlich ordnen. Mitochondriale (energiebezogene) Gene wurden innerhalb weniger Stunden gestört, gefolgt vom Stressgen JUN, dann von stärkerer Aktivierung von Zelltod- und Entzündungsprogrammen, als die Lebensfähigkeit zu fallen begann. Selbst nachdem Paclitaxel entfernt worden war, blieben viele schädliche Signale noch Tage lang erhöht, während die Gene, die für die Herstellung gesunder Membranlipide nötig sind, weiter zurückgingen. Einige spät ansteigende Moleküle, etwa eine Wirkstoffauspumppumpe, die Paclitaxel expulsieren kann, und bestimmte Wachstumsfaktoren, deuteten darauf hin, dass Neuronen Schutz- und Reparaturversuche unternahmen — diese Reaktionen erschienen jedoch im Vergleich zu der schnellen, frühen Entwicklung hin zur Schädigung relativ langsam und unvollständig.
Was das für Patientinnen und Patienten mit Nervenschmerzen bedeutet
Für Nicht-Fachleute lautet die Botschaft: Paclitaxel schädigt sensorische Nerven durch eine koordinierte Abfolge von Treffern: Es belastet ihre Energiesysteme, schaltet genetische Programme in Richtung Zelltod um, fördert Entzündung und Schmerzsignalgebung, stört die inneren "Transportautobahnen" in Nervenzellen und verändert die Lipide, die Nervenzellmembranen stabilisieren. Durch die detaillierte Kartierung dieser Veränderungen in menschlich abgeleiteten Neuronen hebt die Studie konkrete, medikamentös angreifbare Ziele hervor — etwa bestimmte Stressregulatoren, entzündliche Rezeptoren und Lipid-bildende Enzyme —, die blockiert oder unterstützt werden könnten, um Nerven zu schützen, ohne die Krebstherapie zu schwächen. Zwar bedürfen neue Therapien weiterer Prüfungen, doch liefert diese Arbeit eine klarere Roadmap zur Vorbeugung oder Linderung chemotherapieinduzierter Nervenschäden und zur Verbesserung der Lebensqualität von Krebsüberlebenden.
Zitation: Schinke, C., Maierhof, S.K., Hew, L. et al. Time‑resolved multi-omic analysis of paclitaxel exposure in human iPSC‑derived sensory neurons unveils mechanisms of chemotherapy‑induced peripheral neuropathy. Cell Death Dis 17, 211 (2026). https://doi.org/10.1038/s41419-026-08445-2
Schlüsselwörter: chemotherapieinduzierte periphere Neuropathie, Paclitaxel, sensorische Neuronen, Neuroinflammation, Axondegeneration