Clear Sky Science · de
Reversible Arginin-Methylierung reguliert die mitochondriale IDH2-Aktivität: koordinierte Kontrolle durch CARM1 und KDM3A/4A
Feinabstimmung der Kraftwerke der Zelle
Mitochondrien, oft als die Kraftwerke unserer Zellen bezeichnet, leisten weit mehr als nur Energieproduktion. Sie passen laufend an, wie sie Brennstoff verbrennen, um den Bedarf des Körpers zu decken, und wenn diese Anpassung gestört ist, kann das zu Erkrankungen wie Diabetes, Herzversagen und Krebs beitragen. Diese Studie deckt einen verborgenen „Dimm-Schalter“ in den Mitochondrien auf: ein winziges chemisches Kennzeichen an einer einzigen Aminosäure eines Schlüsselenzyms, IDH2, das mitentscheidet, ob die Mitochondrien im Leerlauf bleiben oder ihre Energieproduktion hochfahren.
Ein winziges Zeichen mit großer Wirkung
Proteine in unseren Zellen sind nicht statisch; sie werden häufig mit kleinen chemischen Gruppen modifiziert, die ihr Verhalten verändern. Während viele solche Modifikationen im Zellkern und im Zellplasma gut untersucht sind, sind Modifikationen innerhalb der Mitochondrien weniger erforscht. Die Autorinnen und Autoren konzentrierten sich auf eine bestimmte Art von Markierung, die Argininmethylierung, und fragten, ob sie die Funktion mitochondrialer Enzyme steuern könnte. Sie richteten ihren Fokus auf das Enzym IDH2, einen Arbeitspferd-Enzym des Tricarbonsäure-(TCA-)Zyklus, das hilft, Nährstoffe in Energie und wichtige metabolische Bausteine umzuwandeln. Mit biochemischen Methoden und Massenspektrometrie fanden sie, dass IDH2 eine spezifische Methylmarkierung an einer Aminosäure trägt, Arginin 188, und dass diese Markierung von einem Enzym namens CARM1 gesetzt wird, das überraschenderweise auch in den Mitochondrien wirkt.
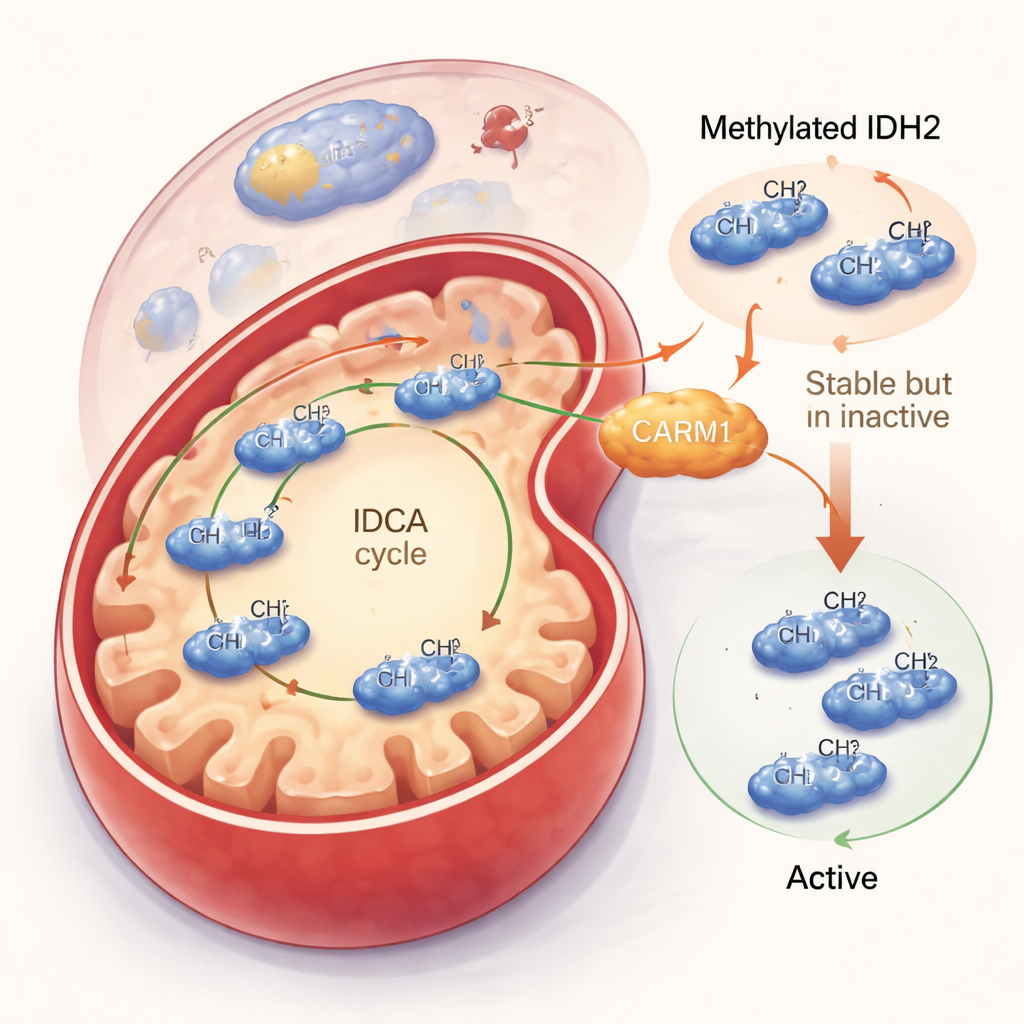
IDH2 abschwächen, aber länger erhalten
Die Gruppe untersuchte dann, welche Wirkung diese Methylmarkierung tatsächlich hat. Wenn CARM1 aktiv war und IDH2 methylierte, wurde das IDH2-Protein stabiler und blieb länger in der Zelle erhalten. Dieser scheinbare Vorteil ging jedoch mit einem Kompromiss einher: methylierte IDH2 war weniger aktiv. In Zellversuchen und Tests mit gereinigtem Protein erzeugte methylierte IDH2 weniger seines Hauptprodukts, Alpha-Ketoglutarat, und produzierte weniger des schützenden Moleküls NADPH. Im Gegensatz dazu bildete eine Variante von IDH2, die an Arginin 188 nicht methylierbar war, häufiger die aktive Dimerform, arbeitete schneller und steigerte sowohl Alpha-Ketoglutarat- als auch NADPH-Spiegel. Obwohl von dieser demethylierbaren IDH2-Variante insgesamt weniger vorhanden war, leistete jedes Molekül mehr Arbeit, was zu einer Nettoerhöhung der mitochondrialen Leistung führte.
Ein reversibler Schalter mit zwei Radierern
Wesentlich ist, dass diese Methylmarkierung nicht dauerhaft ist. Die Forschenden zeigten, dass zwei Enzyme, die normalerweise für das Entfernen einer anderen Art von Markierung bekannt sind — die Lysin-Demethylasen KDM3A und KDM4A — auch die Argininmethylierung von IDH2 entfernen können. Wenn diese Demethylasen vorhanden waren, verlor das methylierte Arginin an Position 188 seine zusätzlichen chemischen Gruppen, IDH2 wurde weniger stabil, aber aktiver, und seine Dimerform nahm zu. Zellen mit verstärkter KDM3A- oder KDM4A-Aktivität zeigten eine höhere mitochondriale Membranpotenzial und einen höheren Sauerstoffverbrauch, Hinweise darauf, dass ihre Mitochondrien stärker oxidativ arbeiteten. Bei Reduktion dieser Enzyme trat das Gegenteil ein: die IDH2-Aktivität sank und die mitochondriale Leistung ging zurück, was unterstreicht, dass es sich um ein reversibles Regulationssystem und nicht um eine Einbahnveränderung handelt.
Verbindung von Stoffwechsel und Krankheit
Da IDH2 mit Krebs und anderen Erkrankungen in Verbindung gebracht wurde, untersuchten die Autorinnen und Autoren, wie dieser Methylierungs-Schalter in krankheitsähnlichen Kontexten relevant sein könnte. In verschiedenen normalen und Krebszelllinien beobachteten sie, dass höhere IDH2-Proteinmengen oft mit stärkerer Methylierung und überraschenderweise geringerer Enzymaktivität einhergingen, was nahelegt, dass „mehr Protein“ nicht immer „mehr Funktion“ bedeutet. In Brustkrebsmaterialien hatte Patienten mit höheren IDH2-Proteinspiegeln tendenziell schlechteres Überleben, obwohl die IDH2-Genaktivität nicht mit dem Outcome korrespondierte. Die Ergebnisse stützen ein Modell, in dem CARM1-getriebene Methylierung den TCA-Zyklus verlangsamt und Zellen zu alternativen, krebsfördernden Wegen der Nährstoffnutzung lenkt, während Demethylasen wie KDM3A und KDM4A Zellen zurück zu effizienterer Energieproduktion treiben können.
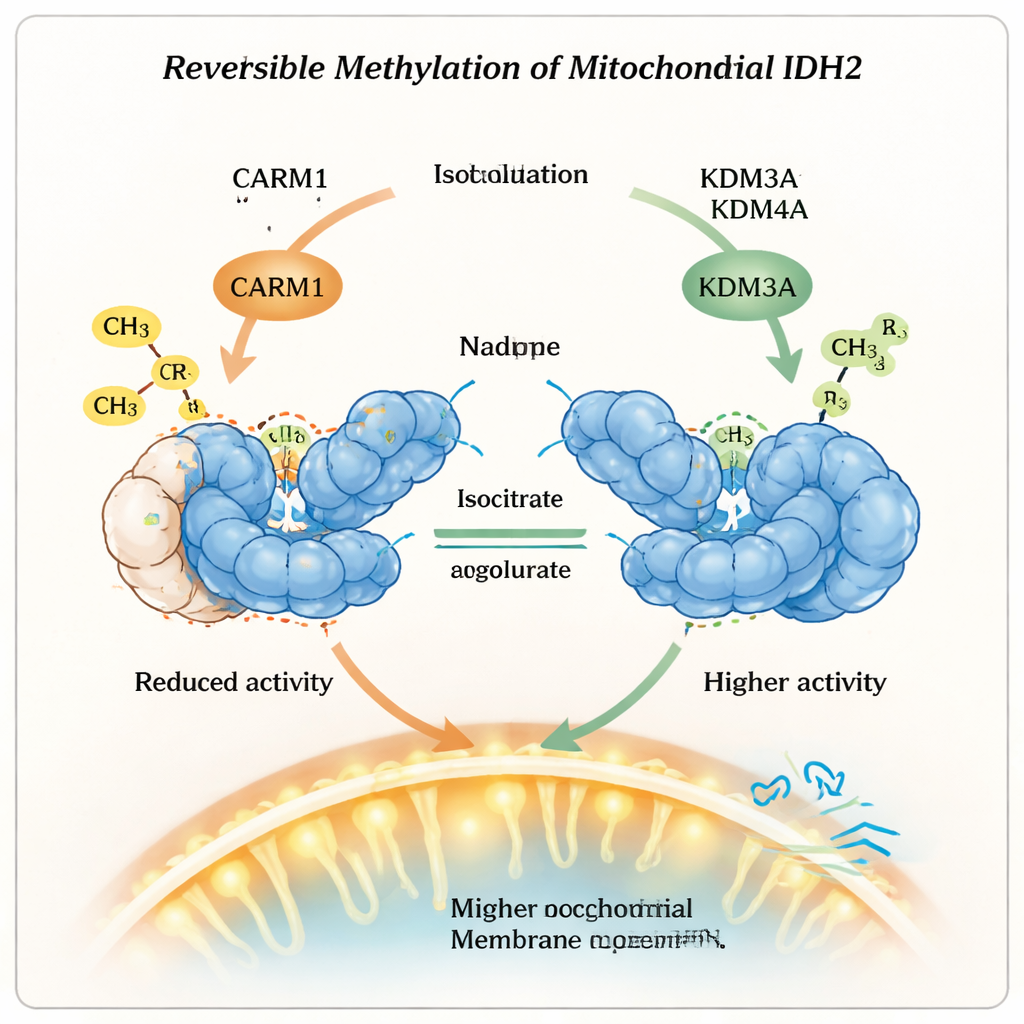
Was das für Gesundheit und Therapie bedeutet
Anschaulich zeigt diese Arbeit, dass Mitochondrien Enzyme nicht einfach nur an- oder ausschalten, sondern reversible chemische Markierungen als fein einstellbare Regler verwenden. Durch das Anfügen einer Methylgruppe verwandelt CARM1 IDH2 in eine langlebigere, aber weniger aktive Form; durch Entfernen dieses Zeichens opfern KDM3A und KDM4A etwas Stabilität, gewinnen aber mehr Leistungsfähigkeit. Dieses Gleichgewicht beeinflusst, wie Zellen zwischen schnellem, aber ineffizientem Zuckerstoffwechsel und langsamerer, effizienterer Energiegewinnung wählen. Das Verständnis dieses Methylierungs-„Dimm-Schalters“ auf IDH2 eröffnet neue Möglichkeiten für Therapien, die darauf abzielen, fehlerhaften mitochondrialen Stoffwechsel bei Erkrankungen wie Krebs und Stoffwechselkrankheiten zu korrigieren, indem die Enzyme adressiert werden, die diese winzigen, aber mächtigen chemischen Markierungen setzen und entfernen.
Zitation: Cho, Y., Winarto, J., Song, DG. et al. Reversible arginine methylation regulates mitochondrial IDH2 activity: coordinated control by CARM1 and KDM3A/4A. Cell Death Dis 17, 195 (2026). https://doi.org/10.1038/s41419-026-08444-3
Schlüsselwörter: Mitochondrien, IDH2, Argininmethylierung, Zellstoffwechsel, CARM1