Clear Sky Science · de
Eine MIF-p38-GSDMD-Entzündungsschleife in Keratinozyten liegt UVB‑induziertem kutanem Lupus zugrunde
Warum Sonnenlicht bei Lupus ein ernstes Problem sein kann
Für die meisten Menschen führt Sonnenlicht höchstens zu einer Bräune oder im schlimmsten Fall zu einem Sonnenbrand. Für viele Lupuspatienten kann jedoch schon wenige Minuten UVB‑Licht schmerzhafte, langanhaltende Hautausschläge auslösen und sogar die gesamte Erkrankung verschlechtern. Diese Studie deckt eine verborgene „Rückkopplungsschleife“ in Hautzellen auf, die erklärt, warum ihre Haut so lichtempfindlich ist — und weist auf neue, sehr lokale Behandlungsansätze hin, die die Reaktion dämpfen könnten, ohne das ganze Immunsystem zu unterdrücken.
Hautzellen als unerwartete Störenfriede
Ärzte wissen seit langem, dass kutaner Lupus erythematodes (CLE) mit chronischer Entzündung und Vernarbung der Haut einhergeht, doch der Fokus lag oft auf eindringenden Immunzellen. Mithilfe von Einzelzell‑RNA‑Sequenzierung richteten die Autorinnen und Autoren ihren Blick stattdessen auf die eigenen Bausteine der Haut — die Keratinozyten in der äußeren Schicht und die darunterliegenden Fibroblasten. Sie fanden, dass bei Lupuspatienten bestimmte Untergruppen von Keratinozyten vermehrt vorkommen und ein starkes „Interferon‑Signatur“‑Muster zeigen, also antivirale Alarmgene dauerhaft aktiviert sind. Innerhalb dieser abnormalen Keratinozyten stach ein Botenprotein hervor: der Macrophage Migration Inhibitory Factor, kurz MIF, das in deutlich höheren Mengen produziert wurde als bekanntere Entzündungsmediatoren wie TNF oder IL‑6.
Ein verborgener Bote, der durch Sonnenlicht freigesetzt wird
Allein hoher MIF‑Gehalt in Keratinozyten erklärte noch nicht, warum Sonnenlicht so gefährlich ist. Als das Team kultivierte Keratinozyten UVB‑Licht aussetzte, zeigte sich, dass die Gesamtmenge an MIF in den Zellen kaum verändert wurde — das Protein jedoch dosisabhängig in die umgebende Flüssigkeit freigesetzt wurde. Je mehr UVB, desto mehr MIF trat aus und korrelierte eng mit einem Marker für Membranschädigung. Wurde diese MIF‑reiche Flüssigkeit auf frische Keratinozyten und Fibroblasten gegeben, löste sie typische CLE‑ähnliche Veränderungen aus: erhöhte Mengen entzündlicher Zytokine und von Enzymen, die die stützende Matrix der Haut abbauen und umbauen. Das Stilllegen von MIF mit genetischen Methoden oder dessen Blockade durch ein niedermolekulares Medikament reduzierte diese schädlichen Reaktionen deutlich, was zeigt, dass von Keratinozyten stammendes MIF kein bloßer Zuschauer, sondern ein wesentlicher Verstärker der UVB‑vermittelten Schäden ist. 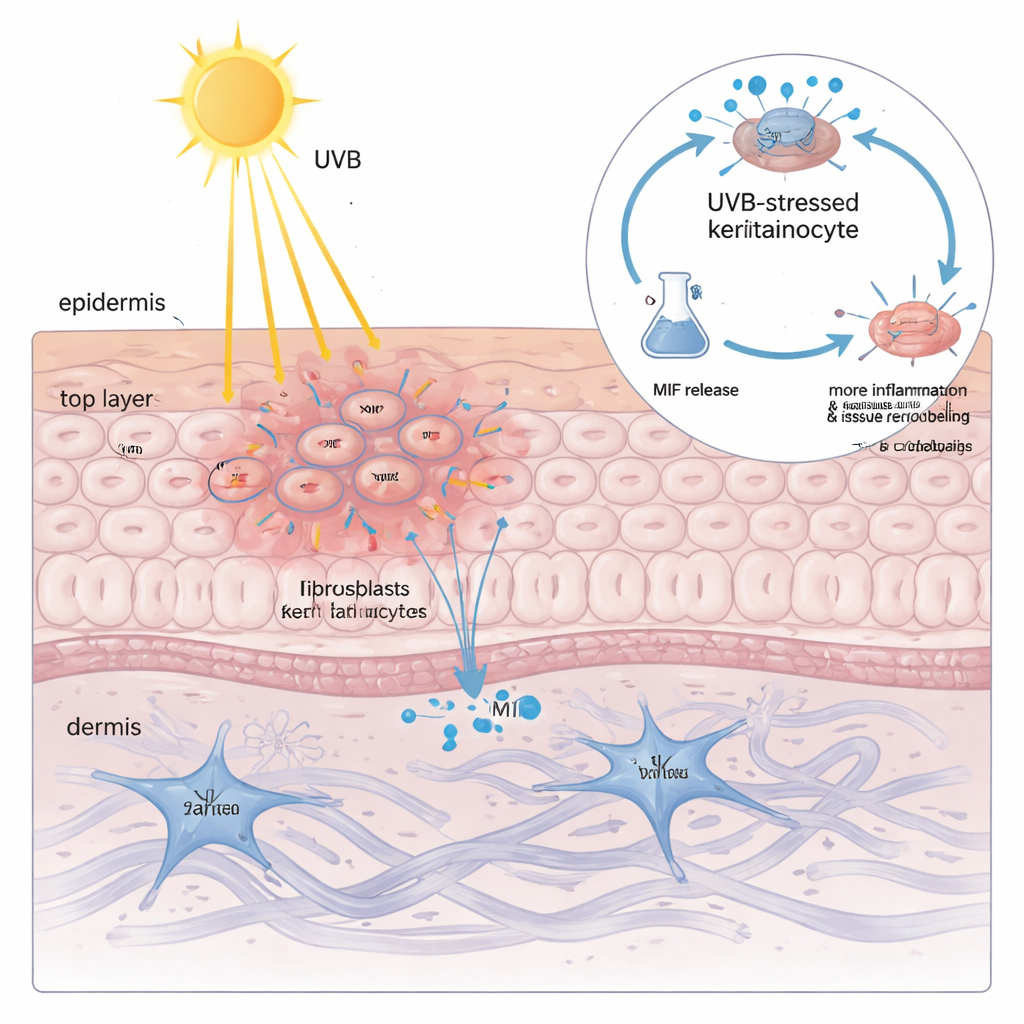
Eine sich selbst erhaltende Entzündungsschleife in Keratinozyten
Um zu verstehen, wie UVB Keratinozyten zur Freisetzung von MIF zwingt, bauten die Forschenden ein „lupusähnliches“ Keratinozytenmodell, indem sie Zellen mit eigenem DNA‑ und RNA‑Material beluden — eine Nachahmung des fehlgesteuerten genetischen Abfalls, der bei Lupus vorkommt. In diesem voraktivierten Zustand löste UVB eine sogenannte ribotoxische Stressantwort aus: ein Schadenssignal von Ribosomen, das die Kinasen ZAKα und daraufhin die Stresskinase p38 aktivierte. Dieser Weg erhöhte einen weiteren Faktor, den Transkriptionsfaktor C/EBPβ, der an die Kontrollregion des NLRP3‑Gens bindet und dessen Expression hochfährt. NLRP3 trieb dann die Spaltung von GSDMD voran, einem porenbildenden Protein, das Löcher in die Zellmembran bohrt und eine entzündliche Form des Zelltods, die Pyroptose, verursacht. Entscheidend entwich MIF hauptsächlich durch diese GSDMD‑Poren — nicht über normale sekretorische Vesikel. Einmal außerhalb, bindet MIF an seinen Rezeptor CD74 auf Keratinozyten und reaktiviert p38, NLRP3 und GSDMD, womit sich ein Teufelskreis schließt: UVB → p38 → NLRP3 → GSDMD‑Poren → MIF‑Freisetzung → verstärkte p38‑Aktivierung.
Vom molekularen Befund zu neuen lokalen Therapien
Diese Schleife war keine bloße Laborneugier. In einer lupusanfälligen Mauslinie führte UVB‑Exposition zu schweren Hautläsionen mit hohen MIF‑Spiegeln, p38‑Aktivierung, NLRP3‑Expression und gespaltenem GSDMD im Epidermis. Als die Forschenden ein gentherapeutisches Virus einsetzten, um das Mif‑Gen gezielt in der Haut stummzuschalten, wurden die UVB‑induzierten Ausschläge deutlich milder, und Entzündungs‑ sowie Geweberemodellierungsmarker sanken in Keratinozyten und Fibroblasten. Um systemische Nebenwirkungen zu vermeiden, entwickelten sie außerdem auflösbare Mikronadelpflaster, die den MIF‑Inhibitor ISO‑1 enthielten. Kurz in die Haut gedrückt, lieferten diese winzigen Nadeln das Medikament schmerzfrei in die oberen Hautschichten. Behandelte lupusanfällige Mäuse entwickelten nach UVB deutlich weniger und weniger schwere Läsionen, und die molekulare Signatur der MIF‑p38‑GSDMD‑Schleife war deutlich abgeschwächt. 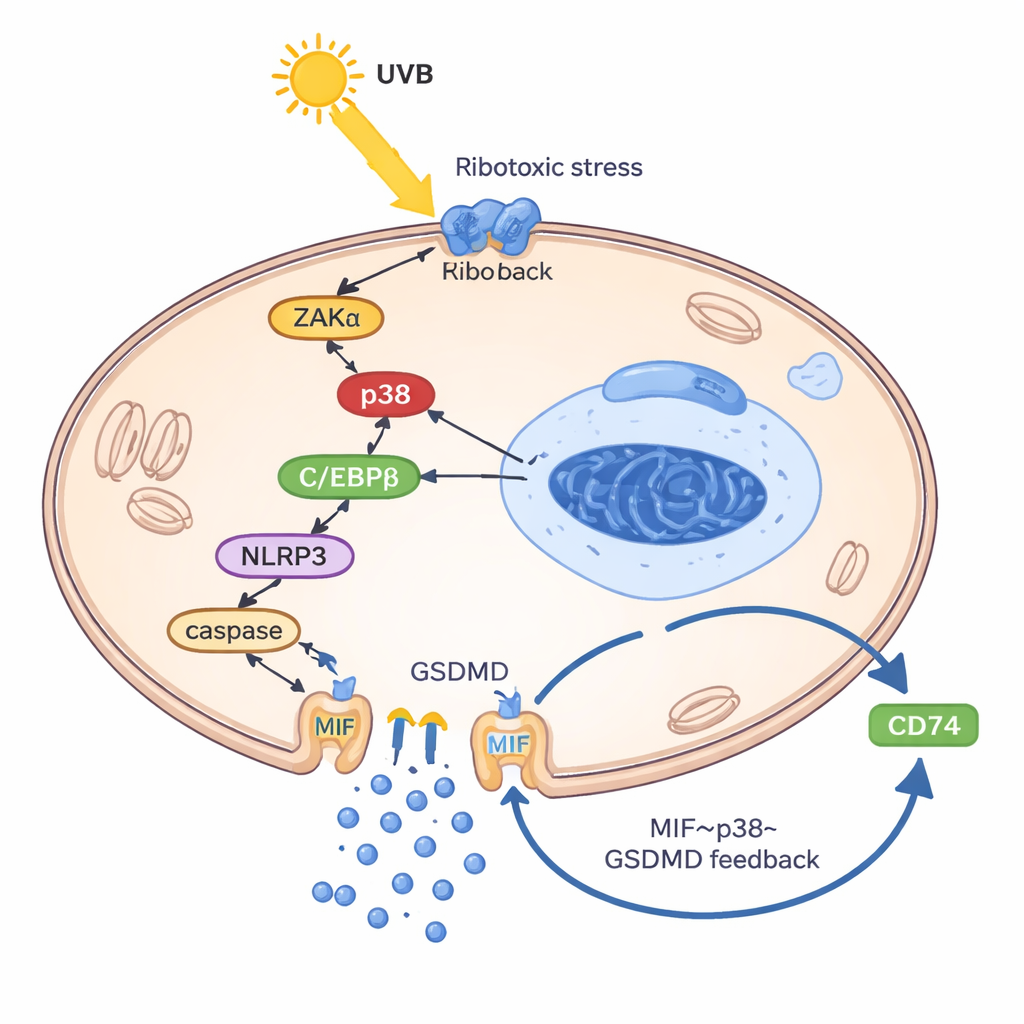
Was das für Menschen mit Lupus bedeutet
Einfache Worte: Die Arbeit zeigt, dass bei Lupus bestimmte Hautzellen so verdrahtet sind, dass sie auf UVB‑Licht überreagieren, indem sie ein kraftvolles „Verstärkermolekül“, MIF, durch selbstverursachte Membranporen freisetzen. Dieser Verstärker hält dann die entzündlichen Mechanismen am Laufen, selbst nachdem die ursprüngliche Lichtexposition vorbei ist. Durch das schrittweise Kartieren dieser Schleife legt die Studie nahe, dass eine lokale Blockade von MIF — etwa durch Genstilllegung oder intelligente Abgabesysteme wie Mikronadelpflaster — den Kreislauf fotosensitiver Schübe unterbrechen könnte, ohne das Immunsystem insgesamt zu dämpfen. Wenn ähnliche Strategien beim Menschen sicher und wirksam sind, könnten sie Menschen mit Lupus neue Möglichkeiten bieten, sich im Licht wohler zu fühlen.
Zitation: Guo, C., Luo, S., Luo, J. et al. A MIF-p38-GSDMD inflammatory loop in keratinocytes underlies UVB-induced cutaneous lupus. Cell Death Dis 17, 198 (2026). https://doi.org/10.1038/s41419-026-08443-4
Schlüsselwörter: kutaner Lupus, Photosensitivität, Keratinozyten, entzündliche Schleife, Mikronadeltherapie