Clear Sky Science · de
SOX21 unterdrückt das Wachstum von Glioblastomen durch Repression der AP-1-Aktivität
Warum diese Studie zu Hirnkrebs wichtig ist
Das Glioblastom gehört zu den tödlichsten Hirntumoren, vor allem weil eine kleine Population hartnäckiger „Starter“-Zellen das Tumorwachstum antreiben und das Wiederauftreten nach einer Behandlung verursachen kann. Diese Studie zeigt, wie ein natürlich vorkommendes Protein in Gehirnzellen, SOX21 genannt, diese gefährlichen Zellen ausschalten kann, indem es ein wachstumsförderndes Programm im Inneren ihrer DNA abschaltet. Das Verständnis dieses internen Aus-Schalters könnte neue Strategien inspirieren, um Glioblastome zu verlangsamen und die Wirksamkeit bestehender Therapien zu verbessern.
Die verborgenen Treiber in Hirntumoren
Innerhalb eines Glioblastoms sind nicht alle Zellen gleich. Eine Minderheit, bekannt als glioblastomvorläuferzellen (GPCs), verhält sich wie Stammzellen: Sie erneuern sich selbst, widerstehen Therapien und können den Tumor nach Operation, Strahlentherapie oder Chemotherapie wieder neu besiedeln. Diese Zellen werden von Netzwerken aus Transkriptionsfaktoren gesteuert, Proteinen, die entscheiden, welche Gene aktiv oder stillgelegt sind. Einige bekannte Faktoren, wie SOX2 und Mitglieder der AP‑1-Familie, fördern typischerweise Wachstum und Überleben. Im Gegensatz dazu wurde SOX21 mit verringerter Zellteilung und erhöhter Reifung normaler neuraler Stammzellen in Verbindung gebracht, und frühere Arbeiten deuteten darauf hin, dass es vor Hirntumoren schützen könnte. Unklar war jedoch, ob eine Erhöhung der SOX21-Spiegel in einem bereits etablierten Tumor dessen Wachstum tatsächlich verlangsamen könnte und wie SOX21 genau in Krebszellen wirkt.
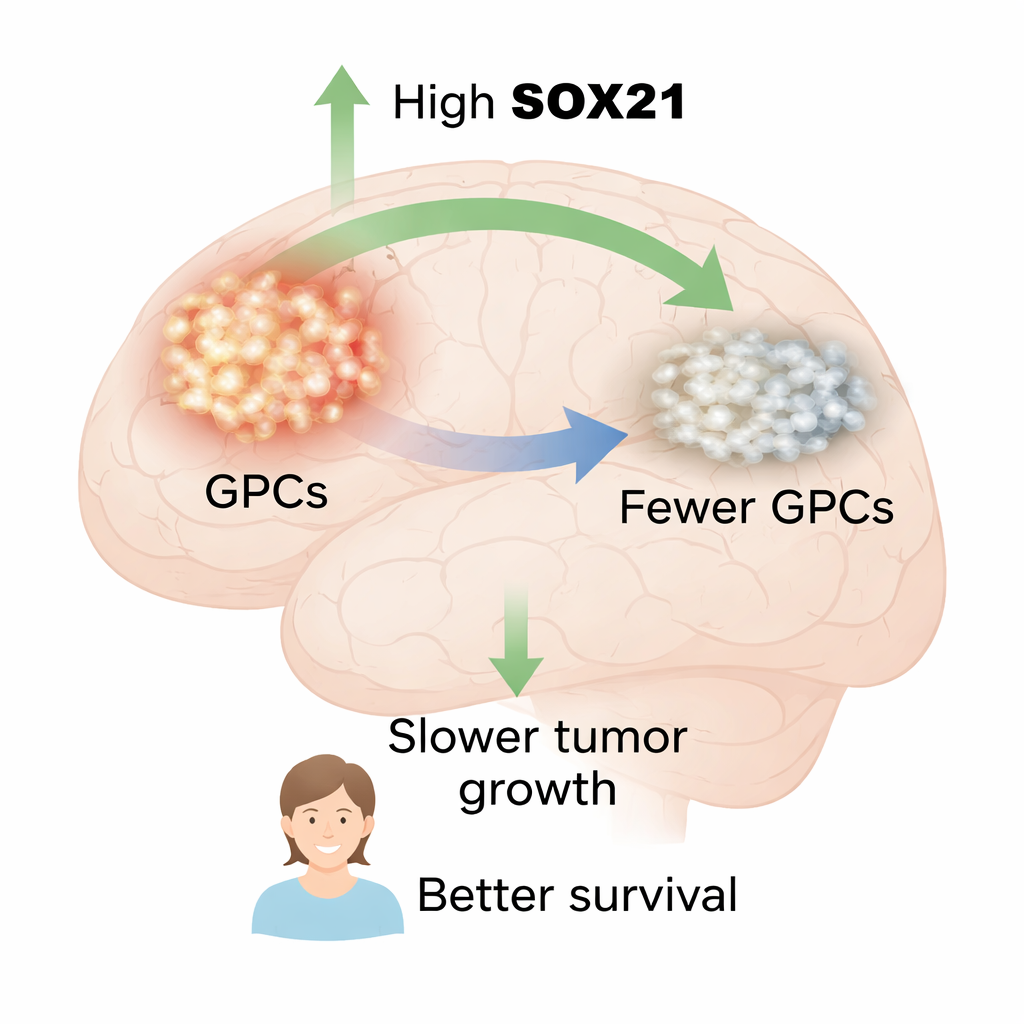
SOX21 steht für eine bessere Prognose und schwächt Tumorzellen
Die Forschenden begannen mit der Analyse menschlicher Glioblastomproben. Sie fanden heraus, dass SOX21-Protein hauptsächlich in Zellen vorkam, die auch Stammzellmarker wie SOX2 und OLIG2 trugen, sowie in sich aktiv teilenden Zellen, identifiziert durch den Marker KI67. Dies zeigte, dass SOX21 genau im GPC‑Kompartiment des Tumors lokalisiert ist. In großen öffentlichen Patientendatensätzen verglichen sie anschließend das Überleben von Personen mit hoher versus niedriger SOX21-Genaktivität. In zwei unabhängigen Kohorten lebten Patientinnen und Patienten mit höherer SOX21-Expression signifikant länger, was SOX21 mit einem günstigeren Krankheitsverlauf verbindet.
SOX21 einzuschalten verlangsamt das Wachstum und verringert Tumorbildungsfähigkeit
Um Ursache und Wirkung zu prüfen, bauten die Forschenden GPCs aus Patientenproben so um, dass sie ein per Doxycyclin schaltbares SOX21-Gen trugen. Nach Induktion von SOX21 in Zellkulturen teilten sich diese Zellen weniger, nahmen weniger DNA-Bausteine auf (ein Zeichen verlangsamter Proliferation) und zeigten mehr Merkmale programmierter Zelltodes. Ihre Fähigkeit, frei schwebende Sphären zu bilden — ein Maß für selbst erneuernde, stammzellähnliche Eigenschaften — sank deutlich, und sie wurden empfindlicher gegenüber dem Standardmedikament Temozolomid. In MausrExperimenten durften humane GPCs zunächst Hirntumoren bilden, bevor SOX21 eingeschaltet wurde. Unter diesen Bedingungen verlangsamte SOX21 — nicht aber SOX2 — das Tumorwachstum, verringerte den Anteil sich teilender und stammzellähnlicher Zellen im Tumor und verlängerte das Überleben der Tiere deutlich. Das zeigt, dass eine Erhöhung von SOX21 auf bestehende Tumoren wirken kann und nicht nur deren Entstehung verhindert.
Wie SOX21 ein krebsförderndes Programm entwaffnet
Auf molekularer Ebene kartierten die Autorinnen und Autoren, welche Gene sich veränderten, wenn SOX21 eingeschaltet wurde, und an welchen Stellen der DNA SOX21 physisch gebunden war. SOX21 erhöhte die Expression von Genen, die an Zellzyklusarrest und Zelltod beteiligt sind, einschließlich des Tumorsuppressors p21, und senkte Gene, die zuvor mit Gliomprogression in Verbindung gebracht wurden, wie CDK6, EFNB2, HDAC9 und sogar SOX2 selbst. Auffällig war, dass SOX21 stark an DNA‑Regionen gebunden war, die auch von c‑JUN besetzt sind — einem Schlüsselmitglied der AP‑1-Familie, das normalerweise wachstumsfördernde Gene aktiviert. Diese gemeinsamen Regionen enthielten klassische AP‑1‑Sequenzmotive und chemische Kennzeichen aktiver Enhancer — DNA‑Abschnitte, die die Genexpression verstärken. Bei erhöhtem SOX21 wurden diese Enhancer weniger zugänglich und verloren Aktivierungsmarken, und die assoziierten Gene wurden herunterreguliert. Wirkstoffe, die AP‑1 blockieren, reproduzierten viele der gleichen Genänderungen und biologischen Effekte wie SOX21, während eine erzwungene Überproduktion von c‑JUN die Zellen vor der unterdrückenden Wirkung von SOX21 bewahren konnte.
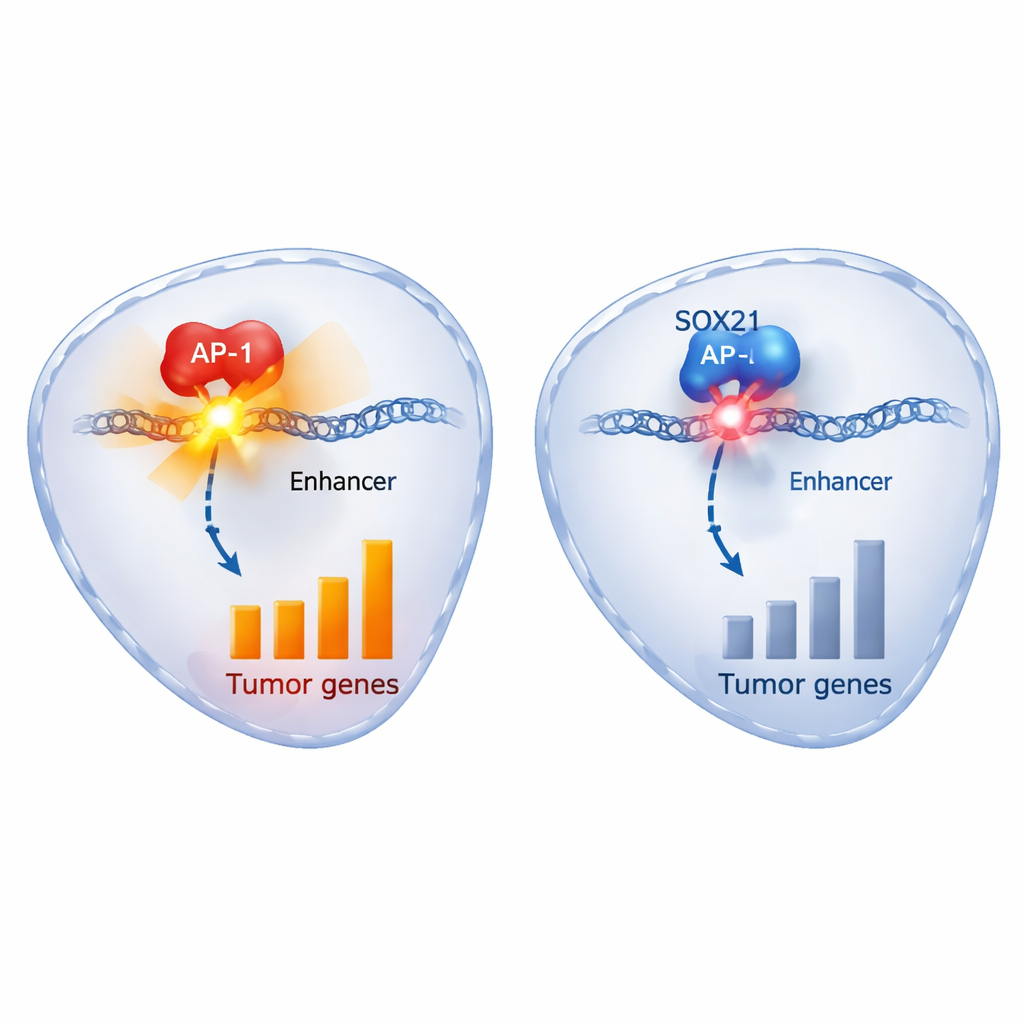
Was das für die künftige Glioblastom-Behandlung bedeutet
Kurz gesagt wirkt SOX21 als Bremse in den gefährlichsten Zellen des Glioblastoms, indem es an dieselben DNA‑Schalter bindet, die AP‑1 zur Förderung des Tumorwachstums nutzt, und diese Schalter dann dämpft. Patientinnen und Patienten, deren Tumoren von Natur aus mehr SOX21 produzieren, haben tendenziell eine bessere Prognose, und in Tiermodellen verlangsamt das Einschalten von SOX21 in etablierten Tumoren deren Wachstum und verbessert die Reaktion auf Chemotherapie. Obwohl die direkte Verabreichung oder Aktivierung von SOX21 beim Menschen noch nicht praktikabel ist, bieten die von SOX21 kontrollierten Signalwege — und sein Tauziehen mit AP‑1 — vielversprechende Ansatzpunkte für neue Wirkstoffe, die den stammzellähnlichen Kern des Tumors schwächen und das Rückfallrisiko verringern könnten.
Zitation: Rrapaj, E., Yuan, J., Kurtsdotter, I. et al. SOX21 suppresses glioblastoma growth by repressing AP-1 activity. Cell Death Dis 17, 191 (2026). https://doi.org/10.1038/s41419-026-08442-5
Schlüsselwörter: Glioblastom, Krebsstammzellen, SOX21, AP-1, Therapie von Hirntumoren