Clear Sky Science · de
Honokiol blockiert Tumorentwicklung und Metastasenbildung durch mitochondriengerichtete Effekte
Aus einer Baumverbindung wird ein Krebsbekämpfer
Viele Krebsmedikamente stammen aus Pflanzen, und Forschende entdecken weiterhin, wie einige dieser natürlichen Moleküle in unseren Zellen wirken. Diese Studie konzentriert sich auf Honokiol, einen Stoff aus der Rinde der Magnolie, der lange in der traditionellen Medizin verwendet wird, und zeigt, wie er direkt winzige Kraftwerke in Krebszellen anvisieren kann, um das Tumorwachstum zu verlangsamen und die Ausbreitung zu blockieren, während normale Zellen weitgehend verschont bleiben.
Die Kraftwerke in unseren Zellen
Jede Zelle ist auf Mitochondrien angewiesen, oft als die „Kraftwerke“ der Zelle bezeichnet, um das Energieträger-Molekül ATP zu erzeugen. Bei Krebs leisten Mitochondrien mehr als nur Treibstoffproduktion – sie helfen mit zu entscheiden, ob eine Zelle überlebt oder stirbt. Eine große molekulare Maschine, die ATP-Synthase, sitzt in der Innenmembran der Mitochondrien und stellt ATP her. Krebszellen produzieren oft im Übermaß ein Partnerprotein namens IF1, das sich an die ATP-Synthase heftet und wie eine Sicherung wirkt, wodurch Tumoren einer Form des Selbstzerstörungsprozesses, der mitochondrialen Permeabilitätstransition, und dem anschließenden Zelltod widerstehen.
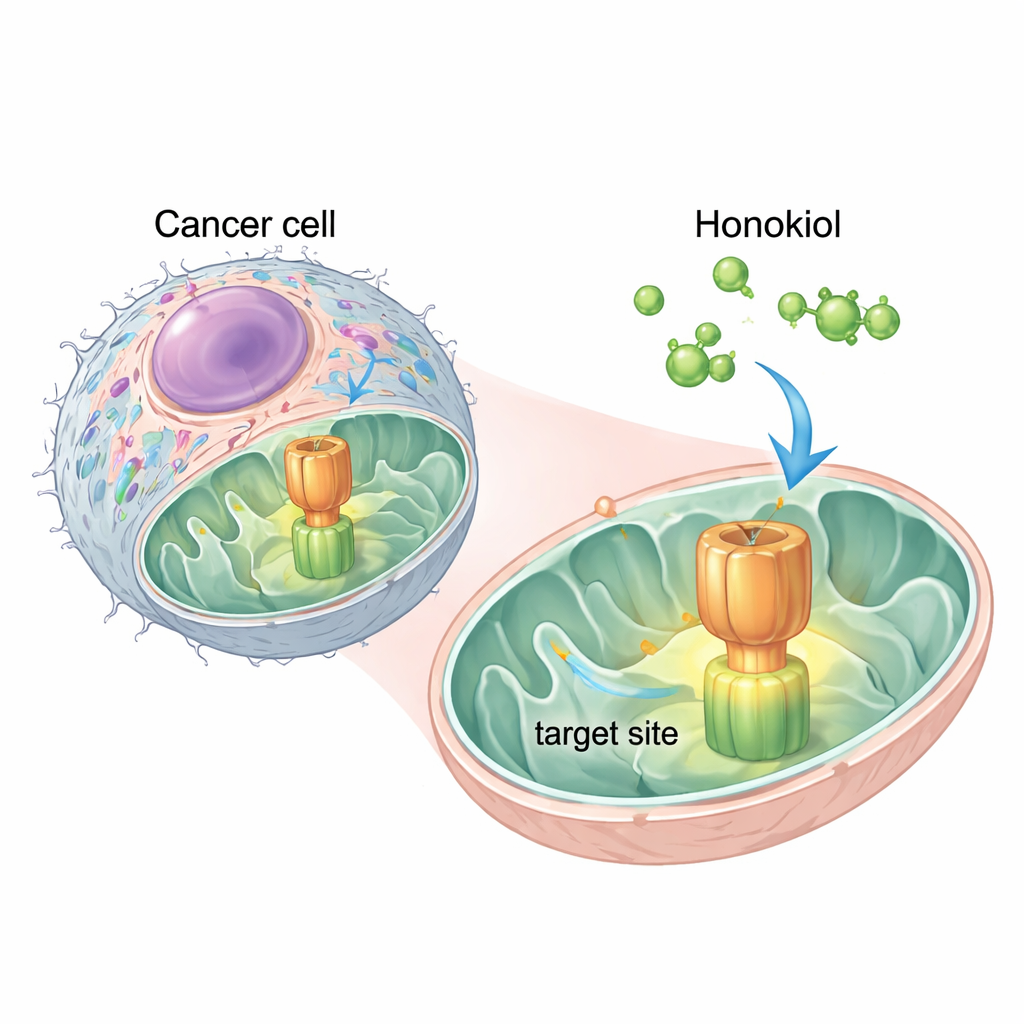
Ein natürliches Molekül trifft einen kritischen Schalter
Die Forschenden verwendeten Computersimulationen, um zu untersuchen, wo Honokiol an der ATP-Synthase anlagern könnte. Sie fanden zwei vielversprechende „Andock“-Stellen an einer ihrer Komponenten, einer Region namens OSCP. Die stärkste Stelle überlappte mit dem Bereich, den IF1 nutzt, um an der ATP-Synthase zu halten. Das deutete darauf hin, dass Honokiol wie ein molekularer Keil wirken könnte, der in OSCP einschiebt und IF1 wegdrängt. Experimente mit menschlichen Gebärmutterhalskrebs-HeLa-Zellen bestätigten diese Idee: Die Zugabe von Honokiol verringerte den physischen Kontakt zwischen IF1 und OSCP, ohne andere Teile des Enzyms zu stören, was zeigt, dass der Effekt spezifisch ist.
Von Zellen zu lebenden Tieren: Weniger Tumor, weniger Ausbreitung
Um zu prüfen, ob dieser molekulare Stoß reale Auswirkungen hat, setzten die Forschenden leuchtende menschliche Krebszellen in winzige Zebrafisch-Embryonen ein, ein etabliertes Ganztiermodell zur Verfolgung von Tumorwachstum und Metastasierung. In Fischen, die mit normalen, IF1-reichen HeLa-Zellen injiziert wurden, verkleinerte Honokiol die Tumormassen signifikant und verringerte die Zahl der Krebszellen, die in entfernte Bereiche streuten, sodass das Muster den Fischen ähnelte, die mit IF1-Knockout-Zellen ohne das schützende Protein injiziert worden waren. Interessanterweise reduzierte Honokiol auch die Anzahl metastasierender Zellen, selbst wenn IF1 fehlte, was auf einen zweiten, IF1-unabhängigen Mechanismus zur Begrenzung der Krebsverbreitung hindeutet.
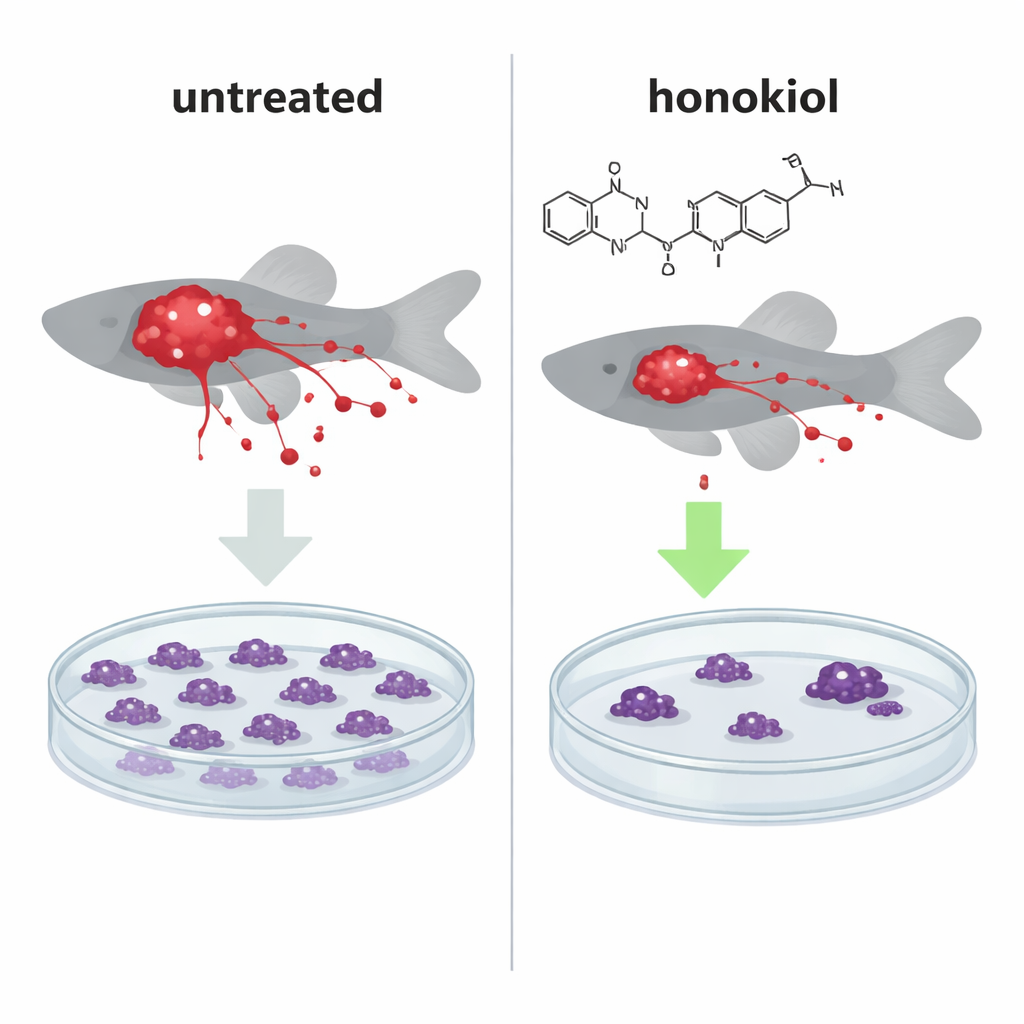
Fehlgeleitete Kraftwerke zum Selbstzerstörungsmodus zwingen
Im Reagenzglas verringerte Honokiol die Fähigkeit von Krebszellen, große Kolonien in weichem Agar zu bilden, einem Test, der die belastenden, sauerstoffarmen Bedingungen innerhalb solider Tumoren nachahmt. Dies geschah ohne eine deutliche Verlangsamung der gewöhnlichen Zellteilung oder der grundlegenden mitochondrialen Atmung und deutet stattdessen auf eine Veränderung darin hin, wie Mitochondrien zwischen Leben und Tod entscheiden. Messungen des Kalziumhandlings zeigten, dass Honokiol die Mitochondrien dazu brachte, den Permeabilitätstransition-Pore bei niedrigeren Kalziumwerten zu öffnen, ein bekannter Auslöser für Schwellung und Freisetzung von todesfördernden Faktoren. Bei moderaten Dosen hing dieser Effekt von der Verschiebung von IF1 ab; bei höheren Dosen wirkte Honokiol über seine zweite OSCP-Bindungsstelle und durch erhöhte reaktive Sauerstoffspezies und sensibilisierte so selbst IF1-defiziente Zellen für den programmierten Zelltod.
Krebszellen am Wegziehen hindern
Krebs wird am gefährlichsten, wenn Zellen sich lösen und in neue Organe wandern. In Wund-ähnlichen „Scratch“-Assays verlangsamte Honokiol stark die kollektive Migration von Zellschichten und verringerte Marker der epithelial‑mesenchymalen Transition, eines Prozesses, der Tumorzellen die Fähigkeit zum Bewegen und Eindringen verleiht. Detaillierte Elektronenmikroskopaufnahmen zeigten, dass wandernde Zellen normalerweise ihre Mitochondrien vergrößern und umgestalten, indem sie innere Falten hinzufügen, um den hohen Energiebedarf an der Vorhut zu decken. Unter Honokiol wurden diese Front‑Mitochondrien stattdessen geschwollen und strukturell geschädigt – Kennzeichen der Öffnung des Permeabilitätstransition-Pores – während Mitochondrien in nicht bewegten Bereichen weniger betroffen waren oder je nach IF1 sogar in der Zahl zunahmen.
Was das für zukünftige Krebstherapien bedeutet
Kurz gesagt, diese Arbeit zeigt, dass Honokiol eine kleine regulatorische Region der mitochondrialen ATP-Bildungsmaschine anvisieren und einen eingebauten Sicherheitsschalter umlegen kann, den Krebszellen häufig arretiert halten. Indem es IF1 verdrängt und den Porus direkt in Richtung Öffnung drängt, fördert Honokiol das Selbstzerstören von Tumorzellen und erschwert ihnen die Migration und das Aussäen von Metastasen. Da diese Effekte auf Merkmalen beruhen, die viele Krebsarten teilen – und nicht auf einem einzelnen Oberflächenmarker – könnte das gezielte Ansprechen der OSCP-Region der ATP-Synthase eine neue Klasse von Therapien inspirieren, die die Verwundbarkeiten der Kraftwerke von Krebszellen ausnutzen und gleichzeitig Schäden an gesundem Gewebe begrenzen.
Zitation: Grandi, M., Boldrin, F., Risato, G. et al. Honokiol blocks tumor development and metastasis through mitochondrion-targeted effects. Cell Death Dis 17, 186 (2026). https://doi.org/10.1038/s41419-026-08441-6
Schlüsselwörter: honokiol, Mitochondrien, ATP-Synthase, Apoptose, Metastasen