Clear Sky Science · de
Immune-Checkpoint-Inhibitor-assoziierte Pneumonitis: aktuelle Fortschritte und die vermutete Rolle der mesenchymalen Stammzelltherapie
Wenn die Krebstherapie der Lunge schadet
Medikamente, die das Immunsystem gegen Krebs entfesseln, haben die Behandlung von Erkrankungen wie Lungenkrebs und Melanom revolutioniert. Diese neue Macht hat jedoch einen Haken: Bei einigen Patientinnen und Patienten richtet derselbe Immunangriff, der Tumoren trifft, auch Schaden in der Lunge an und verursacht eine Erkrankung namens immune‑checkpoint‑inhibitor‑assoziierte Pneumonitis (ICIP). Diese Übersicht erklärt, was ICIP ist, warum sie entsteht, wie Ärzte sie derzeit behandeln und weshalb eine besondere Art von Stammzellen – mesenchymale Stammzellen (MSCs) – eines Tages eine sicherere, zielgenauere Möglichkeit bieten könnte, die Entzündung zu dämpfen, ohne die Krebsbekämpfung zu gefährden. 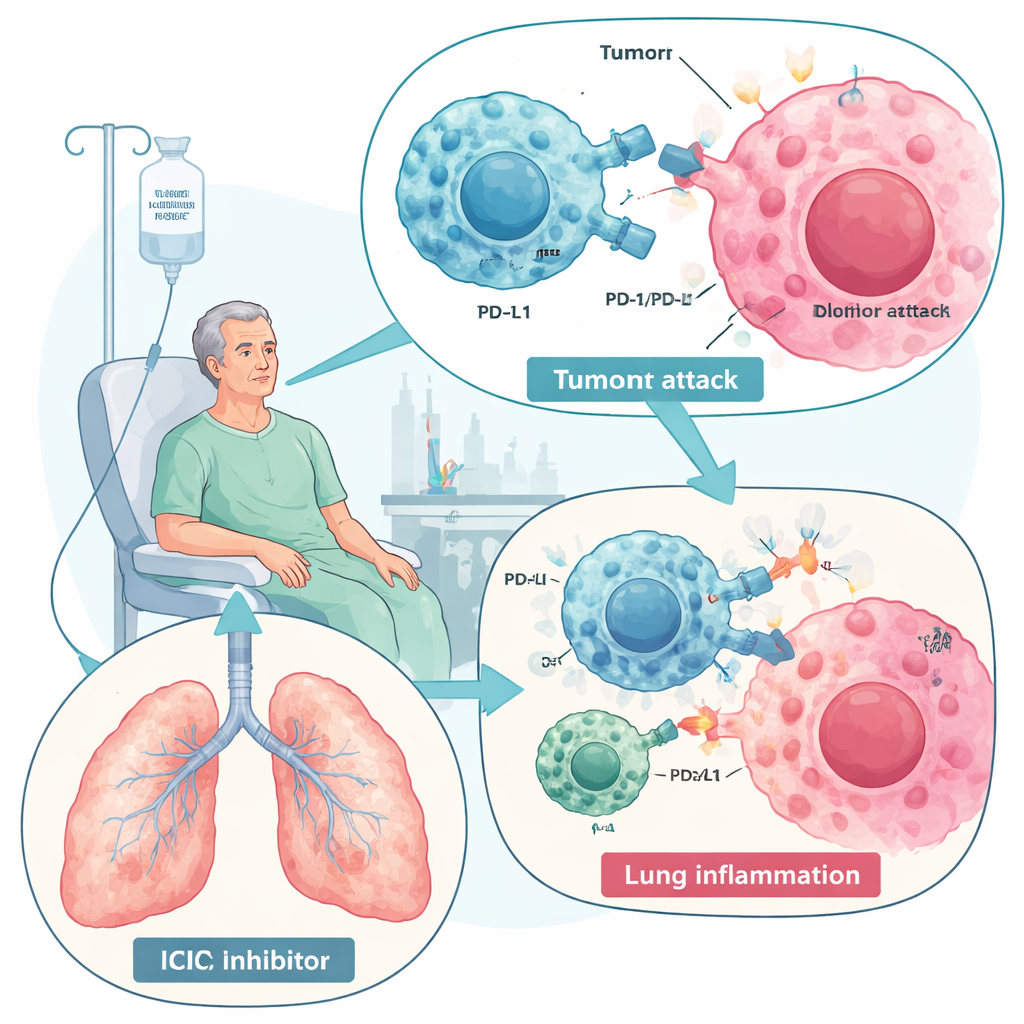
Starke Krebsmedikamente mit verborgenem Lungenrisiko
Immune‑Checkpoint‑Inhibitoren, insbesondere solche, die PD‑1 und PD‑L1 blockieren, wirken, indem sie molekulare „Bremsen“ entfernen, die normalerweise Immunreaktionen begrenzen. Sind diese Bremsen gelöst, können T‑Zellen Krebszellen besser erkennen und zerstören, was in vielen Tumorarten das Überleben verbessert. Dieser Schub kann jedoch die normale Toleranz stören und immunbedingte Nebenwirkungen in verschiedenen Organen auslösen. ICIP ist die schwerwiegendste Lungenkomplikation dieser Medikamente und eine der führenden immunbedingten Todesursachen im Kontext der Behandlung. Die Häufigkeit reicht von wenigen Prozent bis in einigen Real‑World‑Studien fast ein Drittel der Patientengruppen, besonders bei Menschen mit Lungenkrebs oder bereits bestehender Lungenerkrankung wie COPD oder interstitieller Lungenerkrankung. Die Symptome reichen von leichtem Husten und Atemnot bis hin zu lebensbedrohlichem Atemversagen.
Wie das Immunsystem die Lunge schädigt
Die Übersicht beschreibt ICIP als Folge eines gestörten immunologischen Gleichgewichts in der Lunge. Überaktivierte „Kämpfer“‑Zellen — CD8‑T‑Zellen, bestimmte Helfer‑T‑Zellen, proinflammatorische Makrophagen, Neutrophile und natürliche Killerzellen — überschwemmen das Lungengewebe und setzen aggressive Botenstoffe frei, darunter Interferon‑gamma, TNF‑alpha und Interleukine wie IL‑6 und IL‑17. Gleichzeitig sind normalerweise schützende Zellen, die Entzündungen dämpfen, wie regulatorische T‑Zellen und reparationsorientierte Makrophagen, reduziert. Bei einigen Patienten steigen auch die Spiegel selbstreaktiver Antikörper vor oder während der Behandlung, was darauf hindeutet, dass ICIP teilweise einer Autoimmunerkrankung ähneln könnte. Im bronchoalveolären Spülfluid finden sich ein T‑Zell‑reiches Entzündungsmuster und ein Zytokinprofil, das sich von einer Infektion oder Tumorprogression unterscheidet und bei der Diagnose helfen kann.
Erkennen, Einstufen und Behandeln des Schadens
Im CT zeigt sich ICIP am häufigsten als diffuse „Ground‑Glass“‑Trübungen oder fleckige Konsolidierungen, die in beiden Lungenflügeln verstreut auftreten — Muster, die sich von Strahlenschäden unterscheiden, welche auf das bestrahlte Feld beschränkt bleiben. Ärzte stellen die Diagnose ICIP durch Kombination von Bildbefunden, Symptomen und einem sorgfältigen Ausschluss von Infektion und anderen Ursachen. Internationale Leitlinien stufen die Schwere dann von 1 (leicht, oft nur radiologisch) bis 4 (lebensbedrohliches Atemversagen) ein. Die heutige Behandlungssäule sind Glukokortikoide — starke entzündungshemmende Steroide — die in schweren oder steroidresistenten Fällen manchmal mit anderen immundämpfenden Wirkstoffen wie Tocilizumab (IL‑6‑Blockade) oder Infliximab (TNF‑alpha‑Blockade) kombiniert werden. Diese Maßnahmen können lebensrettend sein, sind aber grobe Werkzeuge: Steroide haben viele Nebenwirkungen, manche Patienten sprechen nicht an, und eine breite Immunsuppression kann genau die anti‑tumorale Reaktion schwächen, die die Therapie fördern sollte.
Warum Stammzellen ins Gespräch kommen
Mesenchymale Stammzellen, die aus Knochenmark, Fettgewebe oder Nabelschnur gewonnen werden können, sind als vielversprechende „Immunmodulatoren“ in den Blick geraten, nicht nur als einfache Geweberegeneratoren. Nach intravenöser Gabe bleiben viele dieser Zellen vorübergehend in den feinen Blutgefäßen der Lunge stecken — ein sogenannter First‑Pass‑Effekt — was für die Behandlung entfernter Organe ein Nachteil, für Lungenerkrankungen aber ein potenzieller Vorteil ist. In Tiermodellen und frühen Humanstudien zu schweren Pneumonien, akutem Lungenversagen, entzündlichen Darmerkrankungen und Graft‑versus‑Host‑Krankheit dämpfen MSCs überaktive Immunantworten, verschieben Immunzellen in einen ausgewogeneren Zustand und sezernieren Wachstumsfaktoren, die Gewebereparatur fördern und Narbenbildung begrenzen. Wichtig ist: Ihre Wirkung beruht oft weniger auf der Differenzierung zu Lungenzellen als auf dem Gemisch aus Signalmolekülen und kleinen Vesikeln, das sie freisetzen. 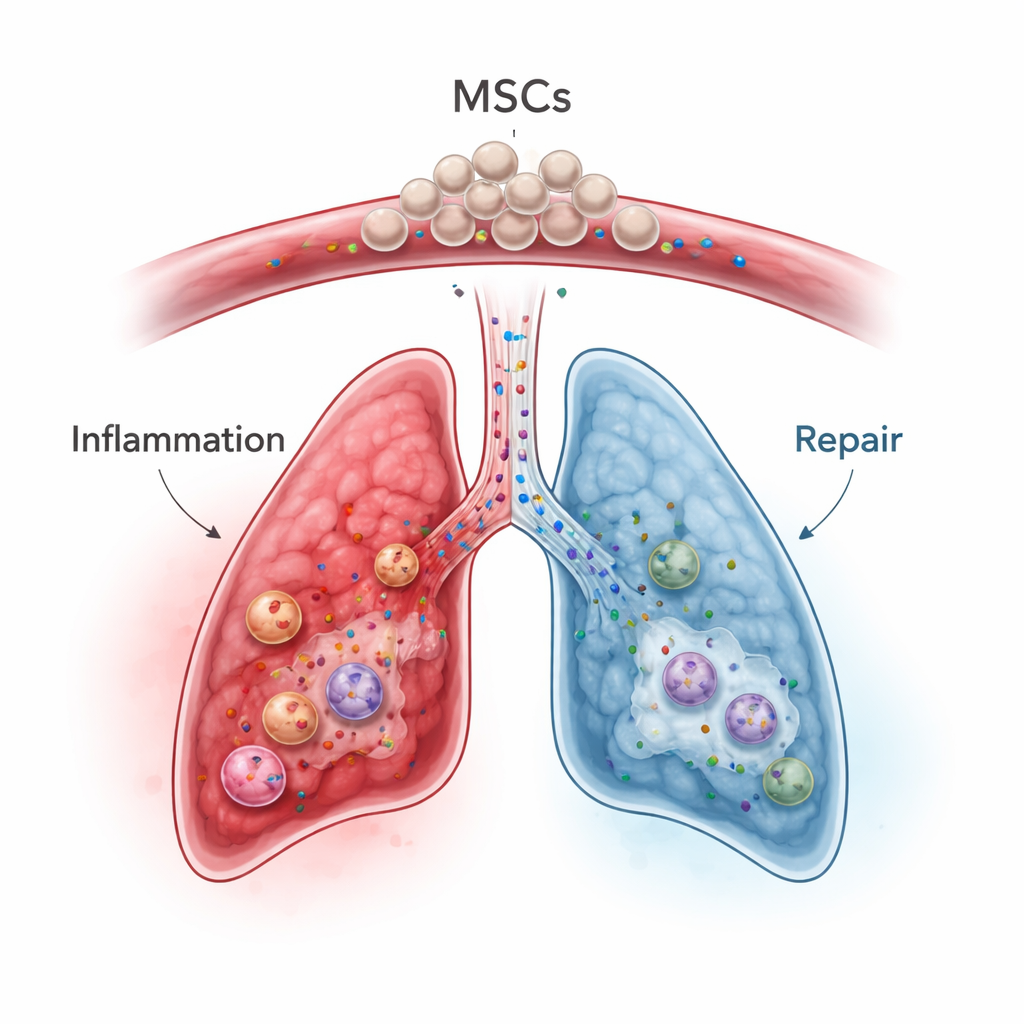
Wie MSCs ICIP beruhigen könnten, ohne die Heilung zu zerstören
Im Kontext von ICIP könnten MSCs theoretisch mehrere Probleme gleichzeitig adressieren. Sie können aktivierte T‑Zellen direkt hemmen, das Wachstum und die Funktion regulatorischer T‑Zellen fördern und Makrophagen von einem aggressiven, gewebeschädigenden Zustand hin zu einem heilungsfördernden Phänotyp lenken. Außerdem senken sie zentrale Entzündungsmediatoren wie IL‑6, IL‑1β und TNF‑alpha und erhöhen antiinflammatorische Faktoren und schützende Proteine wie TSG‑6, die helfen, Lungenverletzung und Fibrose zu begrenzen. Präklinische Arbeiten deuten darauf hin, dass MSCs oder gentechnisch veränderte MSC‑abgeleitete Exosomen Zytokinstürme und Organverletzung, ausgelöst durch Checkpoint‑Inhibitoren oder Strahlung, reduzieren können, während sie in einigen Modellen die antitumorale Aktivität besser erhalten als Standard‑Immunosuppressiva. Die Autoren warnen jedoch, dass MSCs auch komplex mit Tumoren und der Blutgerinnung interagieren können und dass ihre Effekte stark vom umgebenden Entzündungsumfeld und sogar von der MSC‑Quelle (Knochenmark, Fettgewebe oder Nabelschnur) abhängen.
Ausblick: Hoffnung mit sorgfältiger Prüfung
Für Patientinnen und Patienten, deren Krebstherapie wegen schwerer Lungentoxizität unterbrochen oder gefährdet ist, könnten MSC‑basierte Therapien künftig einen zielgerichteteren Weg bieten, Entzündung zu kühlen, Lungengewebe zu reparieren und langfristige Narbenbildung zu verhindern — idealerweise ohne die lebensrettenden Vorteile der Checkpoint‑Hemmung aufzuheben. Bisher wurde jedoch keine ICIP‑spezifische MSC‑Studie abgeschlossen. Die Autoren fordern dringend sorgfältig konzipierte Tierstudien und klinische Prüfungen, um zu klären, welcher Typ von MSCs oder Exosomprodukt am besten wirkt, welche Dosis geeignet ist, wann die Anwendung im Verhältnis zu Steroiden und Immuntherapie erfolgen sollte und wie Risiken wie Tumorwachstum oder Thromboseneigung überwacht werden können. Bis dahin bleiben MSCs eine hoffnungsvolle, aber noch experimentelle Option am Horizont für das Management dieser schweren Nebenwirkung moderner Krebstherapie.
Zitation: Li, Z., Zheng, X., Xia, H. et al. Immune checkpoint inhibitor-related pneumonitis: current advances and the putative role of mesenchymal stem cell therapy. Cell Death Dis 17, 200 (2026). https://doi.org/10.1038/s41419-026-08440-7
Schlüsselwörter: Nebenwirkungen der Immuntherapie, Pneumonitis, Checkpoint-Inhibitoren, mesenchymale Stammzellen, Lungenentzündung