Clear Sky Science · de
c-Myc/GRPEL1 erhalten die Fettsäuresynthese über FASN zur Unterstützung der PDAC-Zellproliferation
Warum der Fettbedarf von Krebszellen wichtig ist
Pankreaskrebs gehört zu den tödlichsten Krebsarten, teilweise weil seine Zellen Meister darin sind, ihren Stoffwechsel umzuprogrammieren, um zu überleben und zu wachsen. Diese Studie beleuchtet einen überraschenden Teil dieser Geschichte: wie Pankreastumorzellen ihre inneren „Fettfabriken“ hochfahren, um unaufhörliches Wachstum zu befeuern, und wie das Blockieren dieses Prozesses neue Therapieoptionen für Patientinnen und Patienten eröffnen könnte.
Ein schwer zu bekämpfender Krebs mit metabolischem Vorteil
Die meisten Pankreaskrebse gehören zum Typ des duktalen Adenokarzinoms des Pankreas (PDAC), das meist spät entdeckt wird und schlecht auf aktuelle Therapien anspricht. PDAC-Zellen leben in einer rauen Umgebung mit wenig Sauerstoff und knappen Nährstoffen, gedeihen aber, indem sie den Umgang mit Zucker, Fetten und anderen Brennstoffen neu verdrahten. Ihre Mitochondrien — winzige Kraftwerke in den Zellen — spielen eine zentrale Rolle bei dieser Umprogrammierung. Um diese Kraftwerke am Laufen zu halten, überwachen und reparieren Zellen ständig Tausende mitochondrialer Proteine, ein Prozess, der als mitochondriale Proteinqualitätskontrolle bekannt ist. Bislang war unklar, wie diese Qualitätskontrolle mit der Art und Weise verknüpft ist, wie Pankreastumoren sich selbst versorgen.
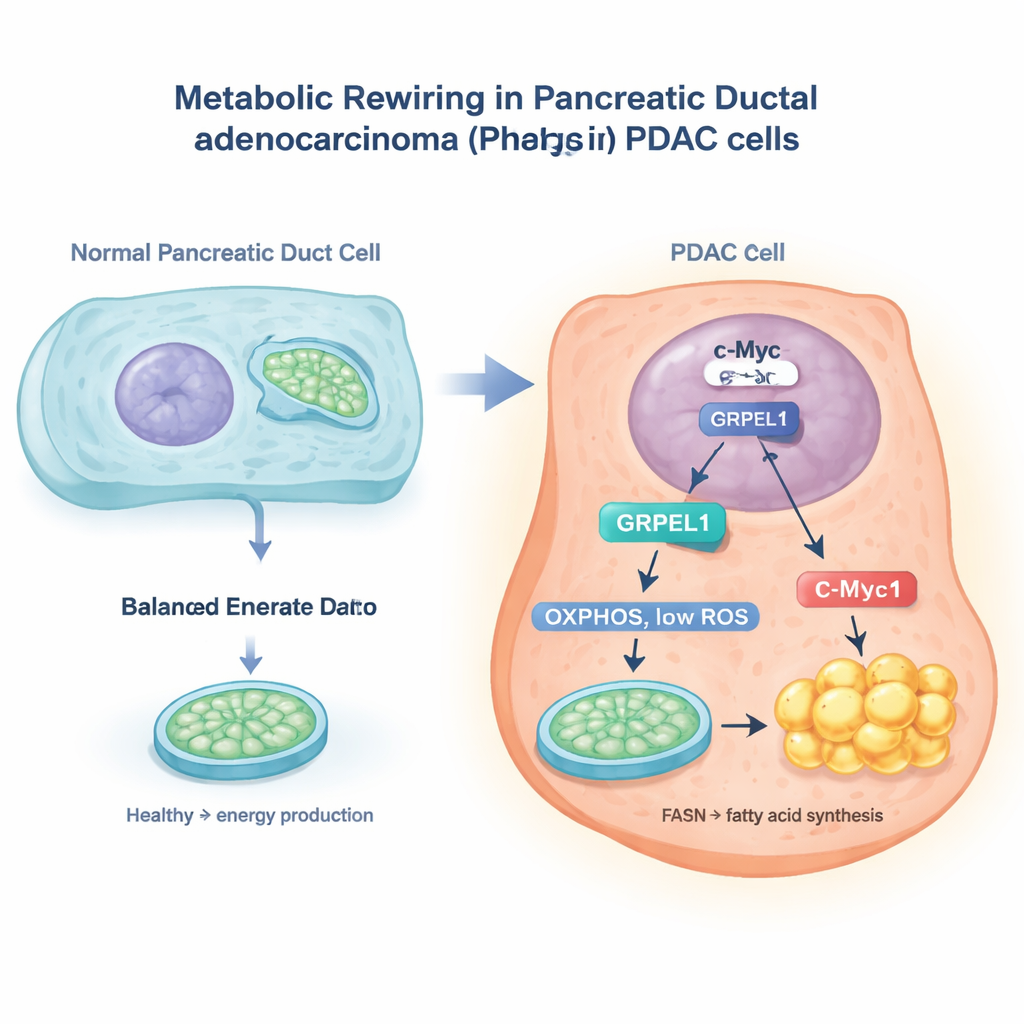
Der c-Myc-Schalter und ein mitochondrialer Helfer
Die Forschenden nutzten große Krebsdatenbanken und Experimente in Pankreaskrebszellen, um ein Protein namens GRPEL1 ins Visier zu nehmen, das bei der mitochondrialen Proteinverarbeitung hilft. Sie entdeckten, dass ein bekanntes Krebsgen, c-Myc, im Zellkern wie ein molekularer Schalter wirkt und das GRPEL1-Gen anschaltet. Sinkt der c-Myc-Spiegel, fällt auch GRPEL1; steigt c-Myc, erhöht sich GRPEL1. Tumorproben von Patientinnen und Patienten zeigten ebenfalls, dass c-Myc und GRPEL1 häufig gemeinsam hoch exprimiert sind und mit schlechteren Prognosen verknüpft sind. In im Labor gezüchteten PDAC-Zellen verlangsamte das Reduzieren von GRPEL1 die Zellteilung und Koloniebildung, während zusätzliches GRPEL1 das Zellwachstum beschleunigte, besonders wenn c-Myc anderweitig blockiert war.
Von den Mitochondrien zur Fettproduktion
Tiefer gehende Untersuchungen zeigten, dass GRPEL1 mehr tut, als nur mitochondriale Proteine zu verwalten. Bei GRPEL1-Mangel wurden die Mitochondrien in PDAC-Zellen weniger effizient bei der Energieerzeugung, verloren ihre normale Gestalt und setzten mehr reaktive Sauerstoffspezies (ROS) frei — chemisch reaktive Nebenprodukte, die man manchmal als zellulären „Rost“ bezeichnet. Dieser ROS-Anstieg hatte Folgen: Er senkte die Mengen an Fettsäuresynthase (FASN), einem Schlüsselenzym für den Aufbau neuer Fettsäuren in der Zelle. Mit reduziertem FASN produzierten die Zellen weniger Fette, speicherten weniger Lipide und ihr Wachstum verlangsamte sich. Als die Forschenden ROS mit einem Antioxidans neutralisierten, erholten sich die FASN-Werte, was zeigt, dass die Verbindung zwischen GRPEL1 und FASN durch ROS vermittelt wird. Interessanterweise schien c-Myc in diesem System nicht direkt das FASN-Gen anzuschalten, sondern beeinflusste FASN indirekt über GRPEL1 und mitochondrialen Stress.
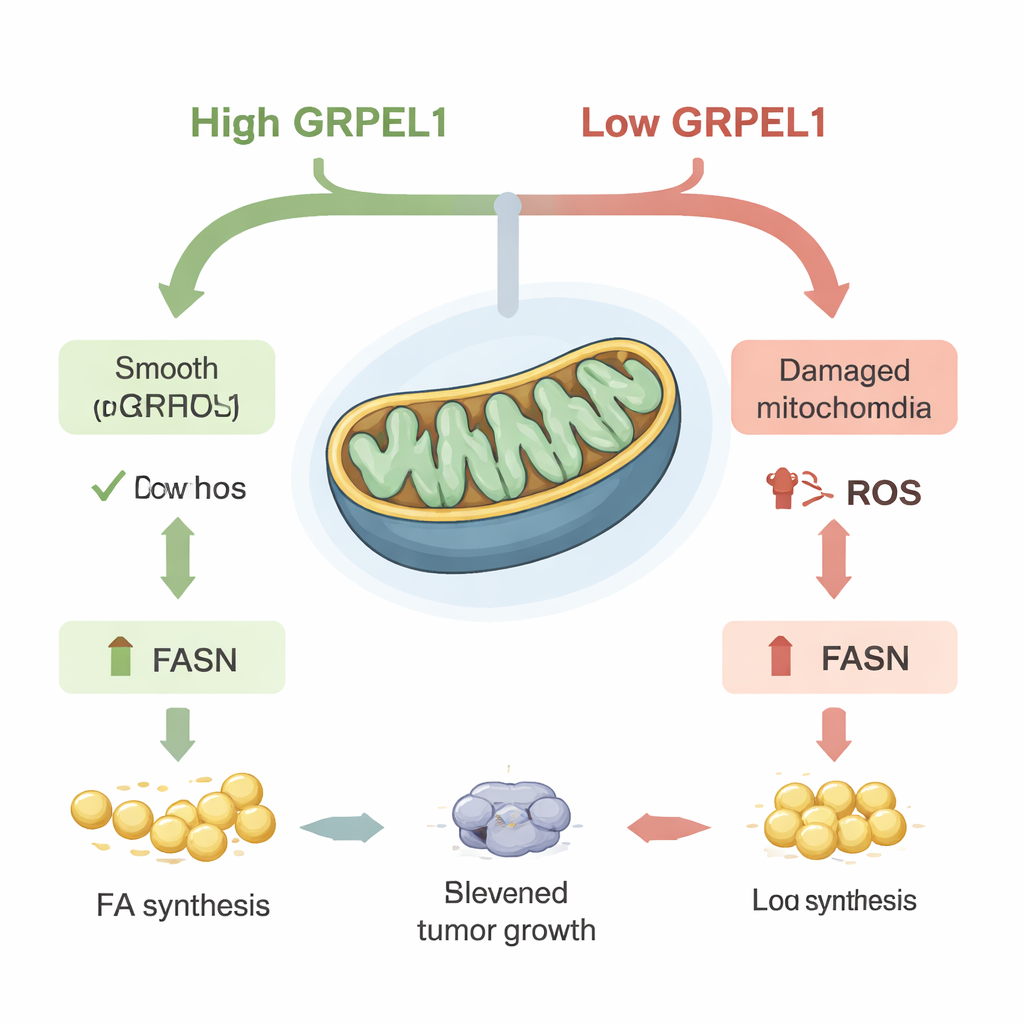
Fett als Treibstoff für Tumorwachstum
Da FASN im Zentrum der Fettbildung steht, prüften die Wissenschaftlerinnen und Wissenschaftler, ob die Wiederherstellung von FASN das Tumorwachstum retten kann, wenn GRPEL1 niedrig ist. In Zellkulturen konnte das erzwungene Hochregulieren von FASN das verlangsamte Wachstum und die verringerte Koloniebildung durch GRPEL1-Verlust teilweise rückgängig machen. Dasselbe galt in Mäusen: Tumoren aus GRPEL1-armen Zellen wuchsen langsamer, aber die Wiedereinführung von FASN belebte sowohl Tumorgröße als auch Fettgehalt wieder. Detaillierte Analysen von Metaboliten und Lipiden zeigten breite Abnahmen vieler fettbezogener Moleküle, wenn GRPEL1 oder c-Myc reduziert wurden. Wichtig ist, dass das Zuführen zusätzlicher Fettsäuren oder einer Lipidmischung von außen das Wachstum in Krebszelllinien und patientenabgeleiteten pankreatischen Tumor-Organoiden — Mini-Tumoren in 3D-Kultur — teilweise wiederherstellte, was darauf hindeutet, dass das Hauptproblem der Verlust neu synthetisierter Fette war.
Eine Verwundbarkeit in eine Therapie verwandeln
Insgesamt zeichnet die Arbeit ein klares Bild: Bei Pankreaskrebs erhöht c-Myc GRPEL1, was den Mitochondrienbetrieb stabilisiert und ROS in Schach hält. Diese ruhige mitochondriale Umgebung ermöglicht es den Zellen, hohe FASN-Spiegel aufrechtzuerhalten und ständig neue Fettsäuren zu produzieren, die als Bausteine für Membranen, Energiespeicher und Wachstumssignale dienen. Wird GRPEL1 blockiert, versagen die Mitochondrien, ROS steigt, FASN sinkt und die Krebszellen können nur noch schlecht wachsen — ein Effekt, der teilweise umgangen werden kann, wenn Fette von außen zugeführt werden. Für den Laien lautet die Kernbotschaft: Pankreastumoren sind auf eine interne „Fettfabrik“-Schaltung angewiesen, die von c-Myc, GRPEL1 und FASN angetrieben wird. Medikamente, die diese Fettsäurebildungsachse stören, insbesondere in Tumoren, in denen sie besonders aktiv ist, könnten einen vielversprechenden Weg bieten, Pankreaskrebszellen gezielt zu „verhungern“, während normales Gewebe weniger betroffen bleibt.
Zitation: Wang, J., Zhang, L., Chen, K. et al. c-Myc/GRPEL1 maintains fatty acid synthesis via FASN to support PDAC cell proliferation. Cell Death Dis 17, 205 (2026). https://doi.org/10.1038/s41419-026-08439-0
Schlüsselwörter: Pankreaskrebs, Tumorstoffwechsel, Fettsäuresynthese, Mitochondrien, c-Myc