Clear Sky Science · de
Erholung von Apoptose in Photorezeptorzellen: Eine Rolle für Mitophagie
Wenn sterbende Augenzellen eine zweite Chance bekommen
Viele erblindende Erkrankungen beginnen auf die gleiche Weise: lichtempfindliche Zellen im Auge, sogenannte Photorezeptoren, beginnen zu sterben und kehren nicht zurück. Diese Studie enthüllt eine überraschende Wendung. Unter den richtigen Bedingungen können Photorezeptoren, die scheinbar am Rande des programmierten Zelltods stehen, sich zurückziehen, zentrale Teile reparieren und überleben. Zu verstehen, wie diese „zweite Chance" funktioniert, könnte neue Wege öffnen, das Sehvermögen bei Zuständen wie Netzhautablösung und altersbedingter Makuladegeneration zu erhalten.
Augenzellen in Gefahr bei häufigen Erblindungsursachen
Photorezeptoren sitzen im hinteren Teil des Auges und wandeln Licht in elektrische Signale um, die das Gehirn verarbeiten kann. Sobald diese Zellen ausgereift sind, teilen sie sich nicht mehr; wenn sie also absterben, ist das Sehen dauerhaft beeinträchtigt. Bei Netzhautablösungen und anderen Netzhauterkrankungen sterben Photorezeptoren häufig durch Apoptose, ein aufgeräumtes Selbstzerstörungsprogramm, das lange als unumkehrbar galt, sobald es voll in Gang gesetzt ist. Klinische Beobachtungen haben jedoch angedeutet, dass eine rasche Wiederanlagerung einer abgelösten Netzhaut nützliches Sehen wiederherstellen kann, was darauf hindeutet, dass zumindest manche Photorezeptoren gerettet werden können, selbst nachdem sie diesen Todesweg eingeschlagen haben.
Vom Todesstrudel zur Erholung
Die Forschenden verwendeten eine Maus-Konen-Photorezeptorzelllinie, um zu untersuchen, ob diese Zellen sich nach starker Belastung erholen können. Sie setzten die Zellen zwei starken Auslösern der Apoptose aus: einem Wirkstoff, der interne Todeswege aktiviert, und langanhaltenden Niedrigsauerstoffbedingungen, die das bei Netzhautablösung eintreten nachahmen. Unter beiden Stressbedingungen zeigten die Zellen klassische Apoptosezeichen: sie rundeten sich ab, bildeten Membranbläschen, aktivierten Schlüsselenzyme, die Proteine zerschneiden, und zeigten Stresssignale an ihrer Oberfläche. Als der Stress jedoch entfernt wurde, gewannen viele Zellen allmählich ihre ursprüngliche längliche Form zurück und schalteten die Todesmaschinerie innerhalb von etwa 24 Stunden ab, was zeigt, dass selbst spätere Veränderungen nicht immer ein Einbahnstraßenprozess sind.
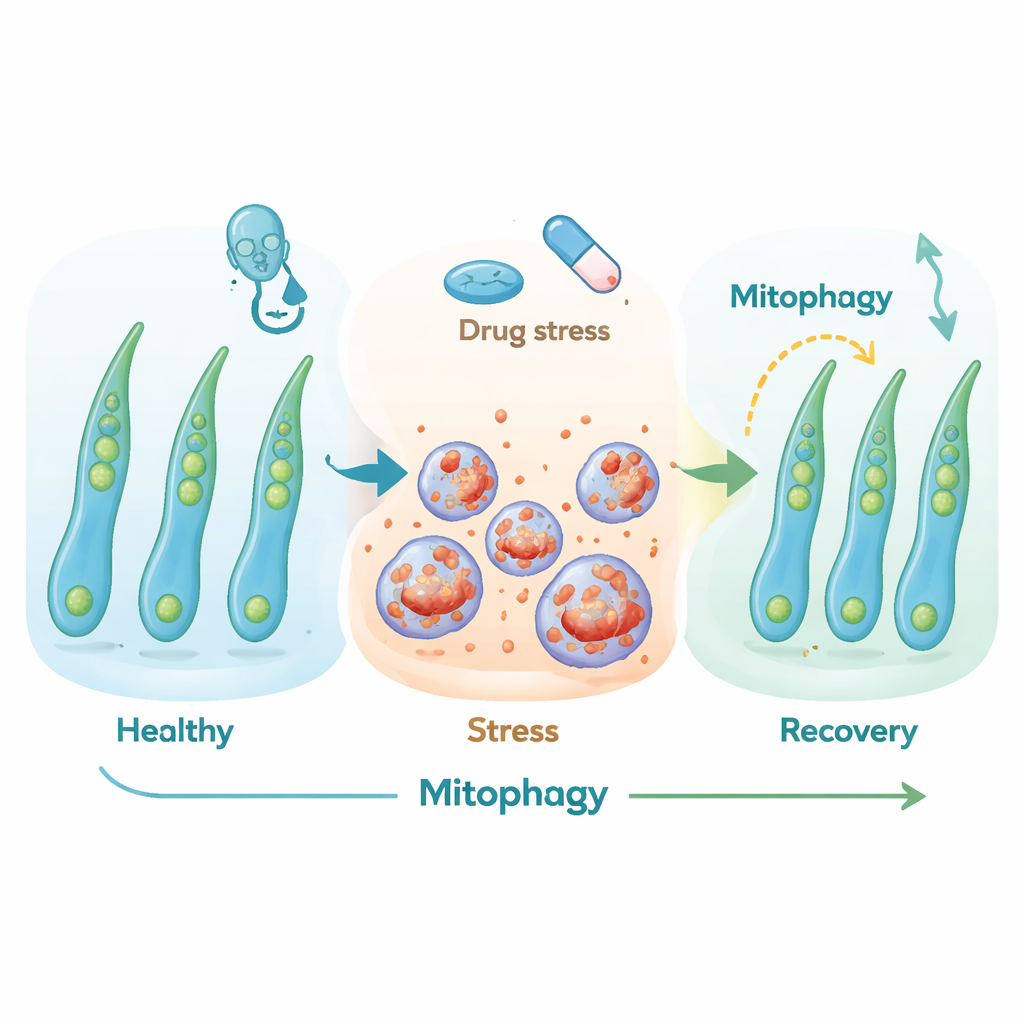
Reparatur der Kraftwerke
Um zu verstehen, wie diese Zellen sich erholen konnten, richtete das Team den Blick auf die Mitochondrien — die winzigen Kraftwerke, die zelluläre Energie liefern und mitentscheiden, ob eine Zelle lebt oder stirbt. Während des Stresses versagte die mitochondriale Funktion: die Energielevels sanken in medikamentös behandelten Zellen, und schädliche Sauerstoffnebenprodukte stiegen in beiden Stressmodellen an. Nachdem der Stress aufgehoben war, stellten überlebende Zellen ihre Energielevels wieder her, reduzierten schädliche reaktive Sauerstoffspezies und zeigten Hinweise auf erneute Mitochondrienproduktion. Das Gleichgewicht zwischen mitochondrialer Teilung und Fusion verschob sich ebenfalls in eine Richtung, die die Bereinigung beschädigter Komponenten und den Wiederaufbau eines gesünderen Netzwerks unterstützt.
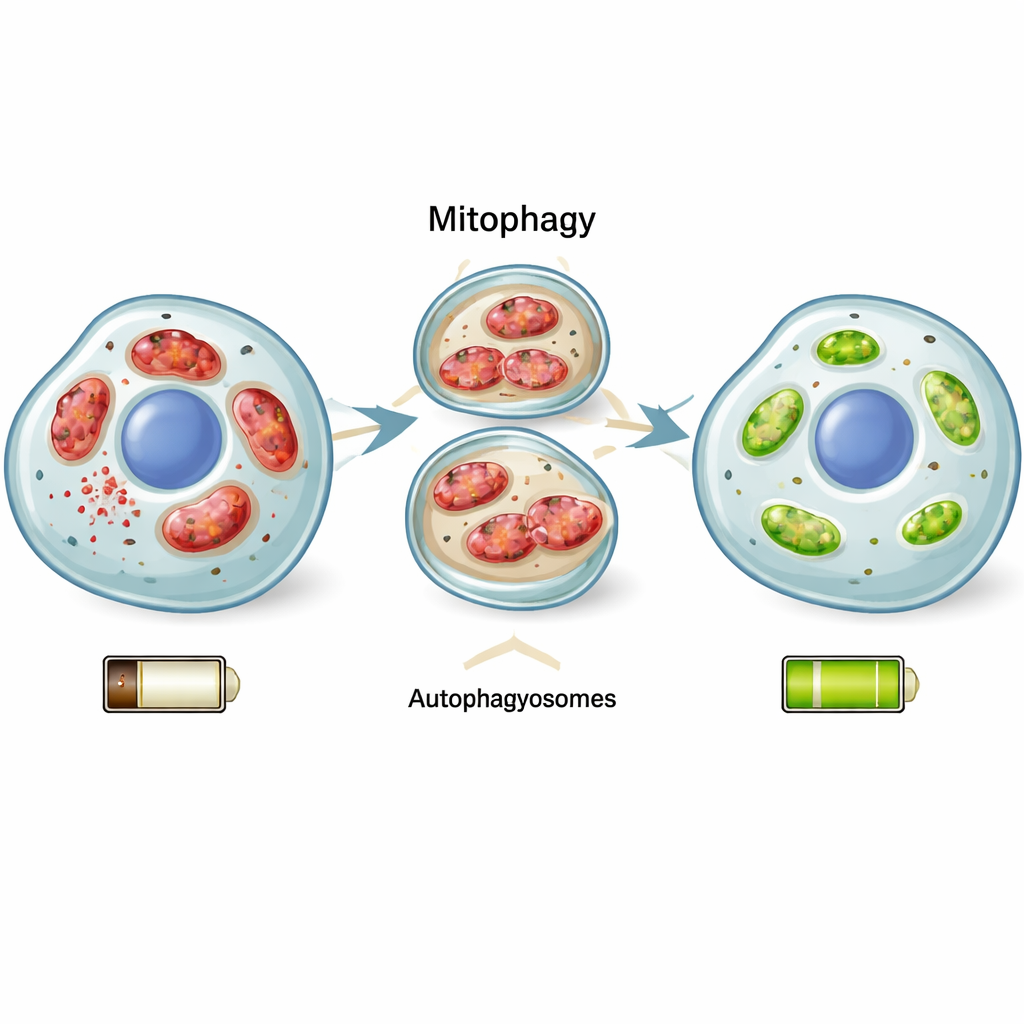
Mitophagie: gezielte Reinigung, die Zellen rettet
Eine zentrale Rolle in dieser Wende spielte die Mitophagie, ein Qualitätskontrollprozess, der defekte Mitochondrien selektiv entfernt, bevor sie den Rest der Zelle vergiften können. Die Forschenden fanden heraus, dass sich beim Erholen der Photorezeptoren Gene und Proteine hochfuhren, die Mitophagie und allgemeines zelluläres Recycling antreiben. Als sie die Mitophagie mit einem Wirkstoff förderten, der diesen Aufräumweg unterstützt, gingen weniger Zellen zugrunde. Wurde die Mitophagie blockiert, war die Erholung praktisch aufgehoben und mehr Zellen erlagen dem Stress. Das spricht dafür, dass Mitophagie nicht nur ein Begleitphänomen, sondern eine entscheidende Überlebensstrategie ist.
Nachweis im lebenden Auge
Zellkultur-Experimente haben ihre Grenzen, daher entwickelten die Forschenden ein Mausmodell, bei dem ein Teil der Netzhaut abgelöst und innerhalb weniger Tage wieder natürlich angelegt ist. In diesen Tieren zeigten die Photorezeptoren in den wieder angelegten Bereichen deutlich weniger Todesmarker und eine besser erhaltene Struktur als in Augen, bei denen die Ablösung dauerhaft hergestellt wurde. Dieses lebende System spiegelt gut wider, was bei Patienten passiert, deren Netzhaut chirurgisch wieder angelegt wird, und stützt die Idee, dass echte Photorezeptoren im Auge sich von starkem Stress erholen können, wenn der Schädigungsreiz rechtzeitig beseitigt wird.
Was das für das Seherhalten bedeuten könnte
Kurz gesagt zeigt die Studie, dass Photorezeptoren manchmal ein weit fortgeschrittenes Selbstzerstörungsprogramm stoppen und umkehren können, sofern ihre mitochondrialen „Motoren" durch Mitophagie repariert werden. Das stellt die alte Vorstellung in Frage, dass diese lichtempfindlichen Zellen nach Eintritt der Apoptose zwangsläufig dem Untergang geweiht sind. Wenn künftige Therapien die Mitophagie und andere mitochondriale Reparaturwege zum richtigen Zeitpunkt — etwa im Umfeld einer Netzhautwiederanlagerung — sicher verstärken können, könnten Ärztinnen und Ärzte mehr Photorezeptoren erhalten und so das Sehvermögen gefährdeter Patientinnen und Patienten besser bewahren.
Zitation: Kaur, B., Miglioranza Scavuzzi, B., Yao, J. et al. Recovery from apoptosis in photoreceptor cells: A role for mitophagy. Cell Death Dis 17, 167 (2026). https://doi.org/10.1038/s41419-026-08436-3
Schlüsselwörter: Photorezeptoren, Netzhautablösung, Apoptose, Mitophagie, Mitochondrien