Clear Sky Science · de
TGFβ-Signal fördert Zellzyklusfortschritt und Resistenz gegen den CDK4/6-Inhibitor Palbociclib durch SOX4-Transkriptionsmodulation in Brustkrebszellen
Wenn Krebszellen ein eigentlich hilfreiches Signal kapern
Unser Körper ist auf zahllose chemische Signale angewiesen, die dafür sorgen, dass Zellen bei Bedarf teilen und aufhören, wenn es erforderlich ist. Eines dieser Signale, das Transforming Growth Factor Beta (TGFβ) genannt wird, hilft normalerweise, Tumoren zu verhindern. Diese Studie zeigt, wie dasselbe TGFβ-Signal in bestimmten Brustkrebsarten verdreht werden kann, sodass Tumorzellen damit wachsen und einem wichtigen Medikament, Palbociclib, widerstehen. Das Verständnis dieses Umschaltmechanismus könnte bessere Kombinationsbehandlungen für Patientinnen und Patienten ermöglichen, deren Tumore nicht mehr auf Therapien ansprechen.
Vom Wachstumsbremsen zum zweischneidigen Signal
Im gesunden Gewebe wirkt TGFβ meist wie eine Bremse: Es verlangsamt die Zellteilung und begrenzt Entzündungen, wodurch frühe Tumorbildung verhindert wird. In etablierten Krebserkrankungen, besonders in Brusttumoren, die bereits krebsfördernde Mutationen erworben haben, kann TGFβ jedoch das Gegenteil bewirken—es fördert Migration, Invasion und Metastasierung. Um dieses doppelte Verhalten zu untersuchen, verwendeten die Forschenden 3D-„Mini-Tumore“, die aus menschlichen Brustzellen gezüchtet wurden. Sie verglichen normalartige Zellen mit ansonsten identischen Zellen, die eine onkogene HRAS-Mutation tragen, welche sie in Richtung Krebs drängt. Dieses kontrollierte System erlaubte es ihnen, zu untersuchen, wie sich dasselbe TGFβ-Signal in einer präkanzerösen gegenüber einer krebsähnlichen Umgebung auswirkt. 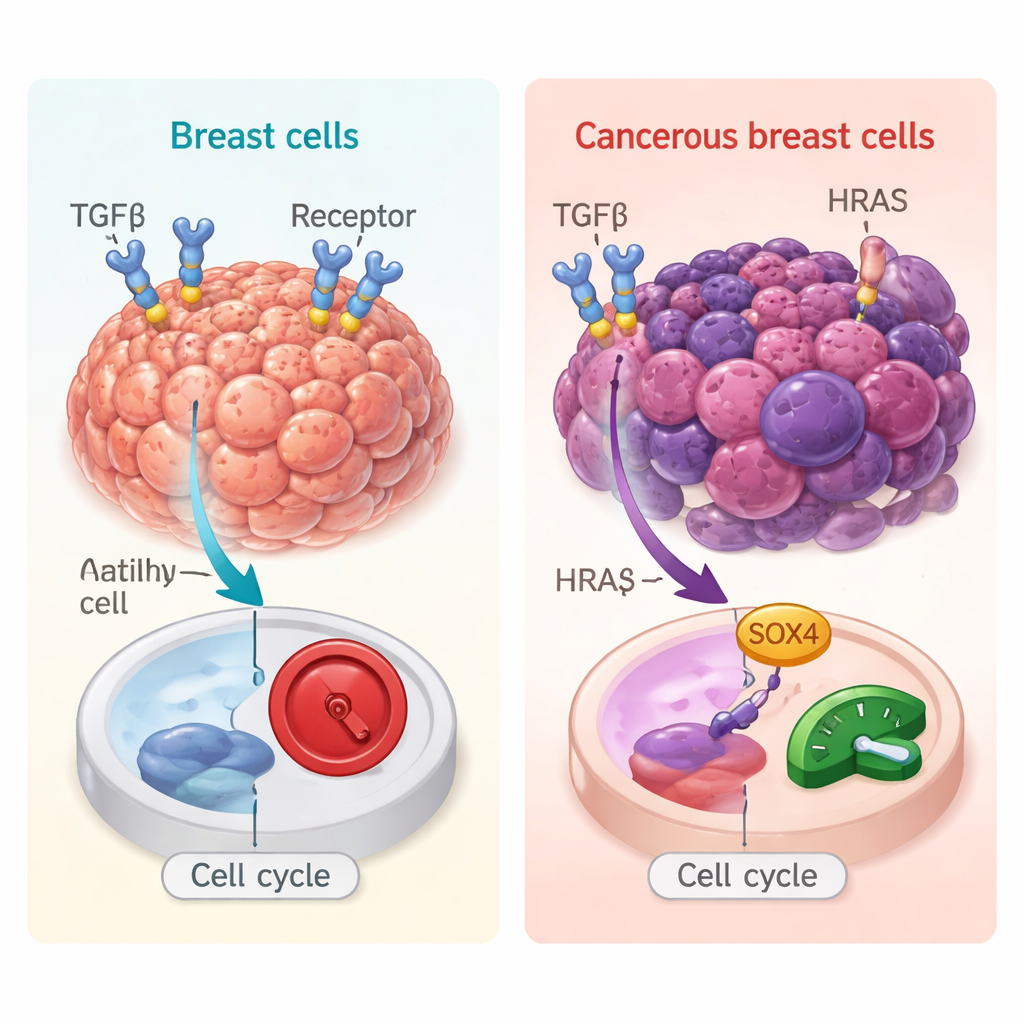
Umschalten der genomischen An-/Aus-Schalter
Das Team untersuchte das Chromatin, die aus DNA und Proteinen bestehende Verpackung, die steuert, welche Gene zugänglich sind und eingeschaltet werden können. Nach Behandlung der 3D-Zellcluster mit TGFβ beobachteten sie eine weitreichende Öffnung des Chromatins an Genstartstellen und entfernten Enhancer-Regionen in sowohl normalartigen als auch HRAS-mutierten Zellen. Das Muster der neu zugänglichen Stellen unterschied sich jedoch deutlich zwischen beiden. In den krebsähnlichen Zellen waren Bindungsstellen für einen Transkriptionsfaktor namens SOX4 besonders angereichert. Gleichzeitig zeigte die Expressionsprofilierung, dass TGFβ nicht mehr nur bekannte Programme wie epithelial-mesenchymale Transition (mit Invasion verknüpft) und Stoffwechselumschichtungen aktiviert; in den HRAS-mutanten Zellen steigerte es außerdem Gene, die an DNA-Replikation, DNA-Reparatur und am Vorankommen durch zentrale Zellzyklus-Kontrollpunkte beteiligt sind.
SOX4 als molekularer Mittelsmann
Bei tiefergehenden Analysen zeigten die Forschenden, dass SOX4 im Zentrum dieses Umschaltens steht. Einzelzell-RNA-Sequenzierungsdaten aus primären Brusttumoren offenbarten, dass SOX4 gemeinsam mit Zellzyklustreibern wie CDK4, CDK6 und Cyclin D1 (CCND1) exprimiert wird, insbesondere in aktiv teilenden Krebszellen. In ihren 3D-Modellen erhöhte TGFβ die SOX4-Spiegel, und SOX4 wurde in der Nähe der Kontrollregionen dieser Zellzyklusgene gefunden, besonders bei CDK4. Wenn SOX4 durch genetische Werkzeuge reduziert wurde, konnte TGFβ viele seiner Zielgene, darunter solche, die mit Zellteilung und Gewebsumbau verbunden sind, nicht mehr effektiv aktivieren, und die krebsähnlichen Sphäroiden wurden weniger invasiv und stabiler. Biochemische Experimente zeigten außerdem, dass SOX4 mit SMAD3—einem zentralen TGFβ-Signalüberträger—zusammenarbeitet und ein kooperatives Modul im Zellkern bildet, das die Genaktivierung verstärkt.
Schwächung eines vordersten Mittels gegen Brustkrebs
Palbociclib ist ein weitverbreitet eingesetztes Medikament, das CDK4 und CDK6 blockiert—Proteine, die Zellen vom Ruhezustand in aktive Teilung treiben. Viele Patientinnen und Patienten entwickeln schließlich eine Resistenz gegen diese Behandlung. Die Autorinnen und Autoren kombinierten große Arzneimittel‑Antwortdatensätze mit Laborversuchen in mehreren Brustkrebszelllinien und 3D-Kulturen. Sie fanden heraus, dass stärkere TGFβ-Aktivität zusammen mit SOX4- und verwandten Gen-Signaturen mit höheren Palbociclib-Dosen assoziiert ist, die benötigt werden, um das Wachstum zu hemmen. Im Labor machte die Zugabe von TGFβ Krebszellen weniger empfindlich gegenüber Palbociclib, während die Blockade der TGFβ-Signalübertragung oder das Herunterregulieren von SOX4 die Empfindlichkeit wiederherstellte. Langzeitexposition gegenüber Palbociclib führte zu resistenten Zelllinien, die verstärkte TGFβ-Signale, mehr SOX4 und stärkere Merkmale aktiven Chromatins am SOX4-Gen selbst zeigten. In Zebrafisch-Modellen reduzierte die Hemmung von TGFβ das Wachstum von Tumoren, die aus Palbociclib-resistenten Zellen hervorgingen, deutlich. 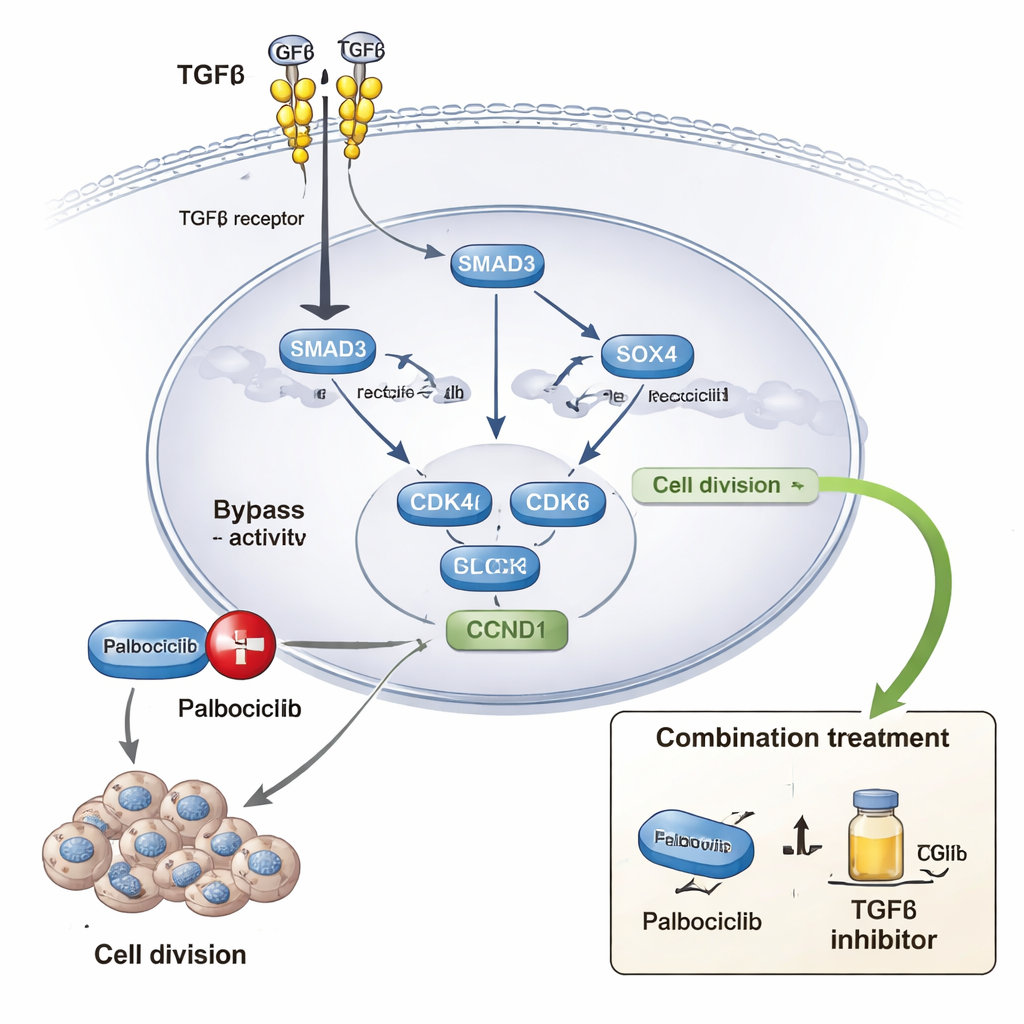
Was das für Patientinnen, Patienten und künftige Therapien bedeutet
Für Nicht-Spezialisten ist die zentrale Botschaft, dass ein Signal, das uns normalerweise vor Krebs schützen soll, im falschen Kontext dazu benutzt werden kann, Tumoren beim Überleben zu helfen und Medikamente zu umgehen. Hier arbeitet TGFβ mit SOX4 zusammen, um entscheidende Bereiche des Genoms zu öffnen, Zellzyklusmotoren wie CDK4 und CDK6 einzuschalten und die Wirkung von Palbociclib abzuschwächen. Die Ergebnisse legen nahe, dass bei einigen Brustkrebsarten die Kombination von CDK4/6-Inhibitoren mit Medikamenten, die TGFβ-Signale blockieren—oder mit Wirkstoffen, die SOX4-gesteuerte Programme anvisieren—Resistenzen verzögern oder überwinden könnte. Obwohl weitere klinische Studien nötig sind, zeichnet diese Studie einen detaillierten molekularen Fluchtweg nach, den Krebszellen nutzen, und weist auf neue Ansatzpunkte hin, ihn abzuschneiden.
Zitation: Ali, M.M., Itoh, Y., Badji, A.M.P. et al. TGFβ signaling promotes cell cycle progression and resistance to the CDK4/6 inhibitor palbociclib through SOX4 transcriptional modulation in breast cancer cells. Cell Death Dis 17, 209 (2026). https://doi.org/10.1038/s41419-026-08435-4
Schlüsselwörter: Brustkrebs, TGF-beta-Signalübertragung, SOX4, Palbociclib-Resistenz, Zellzyklus