Clear Sky Science · de
BCL-xL als therapeutisches Ziel bei cetuximab-refraktärem kolorektalem Krebs
Warum das für Menschen mit Darmkrebs wichtig ist
Kolorektaler (Darm- und Rektum-)Krebs zählt weltweit zu den häufigsten Krebserkrankungen, und viele Patientinnen und Patienten mit fortgeschrittener Erkrankung erhalten ein zielgerichtetes Antikörpermedikament namens Cetuximab. Dieses Medikament kann Tumoren zunächst verkleinern, doch bei den meisten Patientinnen und Patienten findet der Krebs innerhalb weniger Monate Wege, dem Wirkstoff zu entkommen, sodass Ärzten nur wenige gute Optionen bleiben. Die Studie stellt eine drängende Frage: Wenn Darmtumoren nicht mehr auf Cetuximab ansprechen, gibt es dann eine andere Schwachstelle, die neue Medikamente ausnutzen können, um die Krebszellen zum Absterben zu bringen?
Wenn ein zielgerichtetes Medikament nicht mehr wirkt
Cetuximab wirkt, indem es eine Oberflächenantenne auf Krebszellen blockiert, den epidermalen Wachstumsfaktor-Rezeptor (EGFR), der ihr Wachstum antreibt. Das Team erzeugte ein Labor-Modell der Resistenz, indem eine empfindliche kolorektale Krebszelllinie (LIM1215) über sechs Monate hinweg schrittweise mit zunehmenden Cetuximab-Dosen behandelt wurde. Es entstanden zwei unabhängig abgeleitete resistente Zellpopulationen, die auch bei hohen Wirkstoffkonzentrationen weiterwuchsen, sich aber, sobald das Medikament entfernt wurde, genauso gesund und schnell teilten wie die ursprünglichen Zellen. Wichtig ist, dass die resistenten Zellen das Wirkziel noch auf ihrer Oberfläche trugen und Cetuximab weiterhin daran binden konnte, was darauf hindeutet, dass der Tumor den Rezeptor nicht einfach „versteckt“ oder verändert hatte.
Resistente Zellen leiten ihre Wachstumssignale um
Um zu verstehen, wie die Zellen Cetuximab umgingen, untersuchten die Forscher zentrale Wachstumswege innerhalb der Zelle. In den ursprünglichen Zellen dämpfte Cetuximab normalerweise den MAPK-Signalweg, einen wichtigen Motor der Zellteilung. In den resistenten Zellen blieb die MAPK-Aktivität jedoch hoch, selbst wenn EGFR blockiert war, was zeigt, dass das Wachstumssignal vom ursprünglichen Rezeptor entkoppelt worden war. Die Sequenzierung der Zell-RNA offenbarte aktivierende Mutationen in einem anderen RAS-Gen, HRAS, in Subpopulationen der resistenten Zellen, nicht jedoch in den sonst häufigen Kandidaten wie KRAS, NRAS oder BRAF. Versuche, diese umgeleiteten Signale mit einem MEK-Inhibitor (der stromab von RAS wirkt) zu unterdrücken, verringerten das Wachstum nur geringfügig. Das unterstrich die Idee, dass es effektiver sein könnte, statt jeder neuen Mutation hinterherzujagen, die zellulären Lebens‑oder‑Todes‑Mechanismen anzugreifen, die verschiedenen resistenten Klonen gemeinsam sind. 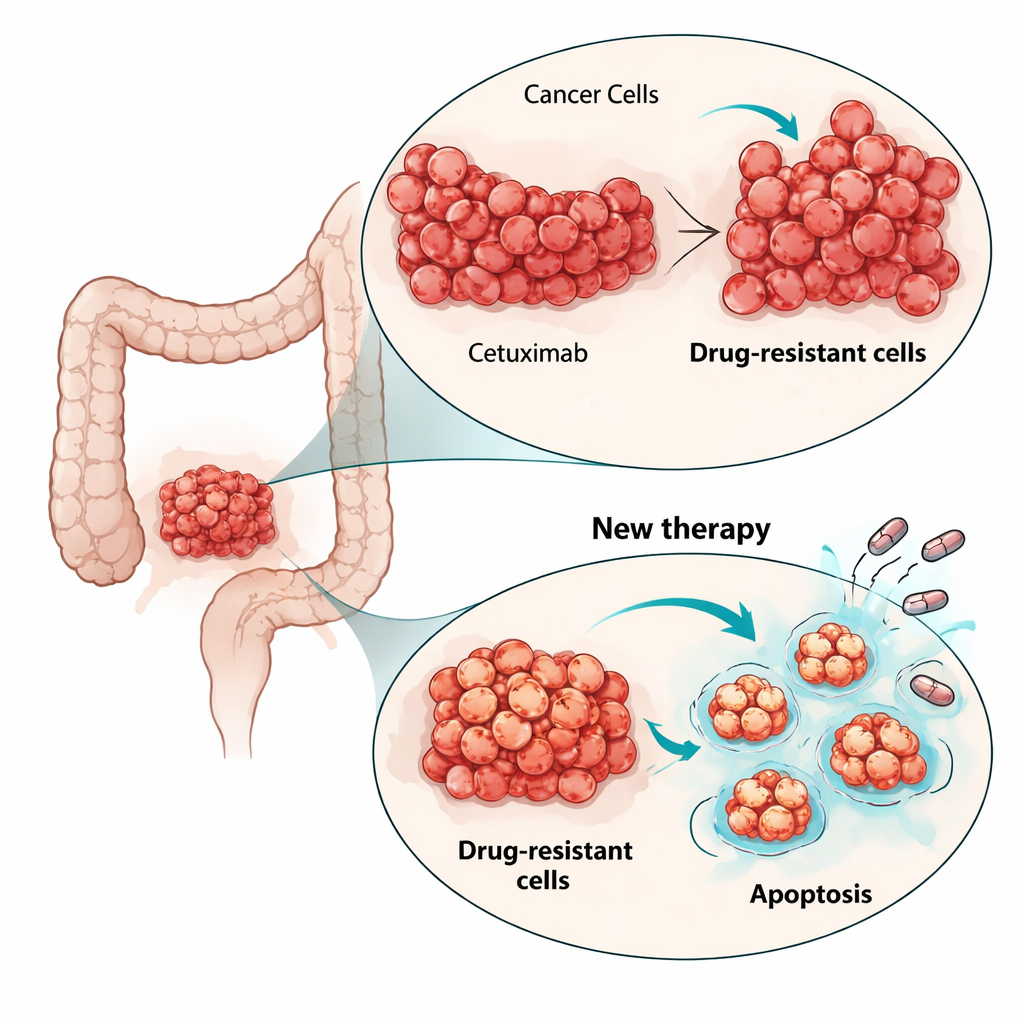
Den Krebs an seiner lebenserhaltenden Einrichtung treffen
Die Wissenschaftler richteten ihren Fokus auf die Apoptose, das eingebaute Selbstmordprogramm der Zelle, das Tumoren oft unterdrücken. Die Genexpressionsanalyse zeigte, dass apoptosebezogene Wege in den resistenten Zellen verändert waren. Insbesondere war das anti‑apoptotische Protein BCL-xL in einer resistenten Population erhöht und in der anderen moderat gesteigert, während ein weiteres Überlebensprotein, MCL-1, ebenfalls vorhanden war. Das Team testete kleine Moleküle, sogenannte BH3‑Mimetika, die diese Überlebensproteine blockieren und das Todesprogramm freisetzen sollen. In zweidimensionalen Zellkulturen waren alle drei Zelllinien – die ursprünglichen und die resistenten – empfindlich gegenüber Wirkstoffen, die BCL-xL oder MCL-1 blockieren, doch auffällig war, dass niedrigere Dosen die cetuximab‑resistenten Zellen wirksamer töteten. Die Zugabe einer niedrigen Dosis des Proteasom‑Inhibitors Bortezomib, der pro‑apoptotische Signale anreichert, verstärkte die Abtötung zusätzlich, insbesondere in Kombination mit dem MCL‑1‑Blocker.
Von flachen Nährböden zu 3D‑Mini‑Tumoren und Patientengewebe
Da zweidimensionale Zellschichten Tumoren im Körper nicht vollständig nachbilden, züchtete das Team die Zellen anschließend als dreidimensionale Sphäroide in einem Gel, was die Architektur und die Herausforderungen der Wirkstoffdurchdringung in echten Tumoren besser widerspiegelt. Auch hier reduzierte die Blockade von BCL-xL oder MCL-1 die Sphäroid‑Vitalität, und die Kombination dieser Wirkstoffe mit Bortezomib führte zu dramatischen Abnahmen der Stoffwechselaktivität und klaren Zeichen von Zelltod. Um zu prüfen, ob diese Verwundbarkeit auch in realistischeren menschlichen Tumormaterialien existiert, nutzten sie dünne Scheiben cetuximab‑resistenter kolorektaler Karzinome, die als patientenabgeleitete Xenografts (in Mäusen gewachsene Tumore) erzeugt wurden. Diese Modelle waren alle KRAS Wildtyp wie die ursprünglichen LIM1215‑Zellen, trugen jedoch verschiedene zusätzliche Mutationen, unter anderem in BRAF und TP53, und spiegelten damit die genetische Vielfalt wider, wie sie klinisch beobachtet wird. 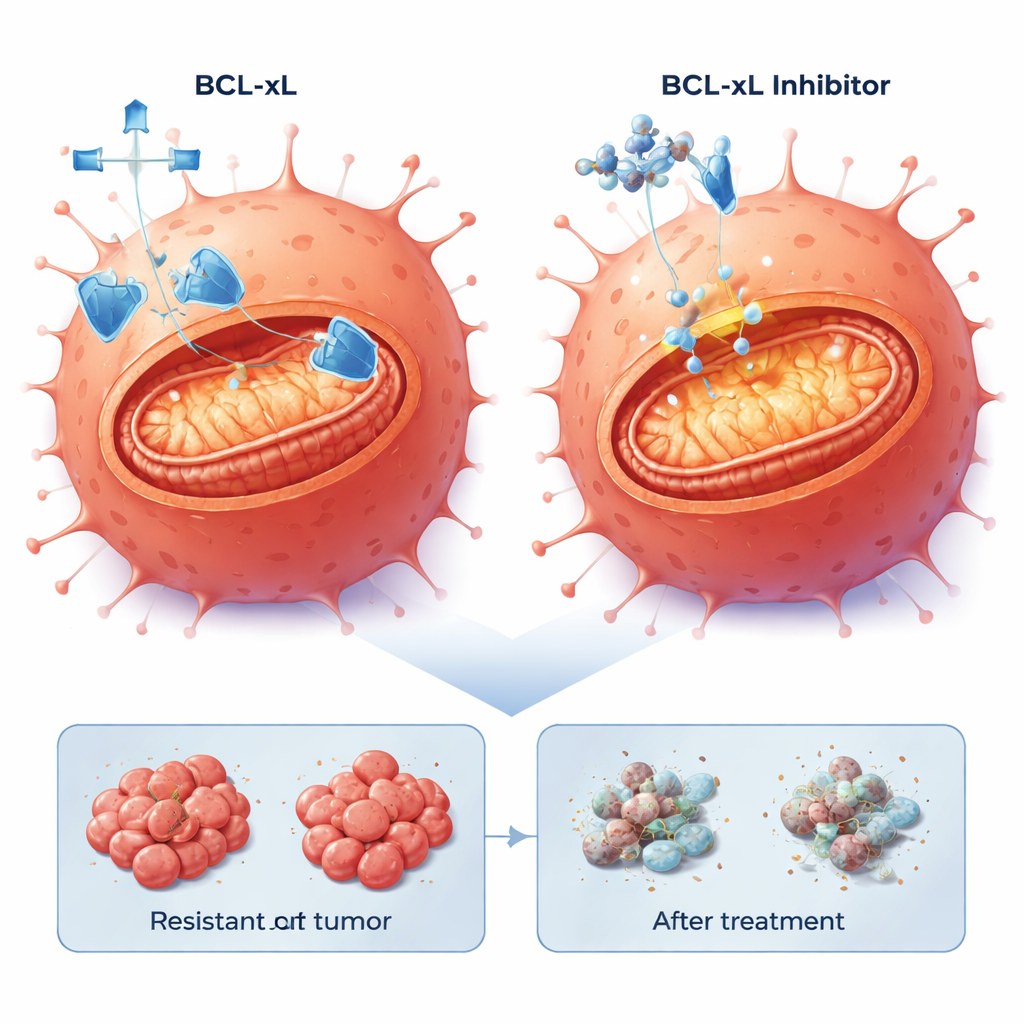
BCL-xL‑Targeting wirkt über unterschiedliche resistente Tumoren hinweg
In diesen patientenabgeleiteten Tumorschnitten löste die Kombination eines BCL‑xL‑Inhibitors mit niedrig dosiertem Bortezomib durchgehend ausgeprägten Zelltod in 20–40 % der Tumorzellen in vier verschiedenen Modellen aus, einschließlich solcher mit aggressiven BRAF‑Mutationen. Im Gegensatz dazu zeigte die Blockade von MCL‑1 mit Bortezomib nur in einer Teilmenge der Tumoren starke Effekte. Wichtig ist, dass die Fähigkeit der resistenten Zellen, Apoptose zu durchlaufen, erhalten blieb: Sobald das BCL‑xL‑„Sicherheitsnetz“ entfernt war, konnte das interne Todesprogramm aktiviert werden, unabhängig von der genauen genetischen Route, über die der Tumor der Cetuximab‑Wirkung entkommen war.
Was das für Patientinnen und Patienten bedeutet
Für Menschen, deren kolorektaler Krebs nicht mehr auf Cetuximab anspricht, bietet die Studie vorsichtigen Optimismus. Sie deutet an, dass viele Krebszellen auch nach Resistenz gegen EGFR‑gerichtete Therapien darauf vorbereitet sind zu sterben, wenn ein zentrales Überlebensprotein, BCL‑xL, blockiert wird. Obwohl BCL‑xL‑Inhibitoren Nebenwirkungen haben können, insbesondere auf Blutplättchen, weist die Arbeit auf kombinatorische und dosisoptimierende Strategien hin, die die Toxizität begrenzen und zugleich eine gemeinsame Achillesferse schwer behandelbarer Tumoren ausnutzen könnten. In Zukunft könnten Wirkstoffe, die BCL‑xL entwaffnen, das Rückgrat neuer Zweitlinienbehandlungen für cetuximab‑refraktären kolorektalen Krebs bilden, weniger abhängig von der sich verändernden Mutationslandschaft des Tumors.
Zitation: Asmanidou, S., Thiel, J., Ekstrom, T.L. et al. BCL-xL as a therapeutic target in cetuximab-refractory colorectal cancer. Cell Death Dis 17, 187 (2026). https://doi.org/10.1038/s41419-026-08434-5
Schlüsselwörter: kolorektales Karzinom, Arzneimittelresistenz, cetuximab, BCL-xL-Hemmung, Apoptose