Clear Sky Science · de
Die Hemmung der Glycerophospholipid-Biosynthese überwindet Chemoresistenz durch SLFN11-Verlust beim Ewing-Sarkom
Warum diese Forschung für Kinderkrebs wichtig ist
Das Ewing-Sarkom ist ein seltener, aber aggressiver Tumor, der überwiegend Kinder und Jugendliche trifft. Viele Patientinnen und Patienten sprechen zunächst gut auf Chemotherapie an, doch bei Rückfällen versagen die verfügbaren Therapien häufig. Diese Studie geht einer zentralen Frage nach: Welche inneren Veränderungen ermöglichen es Ewing-Sarkom-Zellen, chemische Therapien zu überleben — und lassen sich diese Veränderungen in neue, angreifbare Schwachstellen verwandeln?
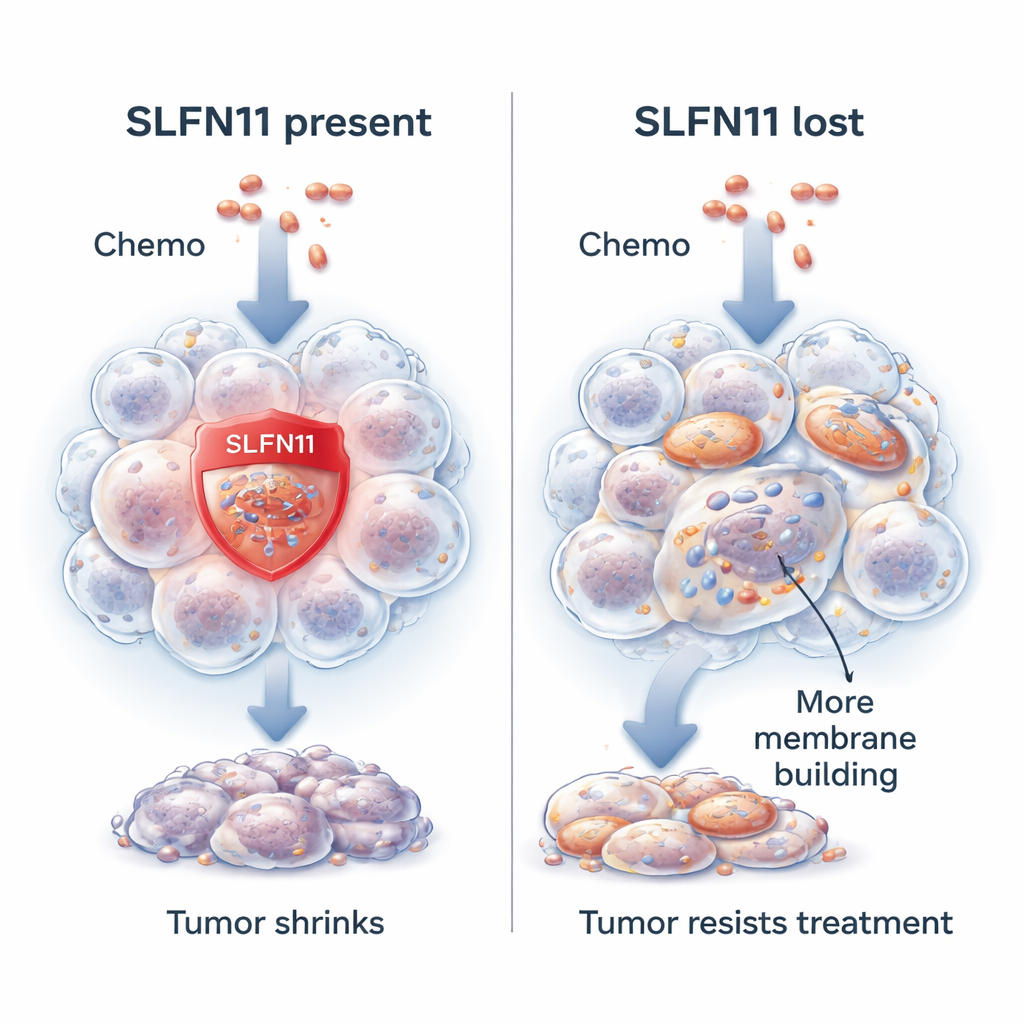
Ein Gen, das Krebszellen leichter zu töten macht
Die Forschenden konzentrieren sich auf ein Gen namens SLFN11. In vielen Ewing-Sarkom-Tumoren ist SLFN11 stark aktiv und macht die Krebszellen deutlich empfindlicher gegenüber DNA-schädigenden Medikamenten, die das genetische Erbgut angreifen. Bei Gabe solcher Wirkstoffe hemmt SLFN11 die DNA-Reparatur und treibt die Krebszelle in Richtung Zelltod. Patientinnen und Patienten mit höheren SLFN11-Spiegeln in ihren Tumoren haben tendenziell bessere Überlebensaussichten und sprechen günstiger auf die Therapie an. Etwa eines von zehn Tumoren weist jedoch von Anfang an wenig oder gar kein SLFN11 auf oder verliert es im Verlauf der Behandlung. In diesen Fällen ist die gleiche Chemotherapie deutlich weniger wirksam, obwohl die Krebszellen weiterhin proliferationsfähig bleiben.
Wie Krebszellen ihren Energie- und Fettstoffwechsel umstellen
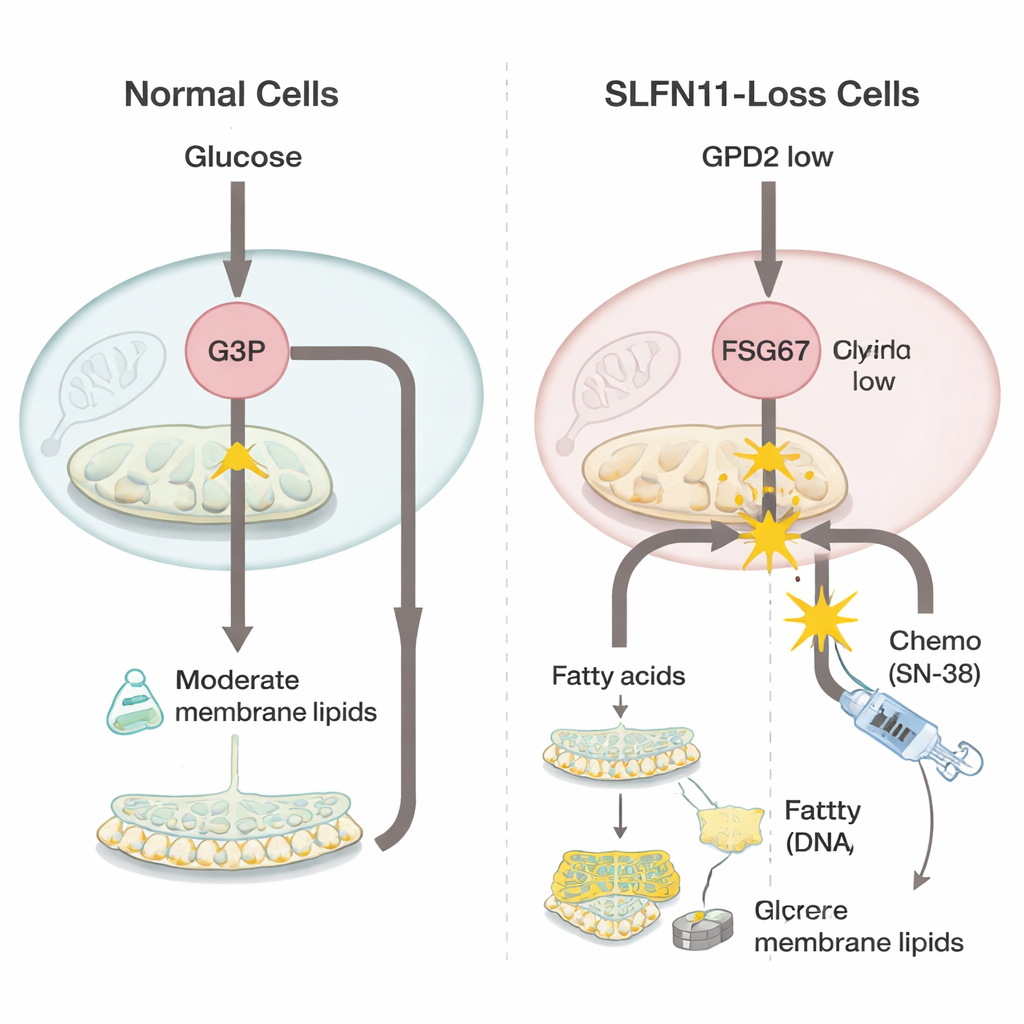
Um zu verstehen, was beim Verlust von SLFN11 passiert, verglichen die Forschenden Ewing-Sarkom-Zellen mit und ohne dieses Gen mittels leistungsfähiger „Omics“-Methoden, die Tausende von Genen und kleinen Molekülen gleichzeitig messen. Sie fanden heraus, dass Zellen ohne SLFN11 ein Enzym in den Mitochondrien namens GPD2 herunterregulieren, das normalerweise beim Abbau von Glycerol-3-phosphat in der Energiegewinnung hilft. Bei vermindertem GPD2 reichert sich Glycerol-3-phosphat an. Statt verschwendet zu werden, wird dieser Baustein vermehrt in die Herstellung von Fettsubstanzen für Zellmembranen umgeleitet — eine Gruppe, die als Glycerophospholipide bekannt ist. Die Zellen zeigten zudem Hinweise auf eine verstärkte Produktion von flexibleren, ungesättigten Fetten, die schnell wachsenden Tumoren helfen können, Stress zu kompensieren.
Aus einem Überlebensmechanismus eine Verwundbarkeit machen
Weil diese SLFN11-defizienten Zellen stärker auf Membranaufbau angewiesen sind, prüften die Forschenden, ob das Blockieren dieses Prozesses die Chemosensitivität wiederherstellen kann. Sie setzten eine Verbindung namens FSG67 ein, die einen Schlüsselbestandteil der Glycerophospholipid-Biosynthese hemmt. Allein war das Standard-DNA-schädigende Medikament SN-38 in SLFN11-defizienten Zellen deutlich weniger wirksam, was das klinische Problem der Resistenz widerspiegelt. In Kombination mit FSG67 wurden die zuvor resistenten Zellen jedoch deutlich stärker getroffen, und die beiden Wirkstoffe wirkten synergistisch stärker als ihre Einzeleffekte erwarten ließen. Dagegen brachte die Zugabe von FSG67 in Zellen, die noch SLFN11 aufwiesen und bereits sehr empfindlich auf SN-38 reagierten, kaum einen zusätzlichen Nutzen und konnte sogar leicht kontraproduktiv sein. Dieses Muster legt nahe, dass die neue Abhängigkeit von Fettsynthese und Membranbildung spezifisch für den resistenten, SLFN11-niedrigen Zustand ist.
Ein potenzieller nichtinvasiver Hinweis auf schwer behandelbare Tumoren
Die Forschenden untersuchten anschließend, ob diese metabolische Umstellung in tatsächlichen Tumoren nachweisbar ist und nicht nur in Zellkulturen. Sie züchteten Ewing-Sarkom-Tumoren mit und ohne SLFN11 in Mäusen und analysierten die chemische Zusammensetzung der Tumorextrakte mittels Kernspinresonanz (NMR). Tumoren ohne SLFN11 zeigten ein höheres Verhältnis zweier cholinhaltiger Moleküle, die mit Membranumsatz verbunden sind: Phosphocholin und Glycerophosphocholin. Ein hohes Phosphocholin/Glycerophosphocholin-Verhältnis wurde in anderen Krebsarten mit aggressiverem Verhalten und schlechterer Therapieansprache in Verbindung gebracht. Da Cholin-Signale mit fortgeschrittenen Bildgebungsverfahren messbar sind, könnte eine solche Verschiebung künftig als nichtinvasiver Marker dienen, um Ewing-Sarkom-Tumoren zu identifizieren, die diesen resistenten, membranaufbauenden Stoffwechselzustand angenommen haben.
Was das für künftige Behandlungen bedeuten könnte
Insgesamt zeigt die Studie, dass Ewing-Sarkom-Zellen beim Verlust von SLFN11 und eingeschränkter Empfindlichkeit gegenüber DNA-schädigender Chemotherapie ihren Stoffwechsel hin zur verstärkten Produktion von Membranfetten umstellen. Diese Umstellung hilft nicht nur dem Überleben der Zellen, sondern schafft auch eine neue Achillesferse. Die Blockade der Glycerophospholipid-Biosynthese mit einem Wirkstoff wie FSG67 kann die Wirksamkeit der Chemotherapie in diesen resistenten Zellen teilweise wiederherstellen. Obwohl FSG67 selbst noch kein klinisch zugelassenes Medikament ist, weist die Arbeit auf eine Strategie hin, bei der Tumoren künftig nach SLFN11-Status und metabolischen Merkmalen charakterisiert werden könnten, um DNA-schädigende Therapien mit gezielten Hemmstoffen der Fett- und Membransynthese zu kombinieren und so Resistenzen zu überwinden.
Zitation: Chakraborty, K., Burman, R., Satheesh, S. et al. Targeting glycerophospholipid biosynthesis overcomes chemoresistance driven by SLFN11 loss in Ewing sarcoma. Cell Death Dis 17, 190 (2026). https://doi.org/10.1038/s41419-026-08432-7
Schlüsselwörter: Ewing-Sarkom, Chemoresistenz, SLFN11, Krebsstoffwechsel, Lipidbiosynthese