Clear Sky Science · de
Modulation von Immunzellen und metabolische Umlenkung bei der Efferocytose
Wie unser Körper stillschweigend sterbende Zellen beseitigt
Jeden Tag gehen Milliarden unserer Zellen zu Ende. Dennoch merken wir diesen mikroskopischen Austausch nicht und werden nicht krank durch die Überreste. Diese stille Hausarbeit übernehmen Immun- und Gewebezellen, die sterbende Zellen erkennen und verschlingen und so schädliche Entzündungen verhindern. Die rezensierte Forschung erklärt, wie dieser Aufräumprozess, Efferocytose genannt, nicht nur Gewebe sauber hält, sondern auch den Stoffwechsel der aufräumenden Zellen umprogrammiert und damit beeinflusst, ob unser Immunsystem sich beruhigt, Infektionen bekämpft oder — wenn etwas schiefgeht — zur Krankheitsentstehung beiträgt.
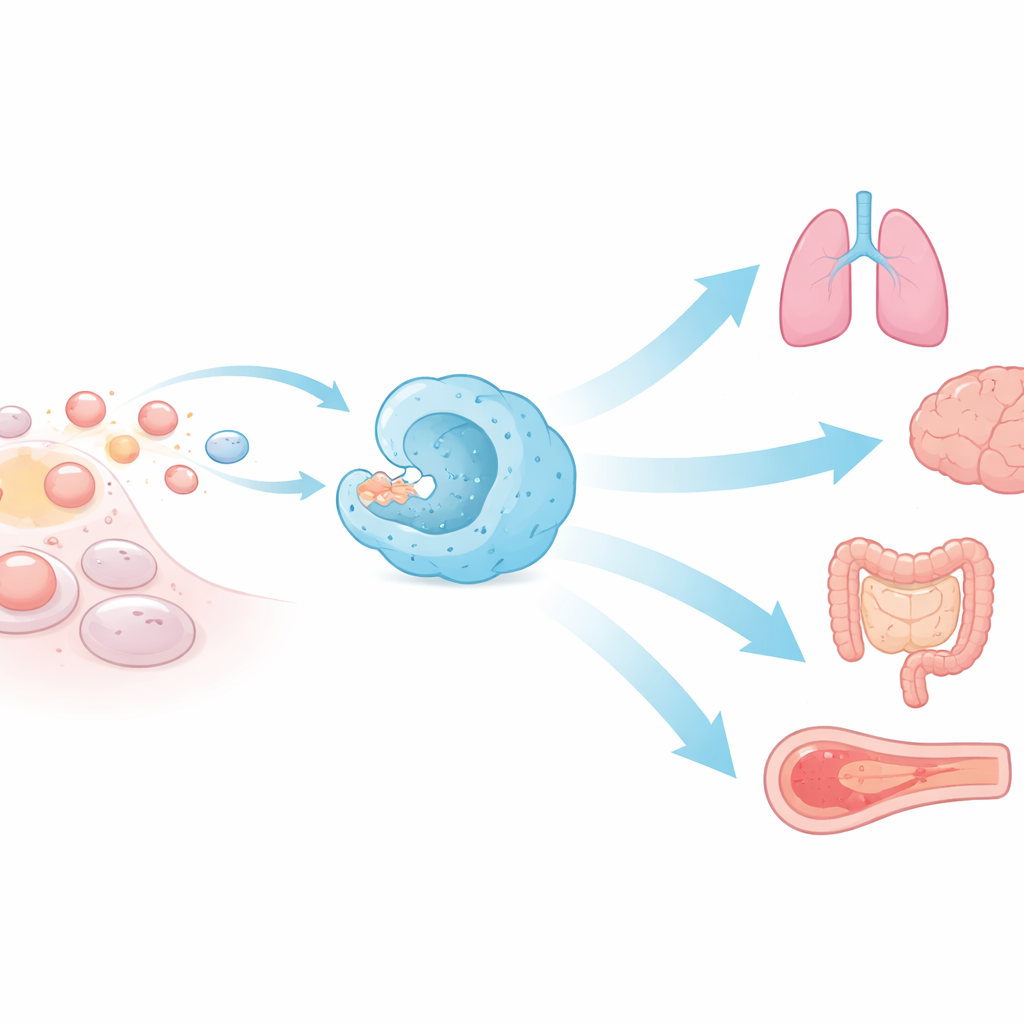
Die stillen Müllsammler des Körpers
Efferocytose bezeichnet das Umschließen und Entfernen apoptotischer, also programmierter sterbender Zellen. Spezialisierte Immunzellen wie Makrophagen und dendritische Zellen leisten den Großteil dieser Arbeit, doch viele Nicht‑Immunzellen — etwa Epithelzellen im Darm, in der Lunge, im Auge und im Hoden — können ebenfalls eingreifen. Sterbende Zellen senden chemische „Find‑me“-Signale aus, die nahegelegene Räuberzellen anziehen, zeigen dann „Eat‑me“-Marker auf ihrer Oberfläche und schalten gleichzeitig „Don’t‑eat‑me“-Signale ab. Nach der Erkennung werden sie in eine membranumhüllte Tasche eingebettet, ins Innere gezogen und in enzymgefüllten Kompartimenten abgebaut. Diese schnelle, mehrstufige Choreographie erklärt, warum apoptotische Zellen trotz massiven täglichen Zellverlusts selten unter dem Mikroskop zu sehen sind.
Haushalt, der Organe schützt
Effiziente Efferocytose schützt Struktur und Funktion vieler Organe. Im Auge führt das Versagen, abgestorbene Fragmente von Photorezeptoren zu entfernen, zu Sehverlust. Im Hoden kann unzureichende Beseitigung sterbender Keimzellen Unfruchtbarkeit verursachen. Während der Schwangerschaft fördert die Efferocytose von Plazentazellen die mütterliche Toleranz, indem sie entzündliche Moleküle dämpft und beruhigende Signale verstärkt. Im Gehirn beschneiden Mikroglia überschüssige Neurone und unterstützen eine gesunde Verschaltung, während im Darm Paneth‑Zellen und andere Phagozyten sterbende Zellen beseitigen, um chronische Darmentzündungen zu verhindern. In der Lunge entfernen Atemwegsmakrophagen kontinuierlich tote Zellen und verhindern so die Freisetzung von Gefahrensignalen, die Asthma, chronisch obstruktive Lungenerkrankung oder schwere virale Schäden antreiben können.
Wenn Infektionen das Aufräumen zur zweischneidigen Klinge machen
Bei Infektionen wird Efferocytose komplexer. Krankheitserreger lösen häufig Zelltod aus, und das anschließende Verschlingen infizierter Leichen kann die Wirtsabwehr entweder schwächen oder stärken. Manche Viren und Bakterien nutzen die entzündungsdämpfende Seite der Efferocytose aus, um sich der Immunabwehr zu entziehen oder sich zu verbreiten, wobei die aufgenommenen Vesikel als „Trojanische Pferde“ dienen. In anderen Fällen liefert das Verschlingen infizierter toter Zellen mikrobielle Fragmente in Makrophagen und dendritische Zellen, die diese dann T‑Zellen präsentieren und so schützende Immunantworten auslösen. Abhängig vom Erreger und Gewebe kann Efferocytose T‑Helferzellen in verschiedene Immunprofile lenken, die entweder die bakterielle Beseitigung unterstützen oder — wenn Selbstmoleküle zusammen mit mikrobiellen Anteilen präsentiert werden — die Entstehung autoreaktiver T‑Zellen begünstigen, die eigenes Gewebe angreifen.
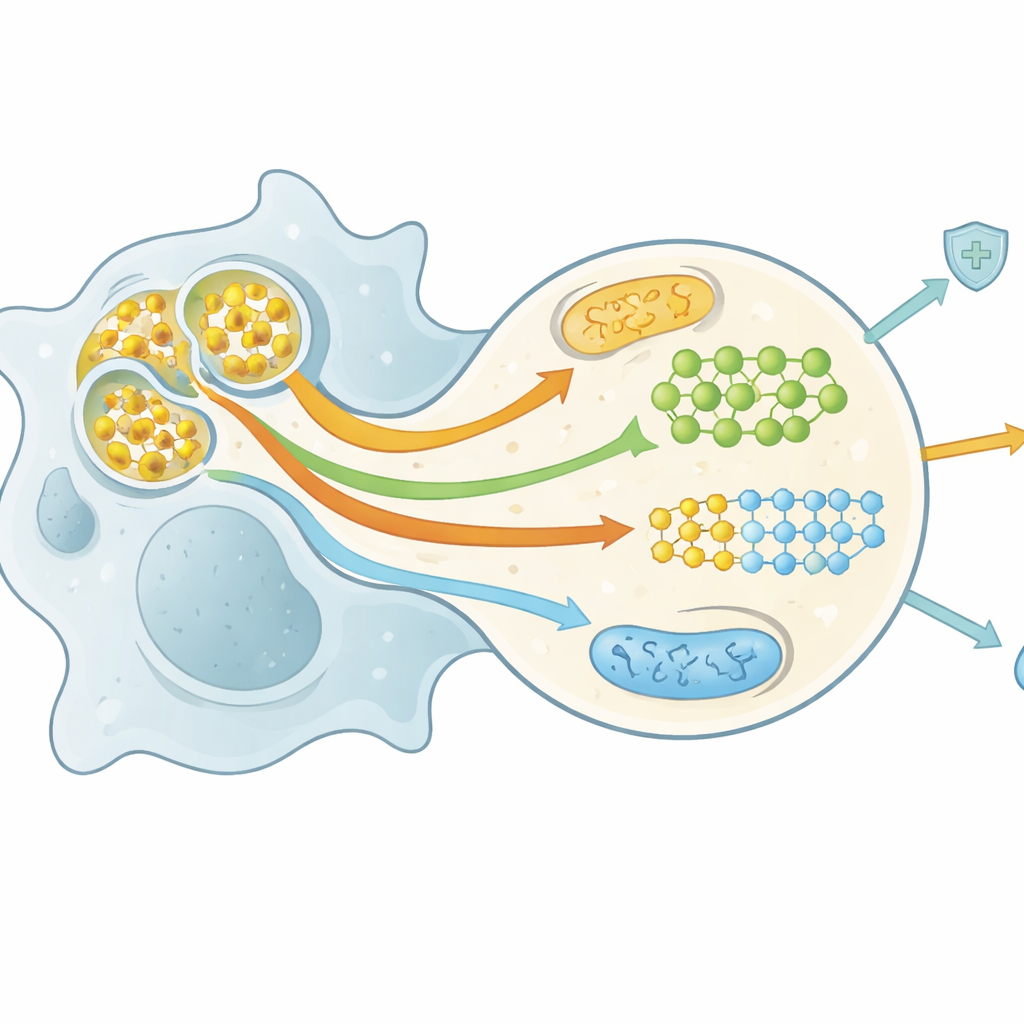
Währung der Gefallenen: wie der Stoffwechsel umprogrammiert wird
Den Abbau einer ganzen Zelle zu leisten ist metabolisch anspruchsvoll, bringt aber zugleich eine Flut an Nährstoffen für die Räuberzelle — Lipide, Zucker, Aminosäuren und Nukleotide. Die Autorinnen und Autoren beschreiben ein wachsendes Forschungsfeld, manchmal als Efferotomie bezeichnet, das nachverfolgt, wie dieser Nährstoffansturm den Stoffwechsel von Makrophagen und dendritischen Zellen umprogrammiert. Lipide aus toten Zellen aktivieren nukleare Rezeptoren, die den Cholesterinexport steigern, die mitochondriale Fettverbrennung unterstützen und einen entzündungshemmenden, gewebereparierenden Zustand fördern. Aminosäuren wie Arginin, Methionin und Tryptophan werden recycelt zu Molekülen, die wiederholte Aufnahmezyklen antreiben und pro‑resolvierende Signale auslösen. Kurzfristige Glukoseabbauphasen und verwandte Stoffwechselwege liefern Energie, erhalten das Redox‑Gleichgewicht und helfen, Rezeptoren und Membranen in dem Zustand zu halten, der kontinuierliches Aufräumen ermöglicht. Diese verflochtenen metabolischen Veränderungen bestimmen, ob efferocytische Zellen tolerant bleiben, in den Reparaturmodus wechseln oder starke antimikrobielle Aktivität beibehalten.
Offene Fragen und künftige Behandlungswege
Das Review betont, dass nicht alle Efferocyten, also Zellfresser, gleich agieren. Professionelle Immunzellen und Gewebezellen können auf unterschiedliche Stoffwechselprogramme angewiesen sein, und verschiedene Formen des Zelltods — etwa Nekrose oder Ferroptose — hinterlassen wahrscheinlich unterschiedliche metabolische und immunologische Spuren. Zentrale Unbekannte sind, wie gemischte Signale aus Selbst‑ und mikrobiellen Komponenten innerhalb derselben toten Zelle Energiewege und langfristige Immunantworten formen. Indem Forscher diese Verknüpfungen zwischen Aufräumen, Metabolismus und immunologischem Schicksal kartieren, hoffen sie, Therapien zu entwerfen, die Efferocytose behutsam lenken: sie zu verstärken, um chronische Entzündungen zu beenden und die Wundheilung zu unterstützen, oder sie so zu justieren, dass antimikrobielle Stärke erhalten bleibt, ohne in Autoimmunität umzuschlagen. Im Kern könnte das Verständnis, wie der Körper von seinen eigenen zellulären Überresten zehrt, neue Wege eröffnen, Entzündung, Infektion und Toleranz im gesunden Gleichgewicht zu halten.
Zitation: Oliveira, K.C., Marcos, C.M., Penteado, L.d.A. et al. Modulation of immune cells and metabolic reprogramming in efferocytosis. Cell Death Dis 17, 257 (2026). https://doi.org/10.1038/s41419-026-08431-8
Schlüsselwörter: Efferocytose, Immuntoleranz, angeborene Immunität, Immunmetabolismus, chronische Entzündung