Clear Sky Science · de
Gezielte Blockade hypoxischer exosomaler IGFBP2 überwindet CD47-vermittelte Immunflucht bei Glioblastom
Warum Tumoren durch Sauerstoffentzug paradox reagieren können
Ärztinnen und Ärzte wissen seit langem, dass das tödliche Hirnkrebs Glioblastom häufig in sauerstoffarmen Bereichen wächst. Diese hypoxischen Nischen machen den Tumor schwerer behandelbar. Die vorliegende Studie zeigt, wie niedriger Sauerstoffgehalt Krebszellen dabei unterstützt, sich vor dem Immunsystem zu verbergen, und schlägt eine neue Kombinationsbehandlung vor, die sie für den Körper leichter angreifbar machen könnte.
Ein tödlicher Hirntumor, der unseren Abwehrkräften ausweicht
Das Glioblastom ist der aggressivste häufige Hirntumor bei Erwachsenen; das Überleben bemisst sich typischerweise in Monaten. Obwohl Immunzellen diese Tumoren durchdringen, entkommen Krebszellen häufig der Zerstörung. Ein wichtiger Fluchtmechanismus ist ein Oberflächenprotein namens CD47, das manchmal als „fress mich nicht“-Signal bezeichnet wird und benachrichtigten Immunzellen wie Makrophagen signalisiert, die Tumorzelle nicht aufzunehmen und zu zerstören. Wirkstoffe, die CD47 blockieren, werden bereits getestet, doch die Resultate bei soliden Tumoren wie dem Glioblastom sind gemischt, was darauf hindeutet, dass andere Faktoren im Tumormikromilieu diese Therapien unterlaufen könnten.
Hypoxische Zonen und winzige Krebspakete
Mithilfe von Einzelzell-RNA-Sequenzierung kartierten die Forschenden Tausende von Zellen aus verschiedenen Regionen von Glioblastomproben und verglichen den sauerstoffarmen Tumorkern mit dem äußeren Rand. Sie identifizierten einen besonders aggressiven Zelltyp im hypoxischen Kern, genannt mesenchymal-ähnliche GBM-Zellen, der stark CD47 und ein Protein namens IGFBP2 exprimierte. Gleichzeitig entdeckten sie, dass diese Kernzellen große Mengen nanoskopischer Vesikel, sogenannte Exosomen, freisetzten, die IGFBP2 auf ihrer Oberfläche trugen. Da Exosomen durch das Gehirn und sogar in den Blutkreislauf reisen können, verbreiten sie Signale weit über ihren Entstehungsort hinaus. 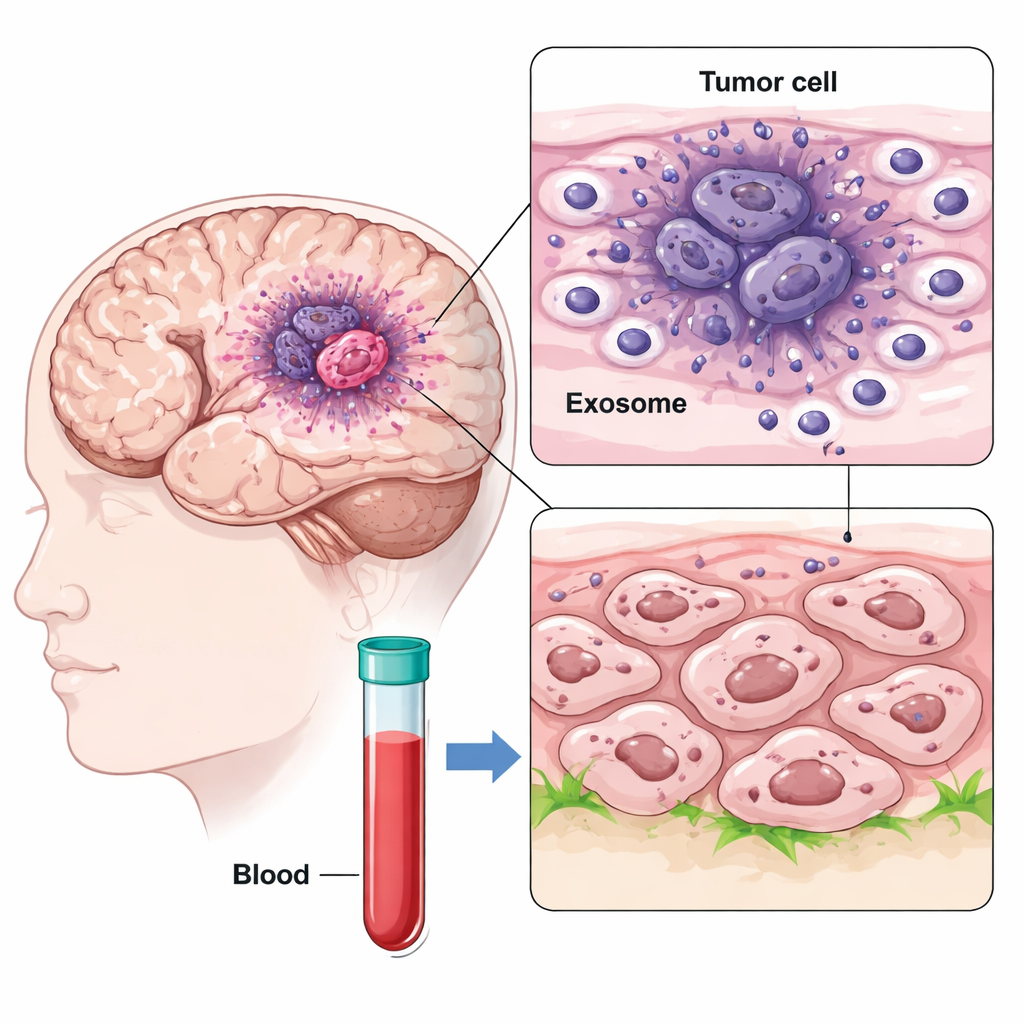
Wie ein Partnerprotein das „fress mich nicht“-Signal verstärkt
Das Team untersuchte anschließend die Funktion von IGFBP2. Sie zeigten, dass unter niedrigem Sauerstoff ein Hypoxie-Sensorprotein namens HIF-2α das IGFBP2-Gen in Tumorzellen einschaltet. IGFBP2 bindet dann an spezifische Rezeptoren, sogenannte Integrine, auf der Oberfläche von Exosomen und schmückt deren Außenmembran. Wenn diese IGFBP2-beschichteten Exosomen mit anderen Tumorzellen verschmelzen, aktivieren sie eine Signalkaskade im Inneren der Zelle, an der Proteine wie FAK und STAT3 beteiligt sind. Diese Kaskade erhöht letztlich die Menge an CD47 auf der Tumorzelloberfläche, verstärkt die „fress mich nicht“-Botschaft an Makrophagen und schützt die Krebszellen weiter vor Immunangriffen. 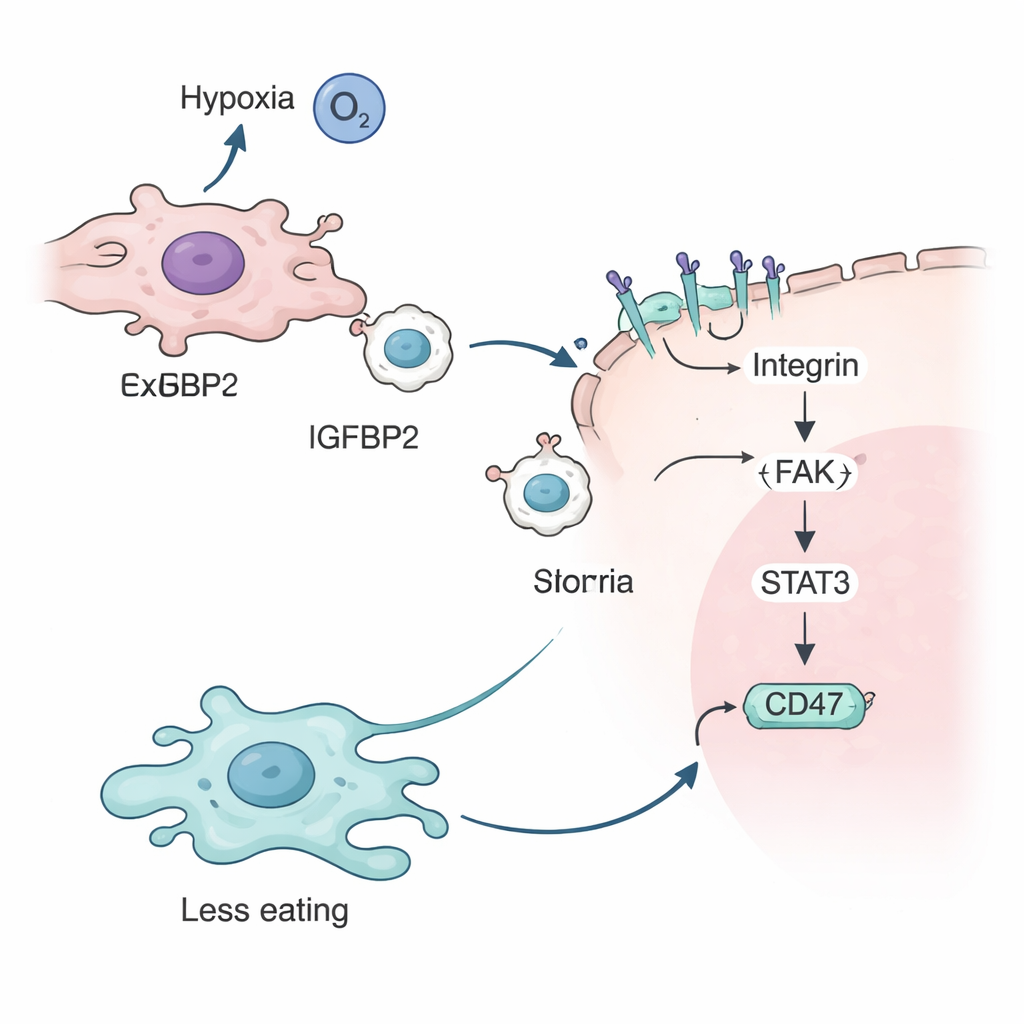
Belege aus Patientenproben und Tiermodellen
Um die Laborbefunde mit der klinischen Realität zu verbinden, untersuchten die Forschenden Tumorgewebe und Blut von Menschen mit Gliom. Sie fanden höhere IGFBP2-Spiegel sowohl in Tumoren als auch in Blutexosomen von Patientinnen und Patienten mit fortgeschrittenerem Krankheitsstadium, was darauf hindeutet, dass IGFBP2-positive Exosomen als blutbasierter Marker für das Tumorstadium dienen könnten. In Mausmodellen machte die Verringerung von IGFBP2 in Glioblastomzellen diese anfälliger dafür, von Makrophagen aufgenommen zu werden, verlangsamte das Tumorwachstum und verlängerte das Überleben. Umgekehrt führten zusätzliche IGFBP2-reiche Exosomen zu erhöhten CD47-Werten, reduzierter Phagozytose durch Immunzellen und beschleunigtem Tumorfortschritt.
Ein vielversprechender Doppelangriff für die Therapie
Schließlich testete das Team, ob die Blockade von IGFBP2 die CD47-zielgerichtete Therapie effektiver machen könnte. Bei Mäusen mit Hirntumoren führte die Behandlung mit Antikörpern gegen sowohl IGFBP2 als auch CD47 zu stärkerer Makrophagenaktivität, kleineren Tumoren und längerem Überleben als jede Einzelsubstanz allein. Indem das hypoxiegetriebene IGFBP2-Signal abgeschnitten und gleichzeitig das CD47-„fress mich nicht“-Signal direkt blockiert wurde, griff diese Kombinationstherapie die Immunverkleidung des Tumors von zwei Seiten an. Für Patientinnen und Patienten deuten diese Ergebnisse darauf hin, dass die Messung von IGFBP2 in Blutexosomen helfen könnte, diejenigen zu identifizieren, die am ehesten von CD47-basierter Immuntherapie profitieren, und dass die Kombination von IGFBP2- und CD47-Inhibitoren eine wirkungsvollere Strategie gegen das Glioblastom sein könnte als eines der beiden Mittel allein.
Zitation: Qi, Y., Zhao, R., Zhang, X. et al. Targeting hypoxic exosomal IGFBP2 overcomes CD47-mediated immune evasion in glioblastoma. Cell Death Dis 17, 192 (2026). https://doi.org/10.1038/s41419-026-08430-9
Schlüsselwörter: glioblastom, Exosomen, Immunflucht, CD47, Hypoxie