Clear Sky Science · de
HSPA5 fördert die Stabilität von YAP/TAZ unabhängig vom Hippo‑Signalweg und löst in Glioblastomen einen proneural‑zu‑mesenchymalen Übergang aus
Warum diese Studie zu Hirntumoren wichtig ist
Glioblastom gehört zu den tödlichsten Hirntumoren, teilweise weil sich viele Tumoren im Verlauf in einen widerstandsfähigeren, therapieresistenteren Zustand verwandeln. Diese Studie zeigt, wie ein verbreitetes Stress‑Antwort‑Protein, HSPA5, diesen Wechsel fördert und tumorfördernde Moleküle länger am Leben erhält, als sie es normalerweise wären. Das Verständnis dieses „Überlebenstricks“ eröffnet neue Ansätze, Glioblastome weniger aggressiv und besser auf bestehende Therapien ansprechbar zu machen.
Ein Tumor, der seine Persönlichkeit ändert
Mediziner und Forscher erkennen zunehmend, dass das Glioblastom keine einheitliche Erkrankung ist, sondern eine Mischung molekularer Subtypen. Zwei Hauptausprägungen sind die „proneurale“ Form, die tendenziell etwas weniger aggressiv ist, und die „mesenchymale“ Form, die stärker invasiv, therapieresistent und mit früherem Rückfall verbunden ist. Tumoren können sich vom proneuralen in den mesenchymalen Zustand entwickeln, ein Prozess, den die Autoren als proneural‑zu‑mesenchymalen Übergang (PMT) bezeichnen. Das Team wollte herausfinden, welche Stress‑Antwort‑Proteine Tumoren auf diesen gefährlichen Pfad treiben könnten.
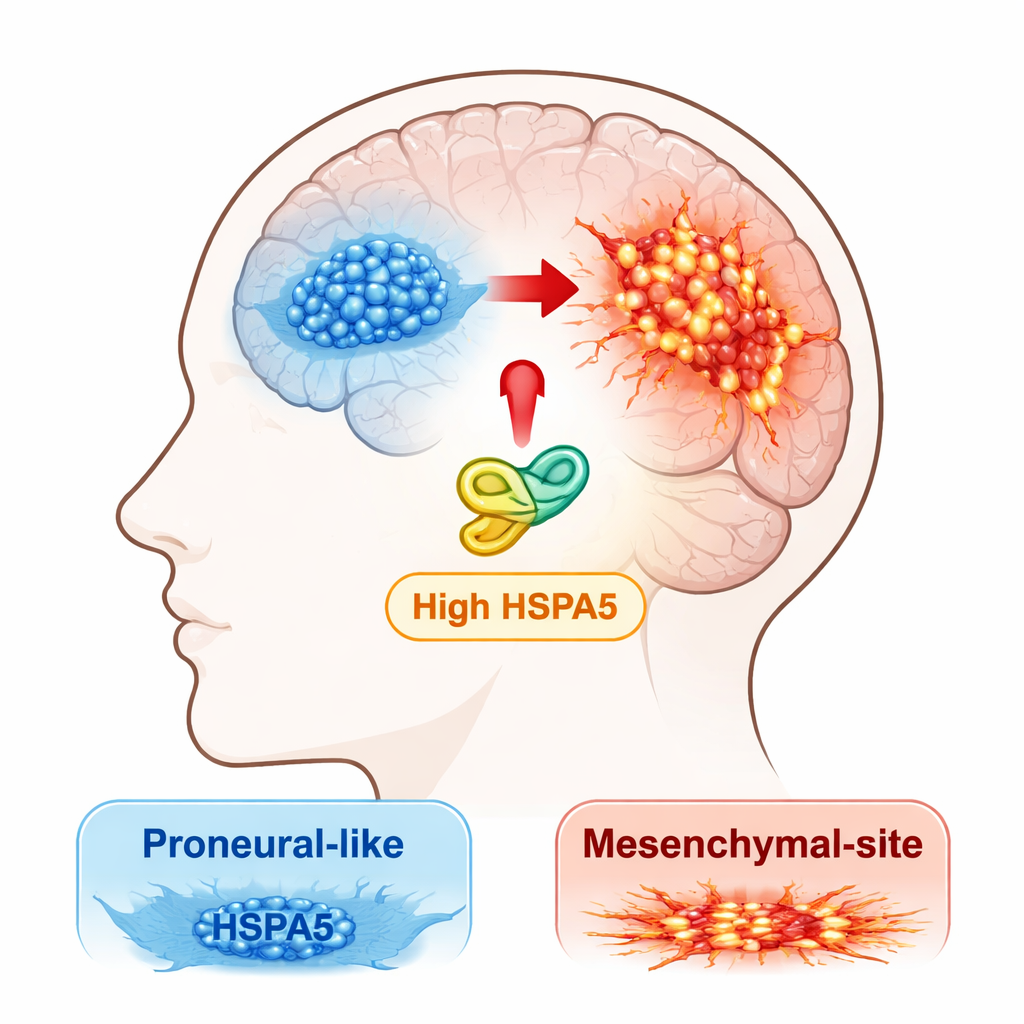
Ein Stress‑Helferprotein im Rampenlicht
Die Forscher begannen damit, große öffentliche Krebsdatensätze und eigene Patientenproben nach Mitgliedern der HSP70‑Familie zu durchsuchen — einer Gruppe von „Chaperon“‑Proteinen, die anderen Proteinen beim Falten und Überleben unter Stress helfen. Ein Chaperon stach hervor: HSPA5. Seine Aktivität war im mesenchymalen Subtyp des Glioblastoms am höchsten und deutlich höher in Tumoren als im normalen Hirngewebe. Patienten mit Tumoren, die mehr HSPA5 zeigten, hatten tendenziell eine schlechtere Gesamtüberlebenszeit, was HSPA5 als möglichen Treiber aggressiver Erkrankung statt als passiven Begleiter hervorhebt.
Zellen zur Aggressivität zwingen
Um zu untersuchen, was HSPA5 tatsächlich in Tumorzellen bewirkt, züchtete das Team primäre Glioblastomzellen direkt aus Patientenproben und teilte sie in proneurale‑ähnliche und mesenchymal‑ähnliche Gruppen. Wenn sie proneurale Zellen dazu zwangen, zusätzliches HSPA5 zu produzieren, begannen diese Zellen, sich mesenchymaler zu verhalten: Sie teilten sich schneller, wanderten und invasierten stärker und schalteten mesenchymale Marker wie CD44 und c‑MET ein, während proneurale Marker wie SOX2 und OLIG2 herunterreguliert wurden. Umgekehrt schwächte das Reduzieren von HSPA5 in mesenchymalen Zellen deren Wachstum und Invasivität ab und drückte sie teilweise zurück in ein weniger aggressives Profil.
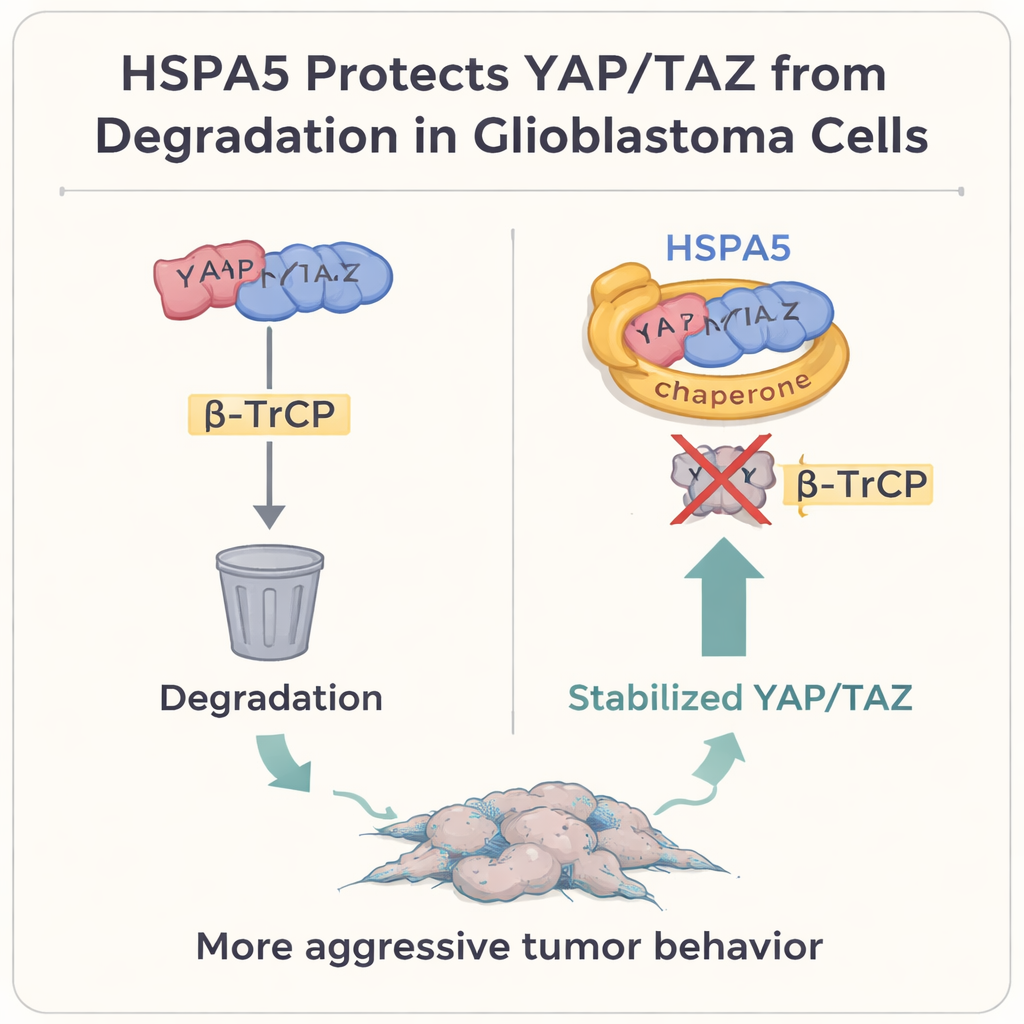
Schutz wichtiger Wachstums‑Schalter vor der zellulären Mülltonne
Tiefergehend fokussierten die Autoren auf zwei starke Wachstumsregulatoren, YAP und TAZ, die im Zentrum des Hippo‑Signalwegs stehen. In vielen soliden Tumoren, einschließlich Glioblastom, wirken diese Proteine als Hauptschalter, die Zellwachstum, Plastizität und den mesenchymalen Zustand fördern. Normalerweise markieren Zellen YAP und TAZ zur Zerstörung durch ein Protein namens β‑TrCP, das sie zur zellulären „Mülltonne“, dem Proteasom, bringt. Die Studie zeigt, dass HSPA5 physisch an YAP und TAZ bindet und dabei seine Substrat‑Bindedomäne wie einen schützenden Handschuh einsetzt. Dadurch blockiert es die Anheftung von β‑TrCP, verhindert die Ubiquitinierung und den Abbau von YAP/TAZ und lässt sie sich im Zellkern anreichern, wo sie mesenchymale Gene einschließlich CD44 und c‑MET aktivieren.
Von Kulturschalen und Mäusen bis zu Patiententumoren
Das Team bestätigte diesen Mechanismus auf mehreren Ebenen. Das Blockieren von HSPA5 ließ YAP‑ und TAZ‑Proteine schneller verschwinden, es sei denn, das Proteasom war chemisch gehemmt, und erhöhte die „Müll‑Markierungs“‑Signale auf ihnen. Die Reaktivierung von YAP und TAZ rettete das Wachstums‑ und Invasionsdefizit, das durch HSPA5‑Reduktion entstanden war, während das Stilllegen von YAP/TAZ die tumorfördernden Effekte einer HSPA5‑Überexpression auslöschte. In Mausmodellen, in denen menschliche Glioblastomzellen ins Gehirn implantiert wurden, wuchsen Tumoren mit hohem HSPA5 schneller und führten schneller zum Tod der Tiere; das Herunterregeln von HSPA5 oder das Unterbrechen seiner Unterstützung für YAP/TAZ verlangsamte das Wachstum und verlängerte das Überleben. Schließlich zeigten in gepaarten menschlichen Proben, die von denselben Patienten vor und nach Rezidiv entnommen wurden, die rezidivierten, stärker mesenchymalen Tumoren höhere Spiegel von HSPA5, YAP, TAZ und mesenchymalen Markern als die ursprünglichen proneural‑ähnlichen Tumoren.
Was das für die zukünftige Behandlung von Hirntumoren bedeutet
Kurz gesagt legt diese Arbeit nahe, dass Glioblastomzellen ein Stress‑Hilfsprotein, HSPA5, ausnutzen, um entscheidende Wachstums‑Schalter (YAP und TAZ) vor dem Abbau zu schützen. Dieser Schutz hilft Tumoren, in einen aggressiveren, therapieresistenteren Zustand zu wechseln und ihn aufrechtzuerhalten. Da es bereits kleinmolekulare Inhibitoren von HSPA5 gibt und Tumorzellen möglicherweise stärker von diesem Chaperon abhängig sind als normale Zellen, bietet die HSPA5–YAP/TAZ‑Achse ein attraktives neues Angriffsziel. Therapien, die diesen Schutzschirm schwächen, könnten Glioblastomzellen weniger anpassungsfähig, weniger invasiv und anfälliger für Standardbehandlungen wie Chemotherapie und Strahlentherapie machen.
Zitation: Gui, S., Yu, W., Song, Z. et al. HSPA5 promotes YAP/TAZ stability independently of the Hippo pathway and induces proneural-to-mesenchymal transition in glioblastoma. Cell Death Dis 17, 208 (2026). https://doi.org/10.1038/s41419-026-08428-3
Schlüsselwörter: Glioblastom, HSPA5, YAP/TAZ, Tumor‑Plastizität, mesenchymaler Übergang