Clear Sky Science · de
Verlust von MLKL bremst die Entwicklung des abdominellen Aortenaneurysmas durch Abschwächung der Nekroptose glatter Muskelzellen
Warum das für Ihr Herz und Ihre Arterien wichtig ist
Abdominelle Aortenaneurysmen sind stille Ausbuchtungen in der Hauptschlagader, die plötzlich aufreißen und tödlich sein können. Bisher bietet die einzige verlässliche Schutzmaßnahme eine Operation, sobald das Gefäß bereits gefährlich erweitert ist. Diese Studie verfolgt einen ganz anderen Ansatz: Statt abzuwarten, bis die Arterie versagt, lässt sich die Gefäßwand vielleicht schützen, indem man eine bestimmte, hochentzündliche Form des Zelltods in ihrer Muskelschicht verhindert?
Wenn eine wichtige Arterie still an Festigkeit verliert
Die abdominelle Aorta transportiert Blut vom Herzen in den Unterkörper. Bei manchen Menschen dehnt sich ihre Wand allmählich und bildet ein Aneurysma, oft ohne Symptome, bis es groß ist oder reißt. Wissenschaftler wissen, dass die glatten Muskelzellen in der Gefäßwand zugrunde gehen und chronische Entzündung das Stützgewebe abbaut, doch die genaue Form des Zelltods war unklar. Die Autoren konzentrieren sich auf einen Prozess namens Nekroptose — eine „chaotische“ Form des programmierten Zelltods, angetrieben von einem Protein namens MLKL, das Zellen zum Platzen bringt und deren Inhalt freisetzt, wodurch Entzündung ausgelöst wird.
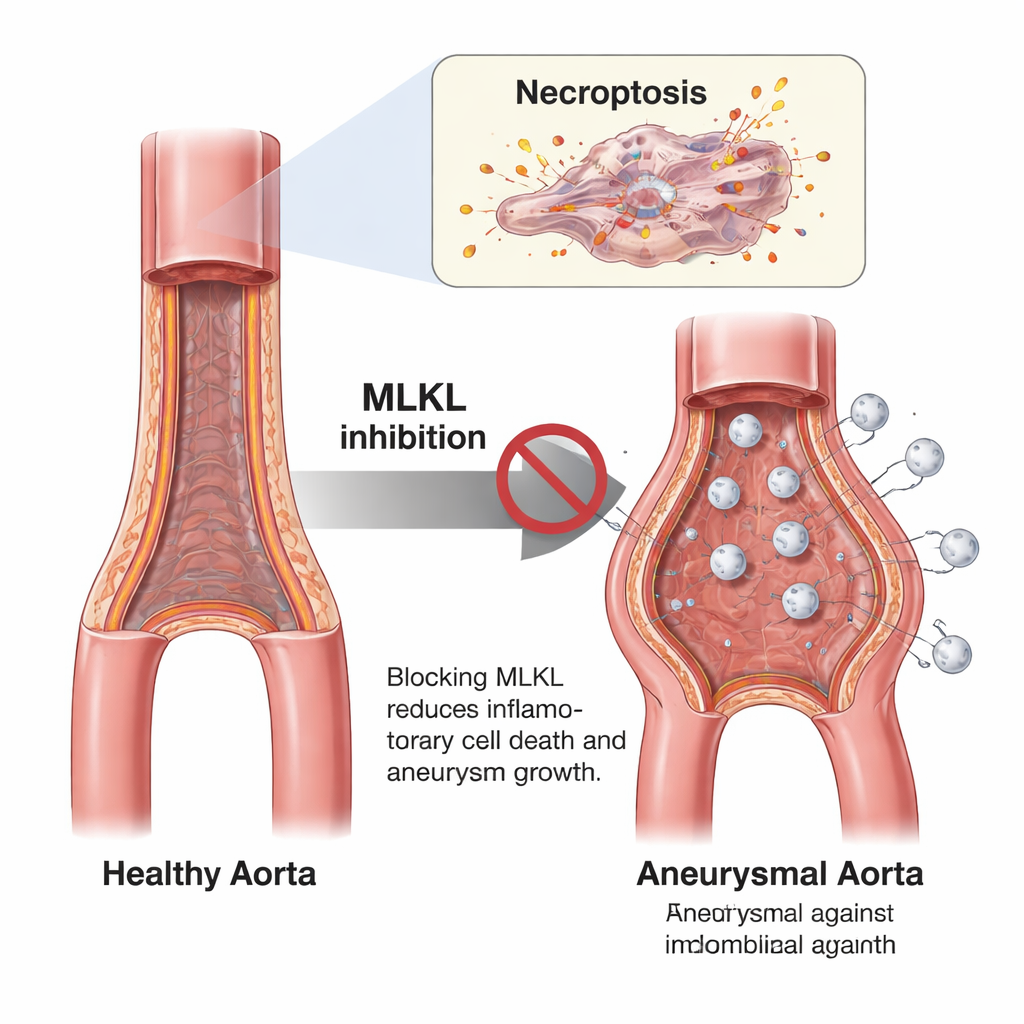
Das Ausschalten eines Todes‑Schalters schützt die Aorta bei Mäusen
Um die Bedeutung der Nekroptose zu prüfen, nutzte das Team Mäuse mit genetischen Veränderungen, die diesen Weg blockieren: Einige fehlten MLKL vollständig, einige trugen eine mutierte Form von MLKL, die nicht aktiviert werden kann, und andere hatten eine Variante des upstream-Proteins RIPK1, die ihre üblichen Signale nicht auslöst. Dann lösten sie aneurysmaähnliche Schäden in der unteren Aorta mit einer Elastase-Lösung aus, die die Gefäßwand schwächt. Im Vergleich zu normalen Mäusen entwickelten Tiere, die Nekroptose nicht ausführen konnten, deutlich kleinere Aneurysmen, behielten eine im Ultraschall normalere Aortenform und zeigten weniger Schäden an Kollagen- und Elastikfasern — den „Bewehrungsstahl und Gummibändern“, die Arterien Festigkeit und Elastizität verleihen.
Weniger entzündliche Zellen dringen in die Gefäßwand ein
Mikroskopische Aufnahmen erklärten, warum die geschützten Mäuse besser abschnitten. Bei normalen Tieren füllte sich die verletzte Aorta schnell mit Neutrophilen und Makrophagen — vorderste weiße Blutkörperchen, die Enzyme und Oxidantien freisetzen und die Wand weiter abbauen. In Mäusen ohne funktionelles MLKL drangen deutlich weniger dieser Zellen in die Aortenwand ein, obwohl ihre Zahl im Blut unverändert blieb. Gleichzeitig war die Schicht der glatten Muskelzellen besser erhalten. Genexpressionsanalysen der Aorta bestätigten dieses Bild: Bei gewöhnlichen Mäusen waren Gene, die mit Entzündung, Rekrutierung von Immunzellen und Blutgerinnungsauflösung verknüpft sind, stark aktiviert, während diese entzündlichen und fibrinolytischen Programme bei nekroptose-defizienten Tieren deutlich abgeschwächt waren.
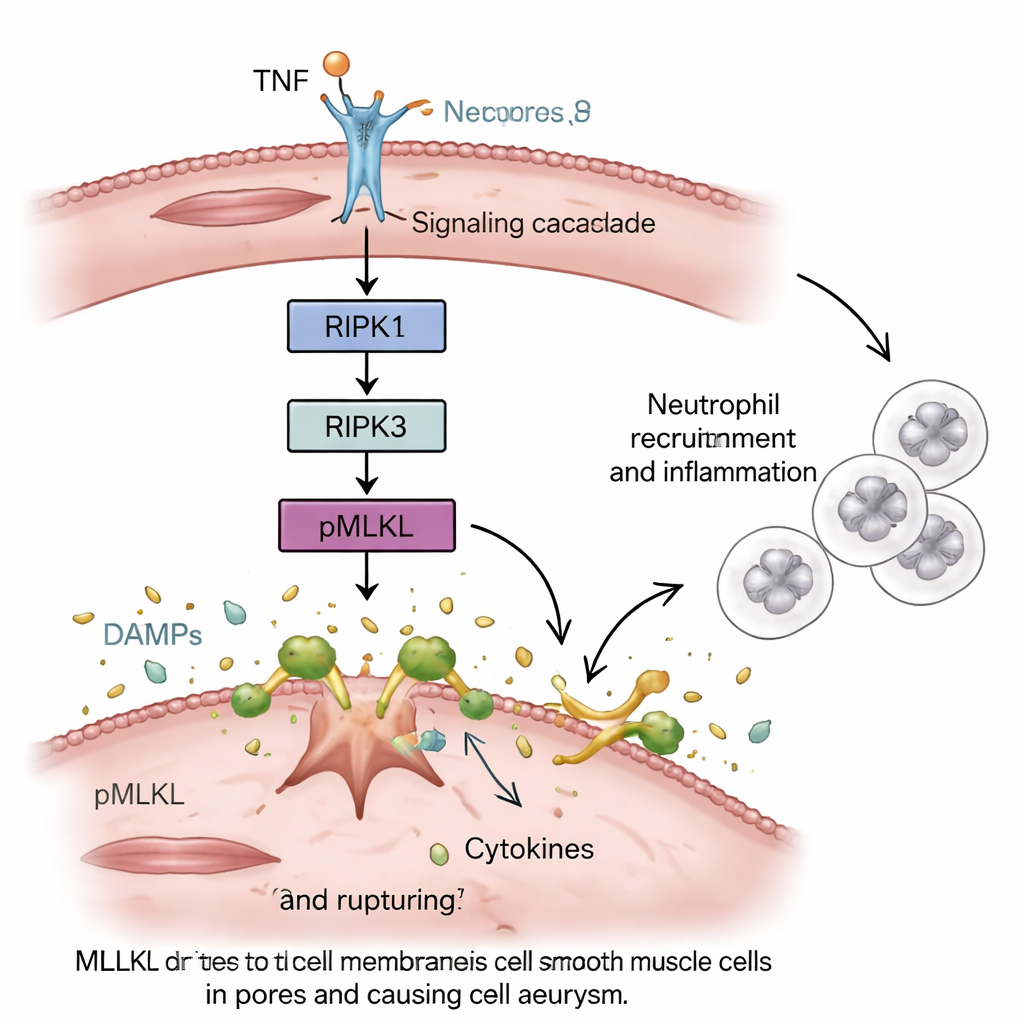
Glatte Muskelzellen vom Schutz in die Anheizung der Entzündung
Als Nächstes fragten die Forscher, wo Nekroptose am wichtigsten ist. Durch Tausch des Knochenmarks zwischen normalen und mutierten Mäusen konnten sie die Effekte in Blutzellen von denen in der Gefäßwand trennen. Der deutlichste Schutz zeigte sich, wenn die aortalen glatten Muskelzellen, nicht die Immunzellen, kein MLKL hatten. In Zellkulturen mit menschlichen und Maus‑glatten Muskelzellen führte erzwungene MLKL-getriebene Nekroptose dazu, dass die Zellen aufplatzten und Gefahren‑Signale sowie entzündliche Moleküle freisetzten. Diese Sekrete zogen Neutrophilen-ähnliche Zellen stark an und aktivierten sie, wodurch diese zu den sterbenden Muskelzellen wanderten. Als ein MLKL-blockierender Wirkstoff hinzugefügt wurde, verringerten sich sowohl der Zelltod der glatten Muskelzellen als auch die daraus resultierende Aktivierung der Neutrophilen.
Ein möglicher neuer Weg, das Wachstum von Aneurysmen zu bremsen
Setzt man diese Ergebnisse zusammen, legt die Studie nahe, dass glatte Muskelzellen in der Aorta, wenn sie durch Nekroptose zugrunde gehen, nicht einfach verschwinden; sie locken aktiv Immunzellen an und entzünden einen Kreislauf aus Entzündung und Gewebeabbau, der das Aneurysmawachstum vorantreibt. Das Entfernen oder Deaktivieren von MLKL bei Mäusen unterbricht diesen Zyklus, erhält die Gefäßwand und begrenzt die Aneurysmenbildung. Für Patientinnen und Patienten eröffnet dies die Möglichkeit, dass künftige Medikamente, die MLKL anvisieren, das Fortschreiten abdomineller Aortenaneurysmen verlangsamen oder verhindern könnten und so eine medizinische Alternative zum „abwarten“ und zur späten OP bieten. Solche Therapien sind zwar noch nicht verfügbar, doch diese Arbeit zeichnet ein konkretes molekulares Ziel zum Schutz eines der wichtigsten Blutgefäße des Körpers nach.
Zitation: Nemade, H., Mehrkens, D., Lottermoser, H.S. et al. Loss of MLKL impairs abdominal aortic aneurysm development by attenuating smooth muscle cell necroptosis. Cell Death Dis 17, 217 (2026). https://doi.org/10.1038/s41419-026-08427-4
Schlüsselwörter: abdominelles Aortenaneurysma, Nekroptose, glatte Muskelzellen, MLKL-Hemmung, gefäßerkrankliche Entzündung