Clear Sky Science · de
TRPA1 fördert das Fortschreiten der überaktiven Blase, indem es den NLRP3-Inflammasom aktiviert und Pyroptose antreibt
Warum eine reizbare Blase wichtig ist
Das plötzliche Dringungsgefühl zur Toilette, mehrmaliges nächtliches Aufstehen oder die Angst vor unwillkürlichem Harnverlust sind häufige Probleme, die unter „überaktive Blase“ zusammengefasst werden. Diese Erkrankung betrifft weltweit etwa eine von fünf Personen und kann Schlaf, Arbeit, Reisen und Sozialleben schleichend beeinträchtigen. Die meisten verfügbaren Medikamente bringen jedoch nur mäßige Linderung und können störende Nebenwirkungen haben. Diese Studie untersucht eine neu entdeckte Kaskade im Inneren der Blase, die erklären könnte, warum sie so überempfindlich wird – und weist auf neue Behandlungsoptionen hin, die über eine rein muskelentspannende Wirkung hinausgehen.
Ein verborgener Auslöser in der Blasenwand
Tief in der Blasenschleimhaut tragen Zellen ein Sensorprotein namens TRPA1, das auf physikalischen und chemischen Stress reagiert. Die Forschenden analysierten Urinzellen von Frauen mit überaktiver Blase sowie Blasengewebe aus Tiermodellen, die sowohl kurzzeitige als auch langanhaltende Erkrankungen nachbilden. Sie fanden heraus, dass die TRPA1-Werte bei überaktiver Blase durchgängig höher waren als bei gesunden Kontrollen, und je mehr TRPA1 die Zellen einer Person produzierten, desto stärker waren ihre Symptombewertungen. Bei Tieren ging ein erhöhtes TRPA1 einher mit einer reizbaren Blase, die häufiger kontrahierte, weniger Urin benötigte, um die Entleerung auszulösen, und Schwellungen sowie strukturelle Veränderungen der Wand zeigte.
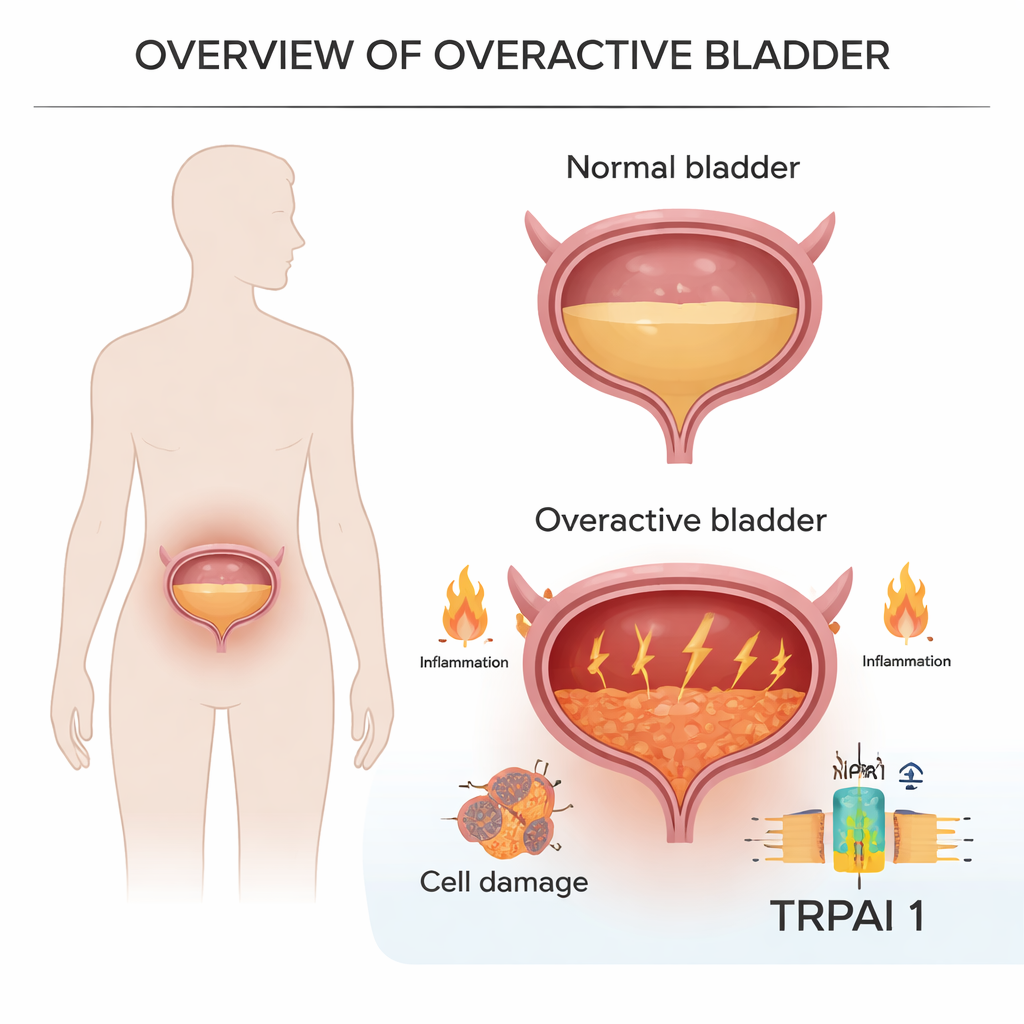
Entzündung verbindet Nerven, Verletzung und Dringlichkeit
Das Team untersuchte anschließend, welche Gene bei überaktiven Blasen hochreguliert sind. Viele davon standen im Zusammenhang mit Entzündung – dem chemischen Alarmsystem des Körpers – einschließlich bekannter Botenstoffe wie IL-6 und TNF. Diese Veränderungen zeigten sich nicht nur in ihren eigenen Mausmodellen, sondern auch in öffentlichen Datensätzen von Menschen mit Blasenproblemen. In Mäusen und Ratten mit überaktiver Blase waren entzündliche Gene im Blasengewebe deutlich hochreguliert, was darauf hindeutet, dass die Erkrankung nicht nur ein mechanisches Muskelproblem ist, sondern auch eine entzündliche Erkrankung, bei der die Schleimhautzellen gestresst, geschädigt sind und fortlaufend Alarmsignale aussenden.
Eine feurige Form des Zelltods
Ein wichtiger Pfad stach heraus: eine molekulare Maschinerie namens NLRP3-Inflammasom. Wenn es aktiviert wird, schaltet NLRP3 ein Enzym (Caspase-1) ein, das ein weiteres Protein, Gasdermin D, so zerschneidet, dass es porenbildend in Zellmembranen wirkt. Dieser Prozess, Pyroptose genannt, lässt Zellen anschwellen und aufbrechen und setzt entzündliche Moleküle wie IL-1β und IL-18 in das umgebende Gewebe frei. Die Studie zeigte, dass in Modellen der überaktiven Blase NLRP3, aktives Caspase-1 und gespaltenes Gasdermin D erhöht waren, besonders in der inneren Schleimhautschicht der Blase. Einfach gesagt: Gestresste Blasenzellen funktionierten nicht nur schlecht – sie starben explosionsartig und schürten einen Kreislauf aus Reizung und Überaktivität.
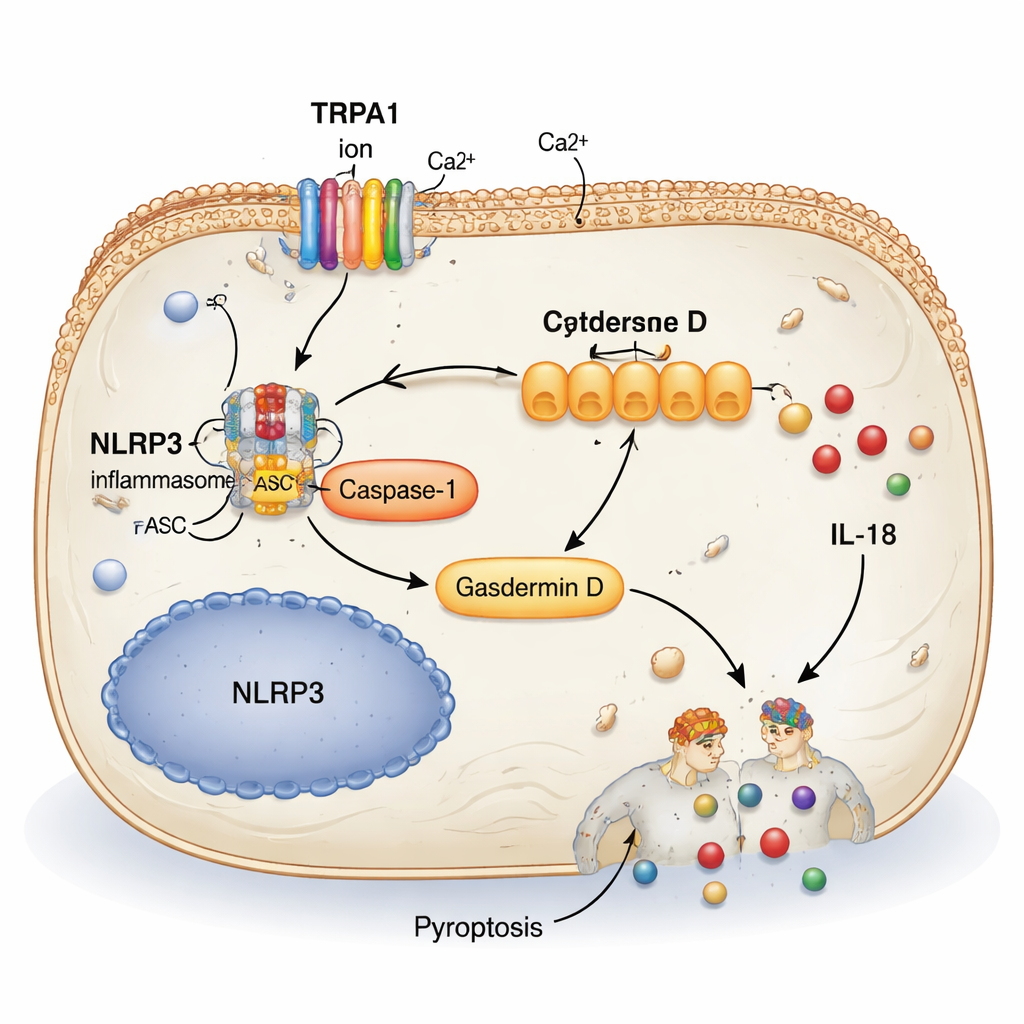
Die Kettenreaktion abschalten
Um zu prüfen, ob TRPA1 diese schädliche Kaskade antreibt, setzten die Forschenden ein Medikament namens HC-030031 ein, das TRPA1-Kanäle blockiert. In Blasenzellen, die einer schädlichen Chemikalie ausgesetzt waren, reduzierte der Blocker die TRPA1-Spiegel, dämpfte entzündliche Gene und verbesserte das Überleben der Zellen. Bei Mäusen mit überaktiver Blase milderte derselbe Blocker Entzündungen, senkte Marker der Pyroptose und verbesserte das Blasenverhalten deutlich – weniger Harnspuren, längere Intervalle zwischen den Entleerungen und bessere Dehnbarkeit der Blase. Als das Team künstlich die NLRP3-Spiegel in der Blase anstieg, verschwanden diese Vorteile größtenteils wieder, was zeigt, dass die schädlichen Effekte von TRPA1 hauptsächlich über den NLRP3–Pyroptose-Weg vermittelt werden. Sie fanden außerdem heraus, dass TRPA1 die NLRP3-Produktion steigert, indem es mit zwei DNA-bindenden Proteinen, MAZ und SMAD3, zusammenarbeitet, die die Expression des NLRP3-Gens fördern.
Was das für Menschen mit Blasendrang bedeutet
Kurz gesagt schlägt die Studie vor, dass eine überaktive Blase zum Teil durch einen überempfindlichen Sensor (TRPA1) auf Schleimhautzellen angetrieben wird, der ein entzündliches Todesprogramm (NLRP3-Inflammasom und Pyroptose) hochfährt. Das macht die Blasenwand durchlässig, entzündet und überreagibel, sodass sie „Jetzt entleeren“ signalisiert, selbst wenn nur eine geringe Urinmenge vorhanden ist. Durch Blockade von TRPA1 oder Unterbrechung des NLRP3-Wegs könnte man dieses innere Alarmsystem beruhigen, die Schleimhaut schützen und Dringlichkeit sowie Häufigkeit reduzieren. Obwohl die Arbeit noch experimentell ist, eröffnet sie die Möglichkeit einer neuen Klasse von Therapien, die die zugrundeliegende entzündliche Verschaltung der überaktiven Blase ansprechen, statt nur ihre Muskelkontraktionen.
Zitation: Rao, Y., Wang, Y., Gao, J. et al. TRPA1 promotes overactive bladder progression by activating the NLRP3 inflammasome and driving pyroptosis. Cell Death Dis 17, 226 (2026). https://doi.org/10.1038/s41419-026-08426-5
Schlüsselwörter: überaktive Blase, TRPA1, Entzündung, NLRP3-Inflammasom, Pyroptose