Clear Sky Science · de
p16-vermittelte G0/G1-Zellzyklusarretierung führt zu SASP und Fibrose bei der Fuchs-Endothel-Dystrophie der Hornhaut
Warum diese Augenerkrankung wichtig ist
Im Alter ist eine weniger bekannte Bedrohung des Sehvermögens die sogenannte Fuchs-Endothel-Dystrophie (FECD), bei der die sonst klare Vorderfläche des Auges allmählich eintrübt. Dieser Artikel untersucht, warum bestimmte Zellen an der Innenseite der Hornhaut im Laufe der Zeit ausfallen und vernarben und warum Frauen häufiger betroffen sind. Das Verständnis dieser verborgenen Veränderungen könnte den Weg für Medikamente öffnen, die eine Hornhauttransplantation verzögern oder vielleicht verhindern.
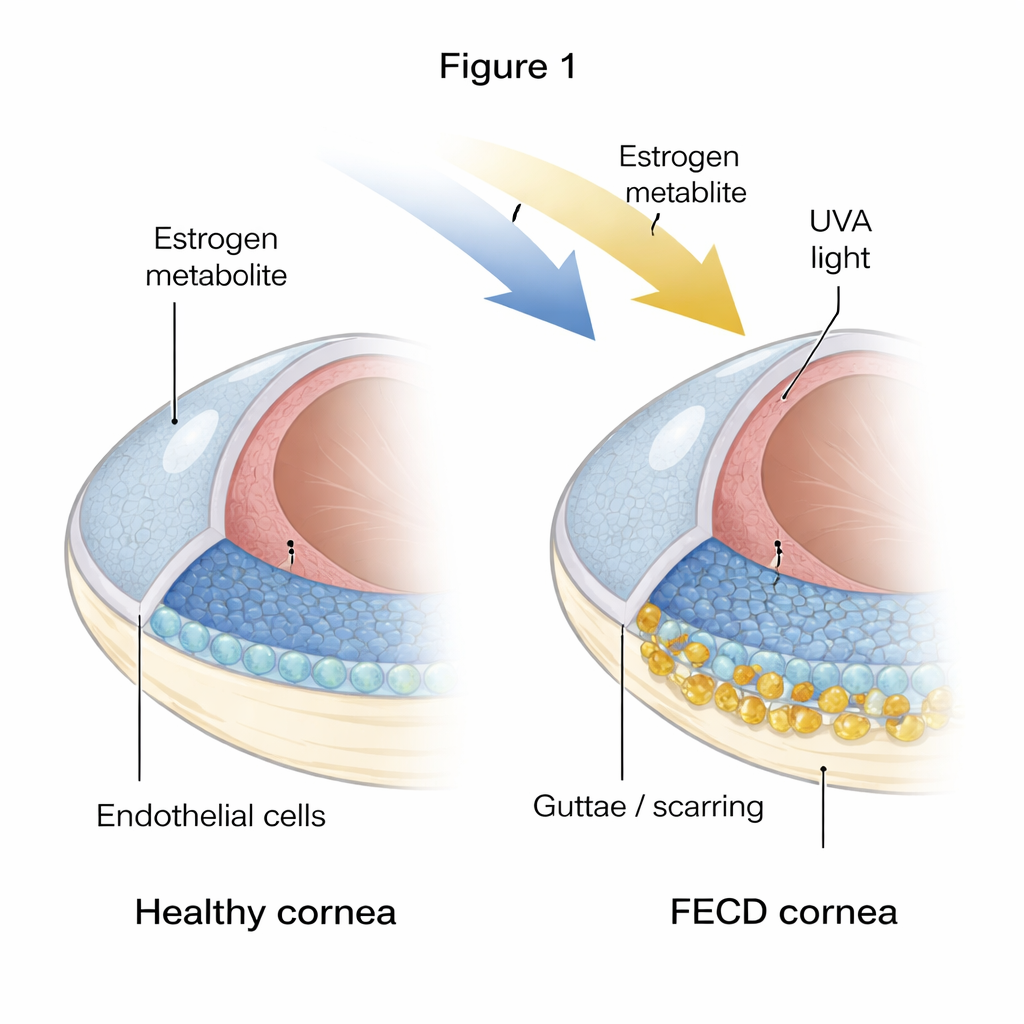
Die fragile innere Schicht der Hornhaut
Die Hornhaut muss präzise entwässert bleiben, um transparent zu sein — eine Aufgabe, die von einer einzigen Zellschicht aus sechseckigen Endothelzellen übernommen wird. Bei FECD sterben viele dieser Zellen und die Schicht wird fleckig und unregelmäßig. Gleichzeitig bilden sich harte Erhebungen und verdicktes Material, bekannt als Guttae und überschüssige extrazelluläre Matrix, an der Innenseite. Die Autoren verglichen gesunde Spenderhornhäute mit Hornhäuten von FECD-Patienten und fanden starke Hinweise darauf, dass das erkrankte Gewebe sowohl „gealtert“ als auch fibrotisch ist: Die Zellen zeigten Marker der Seneszenz (ein permanenter Stillstand) und der Fibrose (Zellen verhalten sich stärker wie narbenbildende Zellen und lagern zusätzliches Gewebe ab).
Chronische Licht- und Hormonbelastung drängt Zellen in eine Sackgasse
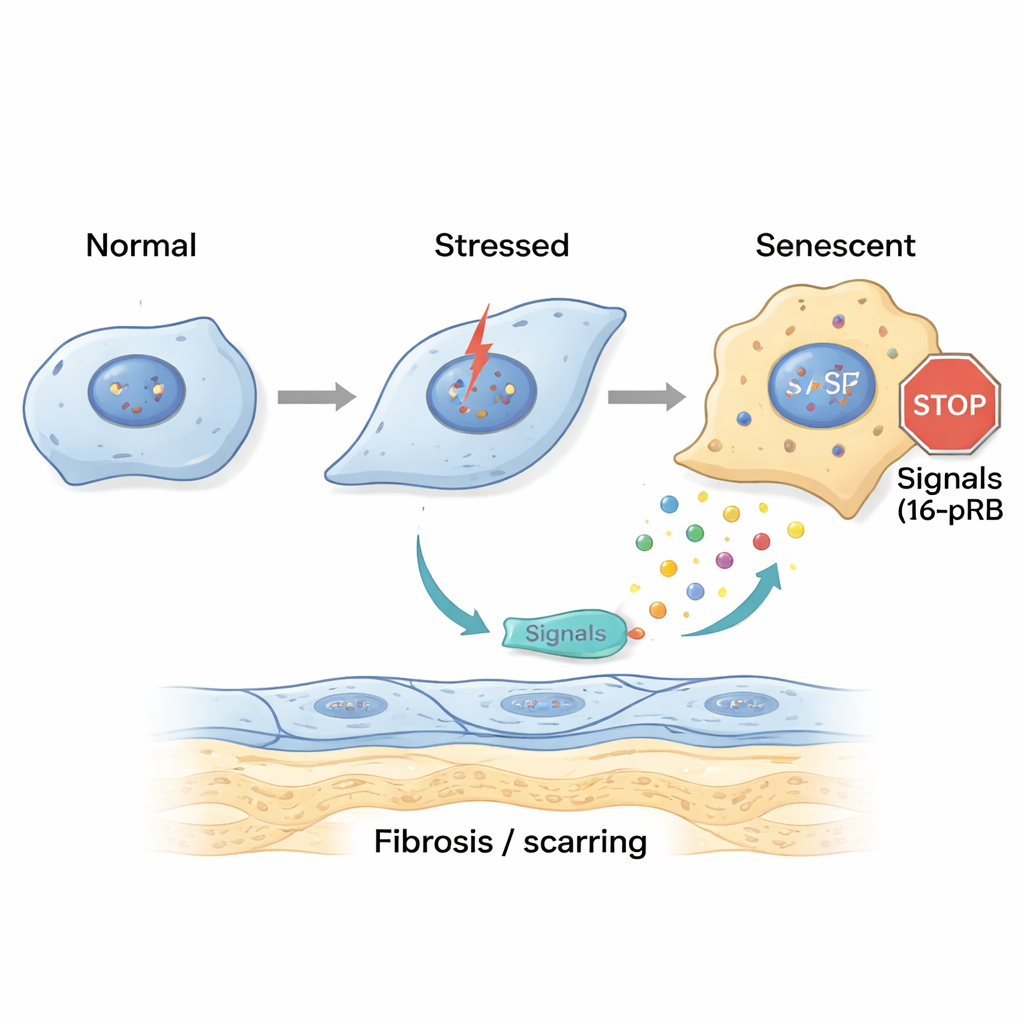
Um zu untersuchen, wie dieser Schaden beginnt, stellten die Forschenden FECD-ähnlichen Stress im Labor nach. Sie setzten gesunde Hornhautendothelzellen ultraviolettem A-Licht (UVA) und 4-Hydroxyestradiol aus, einem oxidierten Östrogenabbauprodukt, das mit DNA-Schäden in Verbindung steht. Ein kurzer, einmaliger Stressstoß ließ Zellen vorübergehend in einem späten Zellzyklusstadium stoppen und eine frühe Umwandlung in einen eher fibroblastähnlichen Zustand beginnen, wobei eine gewisse Erholungsfähigkeit erhalten blieb. Im Gegensatz dazu trieb wiederholte, chronische Exposition die Zellen in einen anderen Zustand: Sie sammelten sich in einem frühen Zellzyklusstadium namens G0/G1 und schalteten ein Gen namens p16 ein, das den Zellzyklus über sein Partnerprotein pRB blockiert. Diese Zellen wurden groß, flach und eindeutig seneszent, zeigten gleichzeitig starke Expression von Fibrosemarkern und Proteinen, die die verdickten Guttae bei FECD ausmachen.
Seneszente Zellen senden schädliche Signale und verbreiten Vernarbung
Seneszente Zellen sitzen nicht einfach ruhig da; sie sezernieren ein Gemisch aus Signalmolekülen, bekannt als senescence-associated secretory phenotype (SASP). Das Team sammelte Flüssigkeit von gestressten Hornhautzellen und trug sie auf frische Zellen sowie auf gesunde Spenderhornhäute auf. Das „akute“ SASP verursachte frühe Anzeichen von Zellformveränderungen, während das „chronische“ SASP viele Zellen in die Seneszenz trieb und Gene förderte, die mit Fibrose und zusätzlicher Matrixablagerung verbunden sind. Detaillierte Analysen zeigten, dass chronisches SASP reich an entzündlichen Botenstoffen wie IL-8 und IL-17 war, die bekanntermaßen Zellalterung, narbige Fibrose und Rekrutierung von Immunzellen fördern. Wenn die Forschenden den IL-17-Signalweg oder den IL-8-Rezeptor CXCR2 blockierten, zeigten Zellen, die chronischem SASP ausgesetzt waren, weniger Seneszenzmarker und weniger Fibrose, was darauf hindeutet, dass diese Signale treibende Kräfte der Erkrankung sind.
Ausmerzen verschlissener Zellen zum Schutz des Sehens
Da p16-positive seneszente Zellen so eng mit Vernarbung verknüpft waren, testeten die Autoren, ob deren Beseitigung die Hornhaut schützen könnte. In einem Mausmodell, in dem UVA-Licht FECD-ähnliche Veränderungen auslöste, behandelten sie die Tiere mit einer senolytischen Wirkstoffkombination, Dasatinib plus Quercetin, die selektiv seneszente Zellen abtötet. Im Vergleich zu unbehandelten Mäusen behielten die mit Senolytika behandelten Tiere ein regelmäßigeres Endothelzellmosaik, behielten insgesamt mehr Zellen und zeigten weniger Marker für Seneszenz, Fibrose und überschüssige Matrix. Mit anderen Worten: Das Entfernen der am stärksten geschädigten Zellen verringerte die Belastung durch schädliche Sekrete und half, eine gesündere Hornhautoberfläche zu erhalten.
Was das für Menschen mit FECD bedeutet
Für Patientinnen und Patienten führt FECD derzeit häufig zur Hornhauttransplantation, wenn das Sehvermögen zu stark eintrübt. Diese Studie schlägt einen anderen Weg vor: Die Erkrankung könnte durch eine langsame Anhäufung gestresster, nicht teilender Zellen angetrieben werden, die sowohl ihre Funktion nicht erfüllen als auch ihre Nachbarn mit entzündlichen und fibrotischen Signalen schädigen. Das Anvisieren dieser Signale mit Medikamenten gegen IL-17- oder IL-8-Wege oder die Anwendung senolytischer Therapien, um selektiv die am stärksten geschädigten Zellen zu entfernen, könnten eines Tages die Vernarbung verzögern, mehr des natürlichen Gewebes erhalten und den Bedarf an Operationen hinauszögern oder verringern.
Zitation: Parekh, M., Adhikari, Y., Deshpande, N. et al. p16-mediated G0/G1 cell cycle arrest leads to SASP and fibrosis in Fuchs endothelial corneal dystrophy. Cell Death Dis 17, 197 (2026). https://doi.org/10.1038/s41419-026-08425-6
Schlüsselwörter: Fuchs-Dystrophie, Hornhautendothel, zelluläre Seneszenz, Fibrose, senolytische Therapie