Clear Sky Science · de
Mitochondriale DNA treibt die Aktivierung der NLRP3-IL-1β-Achse in Mikroglia durch Bindung an NLRP3 und führt zu Neurodegeneration in Parkinson-Modellen
Warum das für Morbus Parkinson wichtig ist
Morbus Parkinson ist vor allem für Tremor und verlangsamte Bewegungen bekannt, doch unter diesen Symptomen findet ein komplexer Kampf im Gehirn statt. Diese Studie zeigt, wie winzige Fragmente genetischen Materials aus geschädigten Mitochondrien in Gehirnimmunzellen eine Entzündung entfachen können, die nach und nach die dopaminproduzierenden Neurone tötet, die für flüssige Bewegungen nötig sind. Das Verständnis dieser Kettenreaktion eröffnet neue, sehr spezifische Angriffspunkte für Medikamente, die das Parkinson-ähnliche Gewebeversagen verlangsamen oder verhindern könnten.
Gehirn-Immunzellen und Kraftwerke unter Stress
Das Gehirn enthält nicht nur Neurone, sondern auch Mikroglia, seine ansässigen Immunzellen. Bei Morbus Parkinson werden diese Mikroglia häufig überaktiv und setzen toxische Moleküle sowie entzündliche Signale frei, die benachbarte Neurone schädigen. Die Autorinnen und Autoren konzentrierten sich auf Mitochondrien, die "Kraftwerke" der Zellen, die ihre eigene DNA tragen. Wenn Mitochondrien durch Toxine, Alterung oder andere Stressfaktoren beschädigt werden, kann ihre DNA oxidiert werden — eine Form chemischer Schädigung durch reaktive Sauerstoffspezies. Da mitochondriale DNA bakterieller DNA ähnelt, können diese beschädigten Fragmente im Gehirn wie Alarmsignale wirken, das Immunsystem aufscheuchen und möglicherweise chronische Entzündungen antreiben.
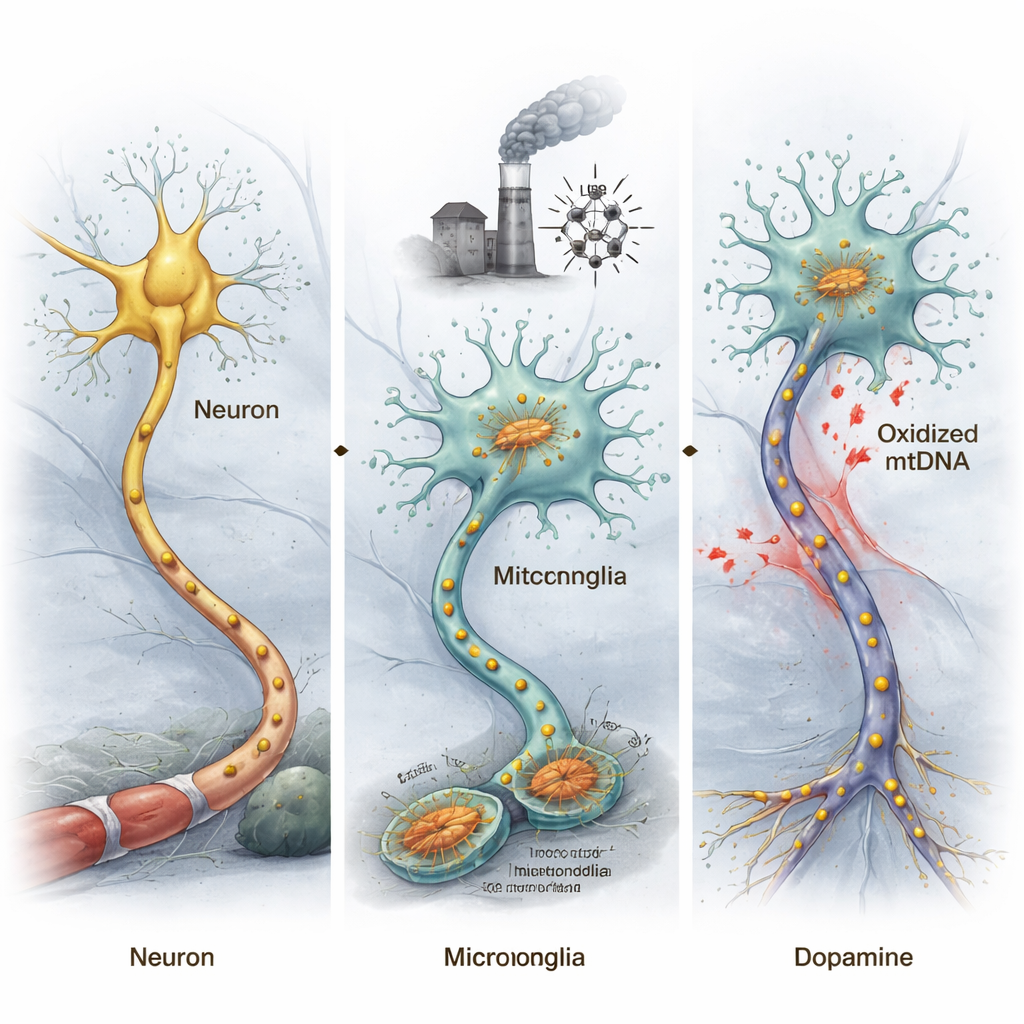
Geschädigte mitochondriale DNA kann Mäuse in Richtung Parkinson-ähnlicher Erkrankung treiben
Um zu testen, ob oxidierte mitochondriale DNA (ox-mtDNA) tatsächlich Parkinson-ähnliche Veränderungen auslösen kann, entnahmen die Forschenden ox-mtDNA aus gestressten Mikroglia und injizierten sie direkt in eine Gehirnregion, die normalerweise dopaminproduzierende Neurone enthält, die für Bewegung wichtig sind. Mäuse, die diesem ox-mtDNA ausgesetzt waren, zeigten in Verhaltenstests verringerte Beweglichkeit und einen Verlust dieser Dopamin-Neurone, was zentrale Merkmale der Parkinson-Krankheit widerspiegelt. Durch die Trennung von Neuronen und Mikroglia aus dem Mittelhirn und die Analyse ihrer Genaktivität stellten die Forschenden fest, dass bei Neuronen Gene, die mit Parkinson assoziiert sind, stärker pathologisch verändert wurden, während entzündungsbezogene Gene in Mikroglia stark aktiviert waren.
Ein molekularer Alarmschalter in Mikroglia
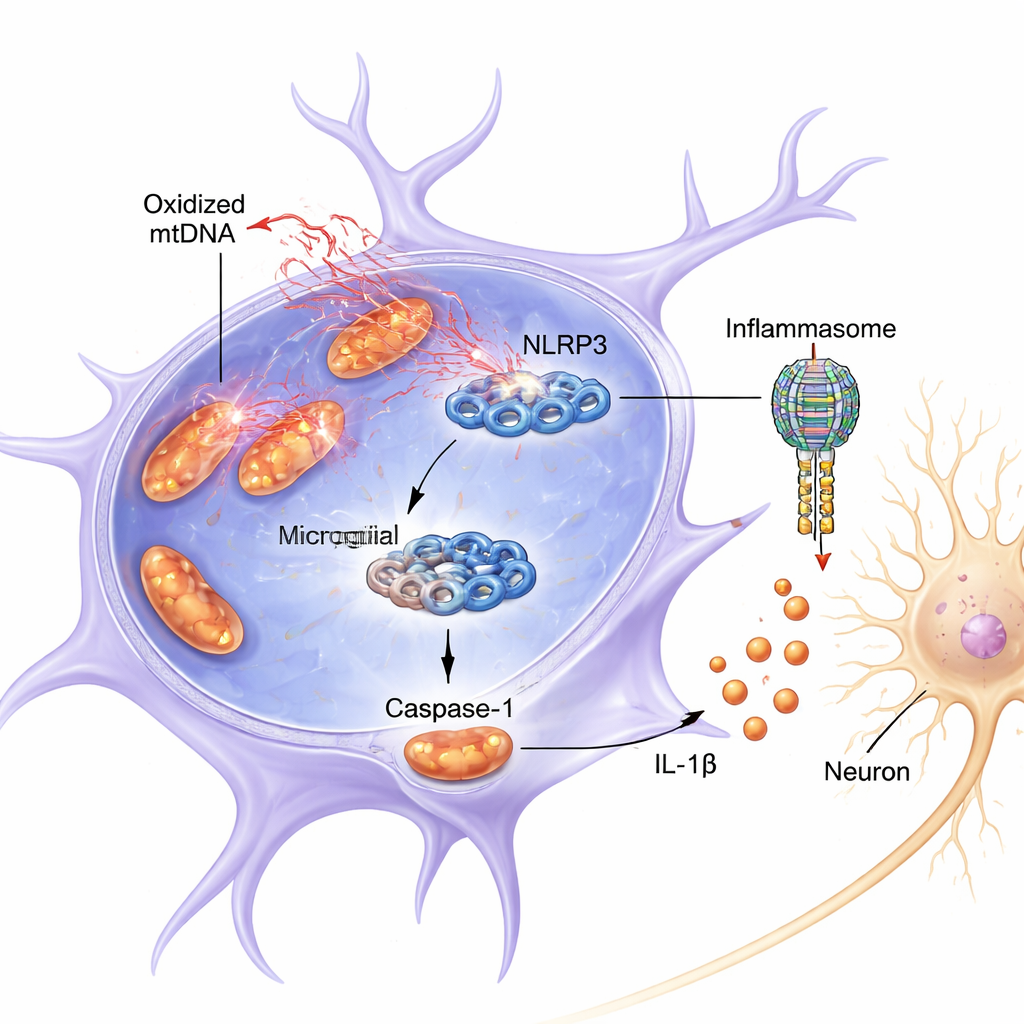
Die Studie fokussierte ein Proteinensemble in Mikroglia namens NLRP3, Teil eines größeren Gebildes, das als Inflammasom bekannt ist. Wenn es eingeschaltet wird, hilft NLRP3 bei der Aktivierung von Caspase-1, einem Enzym, das das entzündliche Molekül IL-1β in seine aktive, schädliche Form schneidet. Sowohl in Mäusen als auch in Kulturen verursachte die Kombination eines entzündlichen Primingsignals (LPS, ein bakterieller Bestandteil) und das pesticidähnliche Toxin Rotenon, dass Mitochondrien in Mikroglia oxidierte mtDNA in das Zellplasma freisetzten. Diese Freisetzung ging einher mit stärkerer Aktivierung von NLRP3, mehr geschnittener (aktiver) Caspase-1 und erhöhten IL-1β-Werten. Medium, das aus diesen überaktivierten Mikroglia entnommen wurde, war direkt toxisch für dopaminähnliche Neurone, die in einer Kultur gezüchtet wurden, reduzierte deren Überleben und den Gehalt ihres wichtigen Markers Tyrosinhydroxylase.
Direkte Bindung: wie oxidierte DNA den NLRP3-Schalter umlegt
Über bloße Korrelation hinaus zeigten die Autorinnen und Autoren, dass ox-mtDNA nicht nur bei Entzündung vorhanden ist — sie scheint physisch an NLRP3 zu binden und es zu aktivieren. Als sie die Freisetzung mitochondrialer DNA mit einem Wirkstoff blockierten, sanken die Aktivierung von Caspase-1 und IL-1β. Umgekehrt erhöhte die direkte Verabreichung oxidierter mtDNA in Mikroglia die NLRP3-Signalisierung deutlich stärker als nicht-oxidierte mtDNA. Biochemische Pull-down-Experimente zeigten mtDNA mit reichen Markern oxidativen Schadens, die an NLRP3 gebunden war. Computermodelle und Proteinchemie enthüllten, dass ox-mtDNA an ein positiv geladenes, flexibles Segment von NLRP3 bindet (eine „intrinsisch ungeordnete Region“ zwischen den Aminosäuren 180–187). Wenn dieser kritische Abschnitt aus NLRP3 entfernt wurde, war seine Fähigkeit, ox-mtDNA zu binden und Caspase-1 zu aktivieren, stark reduziert.
Das Abschalten des Inflammasoms schont Neurone
Die Forschenden fragten dann, ob die Störung von NLRP3 Neurone schützen könne. In kultivierten Mikroglia führte eine genetische Reduktion von NLRP3 zu deutlich geringerer Aktivierung von Caspase-1 und IL-1β nach LPS‑ und Rotenon‑Behandlung, und das konditionierte Medium dieser Zellen war wesentlich weniger toxisch für dopaminähnliche Neurone. In Mäusen reduzierte ein selektiver NLRP3‑Inhibitor (MCC950) die Mikroglia-Aktivierung, bewahrte Dopamin-Neurone und senkte inflammasombezogene Proteine in Modellen, die entweder durch LPS plus Rotenon oder durch injizierte mtDNA ausgelöst wurden. Zusammengenommen zeigen diese Experimente, dass die ox-mtDNA–NLRP3–IL-1β-Kette nicht nur mit Schäden assoziiert ist, sondern für einen Großteil des beobachteten Neuronenverlusts erforderlich ist.
Was das für künftige Parkinson‑Therapien bedeutet
Für Nichtfachleute lautet die Kernaussage: Beschädigte mitochondriale DNA, die aus Gehirn-Immunzellen austritt, kann sich direkt an einen internen „Alarmschalter“ (NLRP3) heften und eine Entzündungswelle auslösen, die Dopamin-Neurone schädigt und in Modellen Parkinson‑ähnliche Erkrankung antreibt. Da diese Wechselwirkung von einem kurzen, klar definierten Abschnitt des NLRP3‑Proteins und von der oxidierten Beschaffenheit der mitochondrialen DNA abhängt, bietet sie präzise neue Arzneimittelziele. Therapien, die mitochondriale DNA‑Schädigung oder deren Austritt verhindern, ihre Bindung an NLRP3 blockieren oder NLRP3 selbst hemmen, könnten prinzipiell diese entzündliche Kaskade dämpfen und das Fortschreiten der Parkinson‑Krankheit verlangsamen.
Zitation: Gan, Q., Fu, X., Zhou, T. et al. Mitochondrial DNA drives NLRP3-IL-1β axis activation in microglia by binding to NLRP3, leading to neurodegeneration in Parkinson’s disease models. Cell Death Dis 17, 213 (2026). https://doi.org/10.1038/s41419-026-08424-7
Schlüsselwörter: Morbus Parkinson, Mikroglia, mitochondriale DNA, NLRP3-Inflammasom, Neuroinflammation