Clear Sky Science · de
Mangel an SLC46A1-vermittelter Folatrestriktion unterdrückt das Fortschreiten von Darmkrebs durch epigenetisch-transkriptionelle Umprogrammierung
Warum Vitamin B9 und Darmkrebs ein unerwartetes Paar bilden
Viele Menschen kennen Folat bzw. Vitamin B9 als wichtigen Nährstoff in der Schwangerschaft und für die Herzgesundheit. Diese Studie zeigt, dass Folat auch eine überraschende Rolle bei Kolon- und Rektumkarzinomen spielt. Der Dreh ist, dass der Nutzen von Folat von einem einzelnen Torwächterprotein auf Krebszellen abhängt, genannt SLC46A1, das entscheidet, wie viel Folat tatsächlich in die Tumorzellen gelangt. Das Verständnis dieses verborgenen Tors kann helfen zu erklären, warum frühere Forschung zu Folat und Krebs so widersprüchlich war, und könnte den sicheren Einsatz von Folat in Ernährung und Therapie leiten.
Ein Nährstoff-Torwächter im Darm
Zellen unseres Darms können Folat nicht selbst herstellen; sie müssen es aus ihrer Umgebung über spezielle Transportproteine aufnehmen. Die Autorinnen und Autoren zeigen, dass SLC46A1 der wichtigste Folattransporter im menschlichen Kolon ist und deutlich aktiver als andere bekannte Folatträger. Beim Vergleich großer öffentlicher Krebsdatensätze und Gewebeproben von Patientinnen und Patienten stellten sie fest, dass die SLC46A1-Spiegel in kolorektalen Tumoren im Vergleich zum angrenzenden gesunden Gewebe deutlich reduziert sind. Tumoren mit weniger SLC46A1 neigten dazu, weiter fortgeschritten zu sein, häufiger zu streuen und mit schlechterem Überleben der Patienten verbunden zu sein, was darauf hindeutet, dass dieser Transporter in diesem Krebs eher wie eine Bremse als wie ein Beschleuniger wirkt.
Wie der Verlust des Tors das Krebsverhalten verändert
Um zu testen, was SLC46A1 tatsächlich bewirkt, veränderten die Forschenden dessen Menge in kolorektalen Krebszelllinien nach oben und unten. Bei Verringerung von SLC46A1 wuchsen die Krebszellen schneller, bewegten sich leichter und invasierten in Labormodellen durch künstliche Barrieren. Bei Erhöhung von SLC46A1 in Zellen mit ursprünglich niedrigen Werten wurden die Zellen weniger invasiv. Ähnliche Muster zeigten sich in Mäusen: Aus SLC46A1-defizienten Zellen gezüchtete Tumore waren größer und führten zu mehr Lungenmetastasen. Gleichzeitig enthielten Tumore und kultivierte Zellen mit weniger SLC46A1 weniger Folat im Inneren, was bestätigt, dass dieses Protein tatsächlich als wichtiger Eintrittspunkt für das Vitamin fungiert.
Von Vitaminmangel zu gestörter Genkontrolle
Folat leistet mehr als nur die Versorgung mit DNA-Bausteinen; es versorgt auch ein chemisches System, das winzige Methyl-„Marken“ an der DNA anbringt, die dabei helfen, Gene ein- oder auszuschalten. Das Team zeigte, dass beim Verlust von SLC46A1 und sinkendem zellulärem Folat die generelle Fähigkeit, diese Marken anzubringen, abnimmt. Das führt selektiv zum Verlust von Methylmarken in der Kontrollregion eines Gens namens FOS, einem bekannten Treiber für Zellwachstum. Ohne diese Marken wird FOS aktiviert und schaltet mehrere Gene an, die „Wachstum und Ausbreitung“ fördern, darunter CCND1, BCL2 und PLAU, die Krebszellen helfen, sich zu teilen, dem Zelltod zu entgehen und ins umliegende Gewebe vorzudringen. Das Blockieren von FOS oder PLAU beseitigte weitgehend das zusätzliche Wachstum und die Invasivität, die durch den Verlust von SLC46A1 verursacht wurden, und verknüpft diese Ereigniskette direkt.
Wenn Folat nur hilft, wenn die Tür offen ist
Die Studie klärt auch, wann Folat für Tumore günstig oder schädlich ist. In Zellkulturen, die in Folatarmen Bedingungen gehalten wurden, verlangsamte das Wiederauffüllen mit Folat in Konzentrationen, die im menschlichen Blut vorkommen, das Wachstum und die Bewegung der Krebszellen – aber nur, wenn SLC46A1 vorhanden war, um das Folat hereinzubringen. In Tumoren von Mäusen führten direkte Injektionen von Folat in die Tumormasse zu kleinerem Wachstum und zu weniger Anzeichen von Zellteilung, wiederum nur wenn die Krebszellen noch SLC46A1 produzierten. Tumoren ohne den Transporter reagierten kaum. In Patientenproben beobachteten die Forschenden ein umgekehrtes Muster: Tumoren mit hohem SLC46A1 hatten weniger Folat in der umgebenden Flüssigkeit, als ob sie es effizient aufnahmen, und zeigten niedrigere Levels von FOS und PLAU. Tumoren mit niedrigem SLC46A1 ließen mehr Folat ungenutzt und wiesen höhere Level dieser aggressiven Marker auf.
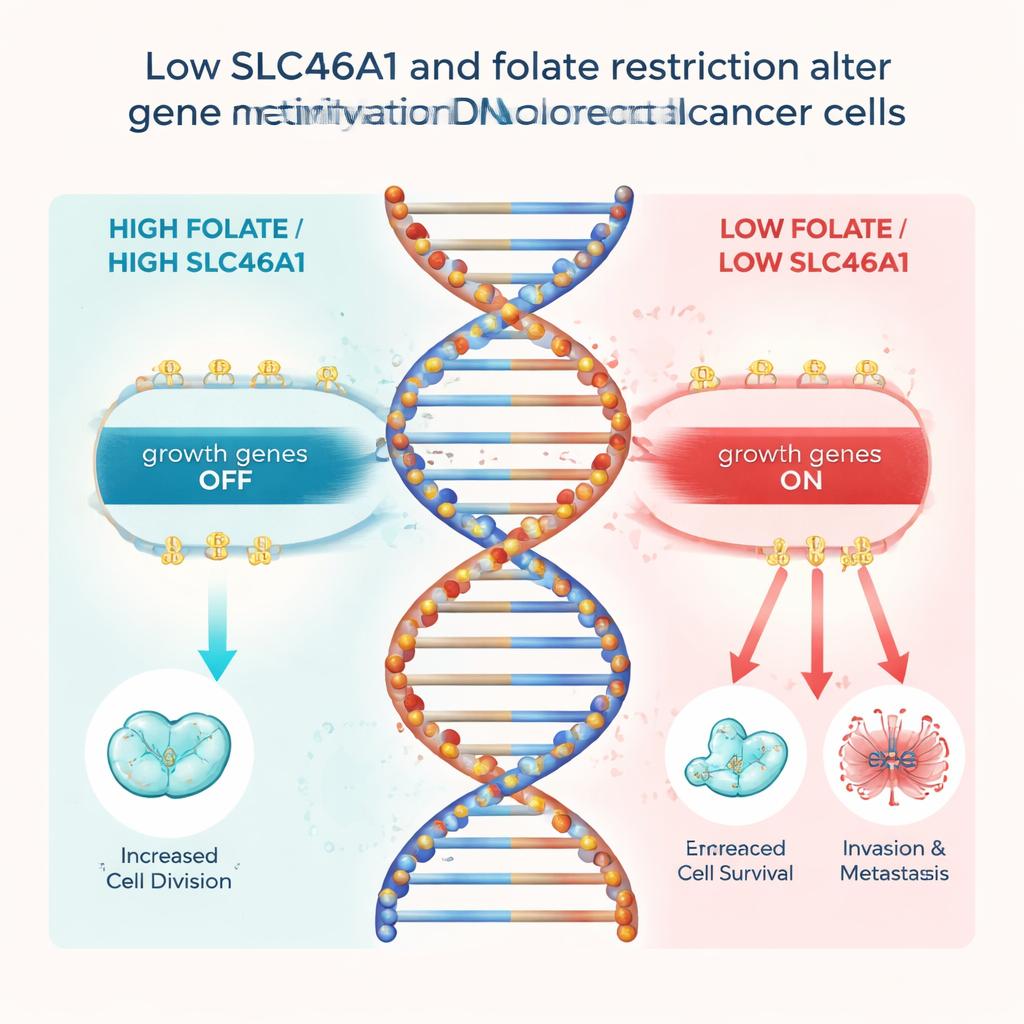
Was das für Patientinnen, Patienten und Prävention bedeutet
Für Laien lautet die Kernbotschaft, dass die Wirkung von Folat auf kolorektalen Krebs davon abhängt, ob die Tumorzellen noch das SLC46A1-„Tor“ exprimieren, das Folat hereinlässt. Ist dieses Tor vorhanden, können realistische Mengen an Folat eine gesunde DNA-Markierung unterstützen und wachstumsfördernde Gene in Schach halten. Fehlt das Tor, kann der Tumor Folat nicht auf diese schützende Weise nutzen und wechselt stattdessen in einen aggressiveren Zustand, angetrieben von entfesselten Genen wie FOS. Diese Arbeit legt nahe, dass künftige Tests kolorektaler Tumore auf SLC46A1-Spiegel Ärzten helfen könnten, Prognose einzuschätzen und zu entscheiden, ob folatbezogene Ernährung oder Therapien wahrscheinlich nützen – ein Schritt hin zu personalisierter, nährstoffbewusster Krebsmedizin.
Zitation: Zhou, Y., Liu, Y., Liu, Y. et al. SLC46A1 deficiency-mediated folate restriction suppresses colorectal cancer progression through epigenetic-transcriptional reprogramming. Cell Death Dis 17, 189 (2026). https://doi.org/10.1038/s41419-026-08423-8
Schlüsselwörter: Folat, Darmkrebs, Epigenetik, SLC46A1, DNA-Methylierung