Clear Sky Science · de
Lactylierung von SLC26A3 im sauren Tumormikromilieu fördert das maligne Fortschreiten von kolorektalem Karzinom
Warum Tumorazidität wichtig ist
Das kolorektale Karzinom gehört weiterhin zu den tödlichsten Krebsarten weltweit, teilweise weil Tumoren häufig zurückkehren, metastasieren oder nicht mehr auf Medikamente ansprechen. Diese Studie untersucht einen bislang wenig beachteten Verursacher dieses Verhaltens: das saure, milchsäurereiche Milieu innerhalb von Tumoren. Indem die Autorinnen und Autoren zeigen, wie diese raue Umgebung ein schützendes Membranprotein namens SLC26A3 destabilisiert, legen sie eine neue Abfolge von Vorgängen offen, die Krebszellen dazu bringt, stamzellähnlicher, invasiver und medikamentenresistenter zu werden — und liefern damit neue Ansatzpunkte für Therapien.
Eine raue Nachbarschaft rund um Krebszellen
Schnell wachsende Tumoren verbrauchen große Mengen Zucker und Sauerstoff und setzen Milchsäure und Wasserstoffionen frei, die ihr Umfeld ansäuern. Anhand großer Patientendatensätze und Gewebeproben zeigen die Forschenden, dass dieser saure Zustand, verfolgt über das Markerprotein CA9, mit aggressiven kolorektalen Tumoren einhergeht. In fortgeschritteneren Tumoren sind die CA9-Werte hoch, während SLC26A3-Werte durchgängig niedrig sind. SLC26A3 sitzt normalerweise an der Oberfläche von Darmzellen und hilft, Salz und Bicarbonat auszubalancieren, was wiederum die pH-Kontrolle unterstützt. In Tumorproben, Zelllinien und Einzelzellanalyse finden die Forschenden, dass mit steigendem Säuregrad die SLC26A3-Spiegel sinken — besonders in malignen, stamzellähnlichen Krebszellen. 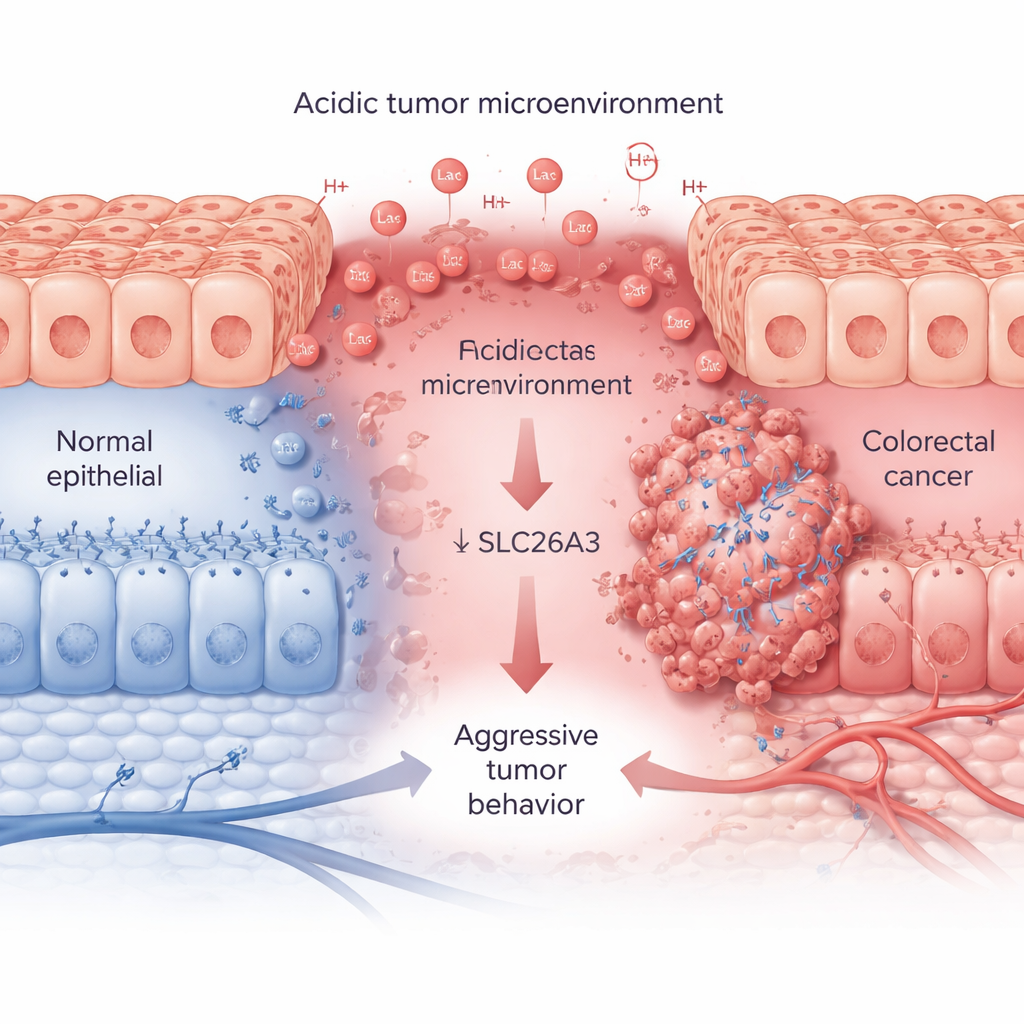
Wie Milchsäure ein Ziel für den Abbau markiert
Die Autoren fragen anschließend, warum SLC26A3 in sauren Tumoren abnimmt. Sie konzentrieren sich auf die Lactylierung, eine neu entdeckte chemische Markierung, die aus Milchsäure entsteht und an Proteine angeheftet werden kann. Wenn kolorektale Krebszellen Milchsäure ausgesetzt oder in sauren Bedingungen kultiviert werden, wird SLC26A3 stark lactyliert. Detaillierte Proteinanalyse identifiziert eine Schlüsselstelle, die Aminosäure K536, an der diese Markierung hinzugefügt wird. Die Lactylierung an K536 macht SLC26A3 weniger stabil: Das Protein wird wahrscheinlicher mit Ubiquitin markiert, einem zellulären „Weg damit“-Signal, und zum Recycling in der Zelle geschickt. Die Blockade des Enzyms p300, das beim Anbringen der Lactylierungsmarken hilft, schützt SLC26A3 teilweise vor dem Abbau. Als Folge macht die Azidität zusammen mit Lactat eine schädliche Rückkopplungsschleife aus — mehr Lactat führt zu mehr Lactylierung, was SLC26A3 reduziert, den pH-Wert weiter stört und ein noch saureres Mikromilieu begünstigt.
Ein Bremsmechanismus für Stammzelligkeit und Ausbreitung wird ausgeschaltet
Bei reduziertem SLC26A3 verhalten sich Krebszellen aggressiver. In Zellkultur exprimieren kolorektale, stamzellähnliche Zellen natürlicherweise weniger SLC26A3 als ihre nicht-stammzellartigen Gegenstücke. Wenn Forschende SLC26A3 bewusst senken, bilden Tumorzellen mehr Sphären (ein Kennzeichen von Stammzelligkeit), erneuern sich effizienter, dringen durch künstliche Membranen ein und wandern schneller über Scratch-Assays. Sie werden außerdem weniger empfindlich gegenüber gängigen Chemotherapeutika wie Oxaliplatin und 5‑Fluorouracil. Umgekehrt reduziert eine Erhöhung von SLC26A3 Stammzellmarker und verlangsamt Invasion und Migration — dieser Nutzen wird jedoch abgeschwächt, wenn zusätzlich Lactat zugeführt wird, was verdeutlicht, wie Azidität den Schutzmechanismus außer Kraft setzen kann.
Eine verborgene Verbindung zur Genkontrolle
Über die pH-Regulation hinaus dient SLC26A3 auch als Gerüst, das zwei RNA-bindende Proteine, HuR und CUGBP1, bindet. Diese Proteine steuern die Lebensdauer vieler mRNAs, die für krebsrelevante Proteine kodieren. Wenn SLC26A3 reichlich vorhanden ist, sequestriert es einen Teil von HuR und CUGBP1 und begrenzt damit deren Fähigkeit, bestimmte Krebs-assoziierte Botschaften zu stabilisieren oder zu destabilisieren. Geht SLC26A3 durch Lactylierung und Abbau verloren, sind HuR und CUGBP1 freier, onkogene mRNAs zu binden, die Stammzelligkeit, epithelial-mesenchymale Transition (EMT), Invasion und Überleben fördern. Experimente zeigen, dass HuR mRNAs für Stammzellmarker und Zellverbindungsproteine stabilisiert, während CUGBP1 bei einigen Zielen HuR entgegenwirken kann, die Integrität von Verbindungen reduziert und EMT fördert — beides begünstigt Tumorausbreitung.
Das Milieu wieder ins Gleichgewicht bringen, um Krebs zu bekämpfen
Um zu prüfen, ob sich diese Erkenntnisse therapeutisch nutzen lassen, verwenden die Forschenden Mausmodelle des kolorektalen Karzinoms. Die Neutralisierung der Tumorazidität mit Natriumbicarbonat, die Blockade des Lactattransports mit einem MCT1-Inhibitor oder die Überexpression von SLC26A3 verlangsamen alle das Tumorwachstum. Die Kombination der Wiederherstellung von SLC26A3 mit Chemotherapie verkleinert Tumoren weiter. In Patientendaten korrelieren höhere SLC26A3-Werte mit besserem Überleben, weniger Rückfällen, weniger Metastasen und besseren Ansprechen auf Chemotherapie, was darauf hindeutet, dass dieses Protein sowohl als Biomarker als auch als therapeutisches Ziel dienen könnte. 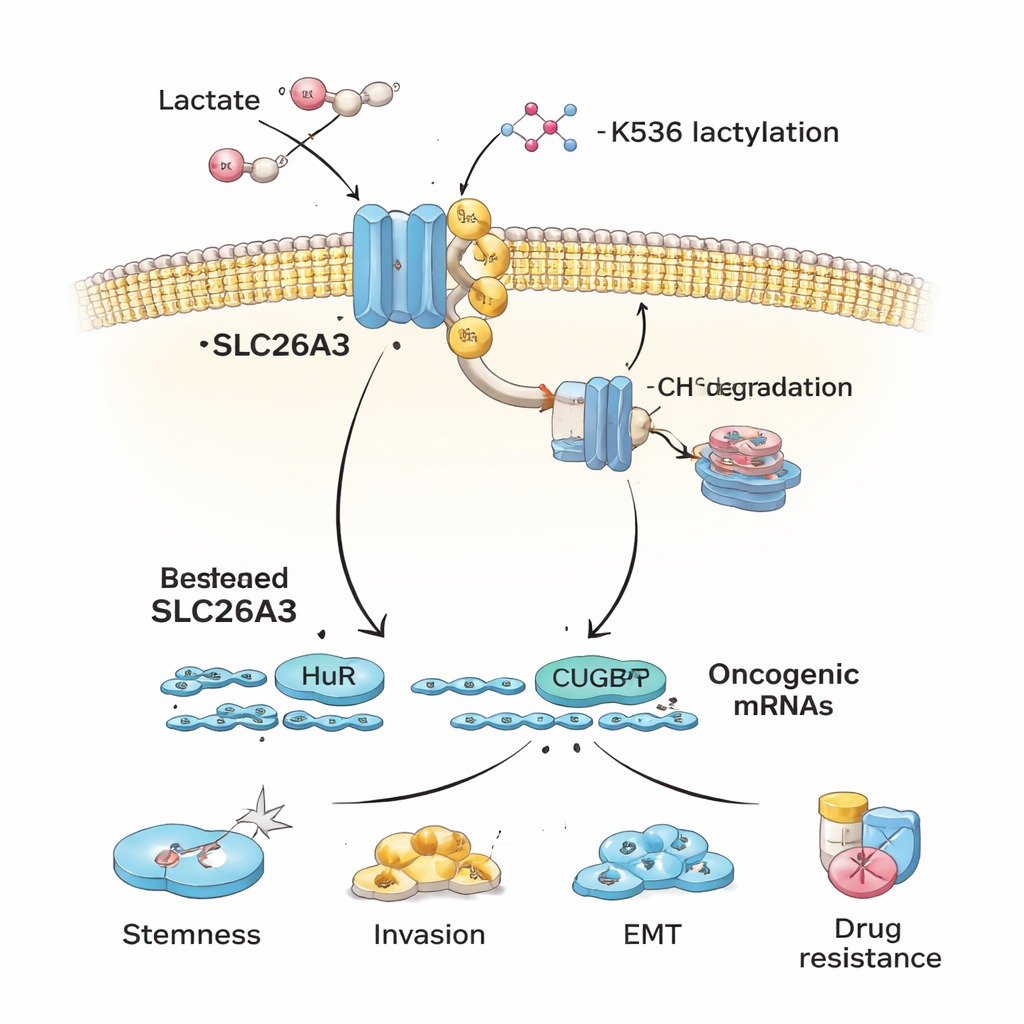
Was das für Patientinnen und Patienten bedeutet
Einfach ausgedrückt zeigt diese Studie, dass kolorektale Tumoren in einem sauren, milchsäurereichen Bad gedeihen, das ein schützendes Torwächterprotein, SLC26A3, chemisch „markiert“ und zerstört. Ist dieser Torwächter weg, nehmen Krebszellen leichter stamzellähnliche Eigenschaften an, breiten sich aus und werden resistent gegen Behandlungen, unterstützt von mächtigen RNA-Regulatoren im Inneren der Zelle. Durch das Puffern der Tumorazidität, die Blockade des Lactatumgangs oder die Wiederherstellung von SLC26A3 könnte man diese maligne Rückkopplungsschleife schwächen und Standardtherapien effektiver machen. Solche Ansätze müssen zwar noch in kontrollierten klinischen Studien geprüft werden, eröffnen aber einen vielversprechenden neuen Blick darauf, wie die Steuerung der chemischen Umgebung des Tumors zur Kontrolle des kolorektalen Krebses beitragen könnte.
Zitation: Chen, C., Cai, D., Liu, X. et al. Lactylation of SLC26A3 in the acidic tumor microenvironment promotes malignant progression of colorectal carcinoma. Cell Death Dis 17, 164 (2026). https://doi.org/10.1038/s41419-026-08422-9
Schlüsselwörter: kolorektales Karzinom, Tumormikromilieu, Lactylierung, Krebsstammzellen, Chemotherapie-Resistenz