Clear Sky Science · de
Die Hemmung von GNG4 stoppt das Tumorwachstum und stellt die Empfindlichkeit gegenüber Enzalutamid bei Prostatakrebs wieder her, indem Autophagie unterdrückt wird
Warum diese Forschung wichtig ist
Bei vielen Männern mit fortgeschrittenem Prostatakrebs wirken starke Hormonblocker wie Enzalutamid anfangs gut, verlieren aber mit der Zeit an Effektivität. Diese Studie enthüllt einen versteckten Überlebensmechanismus von Tumorzellen und benennt ein spezifisches Protein, GNG4, das Tumoren hilft, weiter zu wachsen und Therapien zu widerstehen. Das Verständnis dieses Mechanismus könnte zu Kombinationsbehandlungen führen, die aktuelle Medikamente wirksamer und langlebiger machen.
Ein Proteinschalter, der offen sichtbar ist
Prostatakrebszellen werden stark von Androgenen gesteuert; daher zielt die Standardbehandlung bei fortgeschrittener Erkrankung darauf ab, diese Signale zu unterbinden. Dennoch werden die meisten Tumoren schließlich „kastrationsresistent“ und wachsen wieder. Die Autoren suchten nach Genen, die in Tumorgewebe deutlich stärker exprimiert sind als im benachbarten normalen Prostatagewebe derselben Patienten. Unter mehreren Kandidaten stach GNG4 hervor: Bei Reduktion seines Gehalts in Prostatakrebszellen nahm das Tumorzellwachstum deutlich ab. Analysen von Hunderten Patientenproben bestätigten, dass GNG4 in Primärtumoren höher ist als im Normalgewebe und besonders in aggressiveren, höhergradigen Tumoren ausgeprägt auftritt.
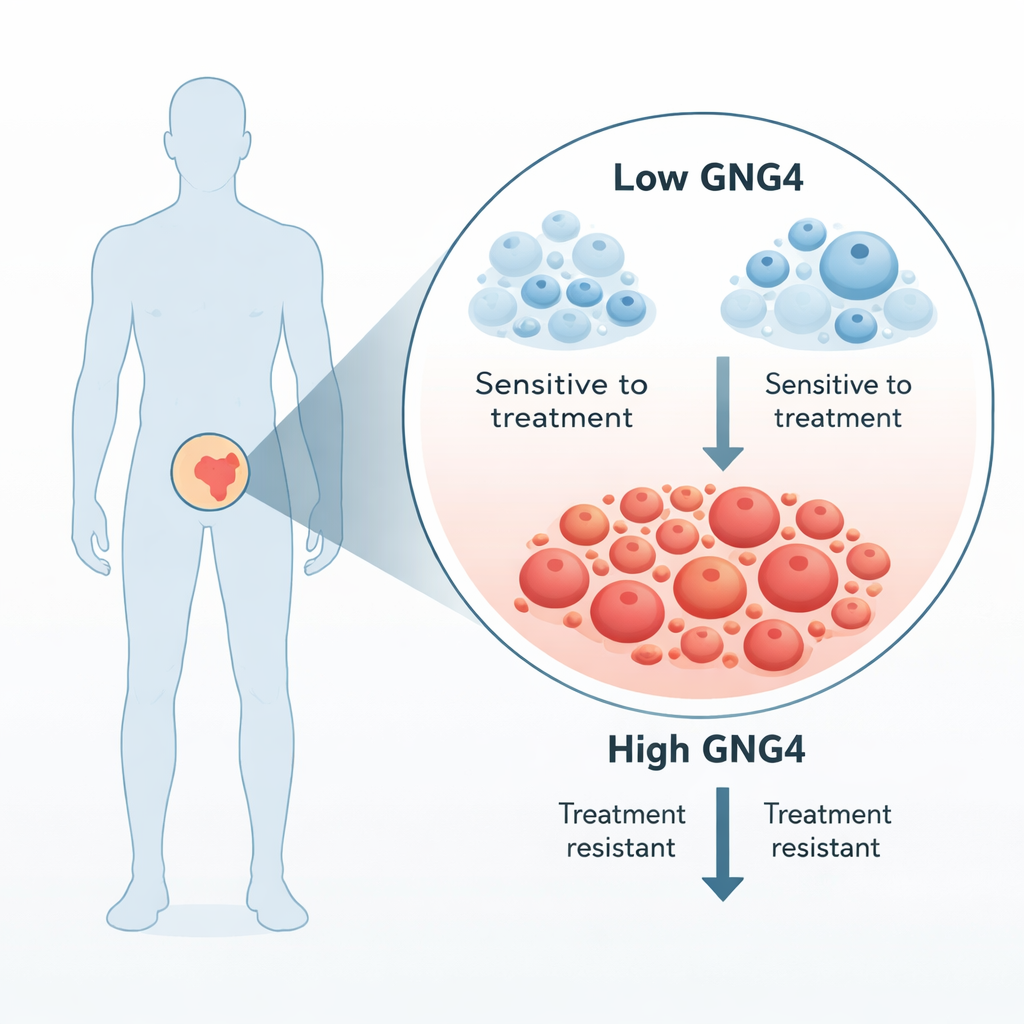
Wie GNG4 Tumoren hilft zu gedeihen
GNG4 gehört zur Familie der G‑Proteine, die an der Zellmembran sitzen und Signale von außen ins Zellinnere weiterleiten. Das Team zeigte, dass das Herunterregeln von GNG4 in Prostatakrebszelllinien die Zellteilung verlangsamte, Zellen in einer Kontrollphase des Zellzyklus verharren ließ und die programmierte Zelltodrate erhöhte. Diese Veränderungen verringerten außerdem die Wanderungsfähigkeit der Krebszellen und ihre Wundverschlusssicherheit in Labortests, und aus GNG4‑armen Zellen gebildete Tumoren wuchsen in Mäusen langsamer. Zusammengenommen deuten diese Befunde darauf hin, dass GNG4 wie ein Gaspedal für Wachstum und Ausbreitung von Prostatakrebs wirkt.
Autophagie: die Notration der Krebszelle
Die Forscher richteten ihr Augenmerk anschließend auf die Autophagie, einen Prozess, bei dem Zellen eigene Bestandteile abbauen und recyceln, um Stress wie Hunger oder medikamentöse Behandlung zu überstehen. In vielen fortgeschrittenen Tumoren dient Autophagie als Notration, die Tumorzellen hilft, widrige Bedingungen zu meistern. In dieser Studie zeigten Prostatakrebszellen mit hoher GNG4‑Aktivität vermehrt Merkmale aktiver Autophagie, während GNG4‑reduzierte Zellen weniger Recyclingstrukturen und niedrigere Spiegel wichtiger Autophagiemarkern aufwiesen. Bei Überexpression von GNG4 vertrugen Zellen Enzalutamid besser und unterlagen seltener dem Zelltod. Die Blockade der Autophagie mit einem chemischen Inhibitor hob diesen Schutz größtenteils auf, was darauf hinweist, dass GNG4 die Behandlungstoleranz maßgeblich durch Hochfahren dieses Recycling‑Systems vermittelt.
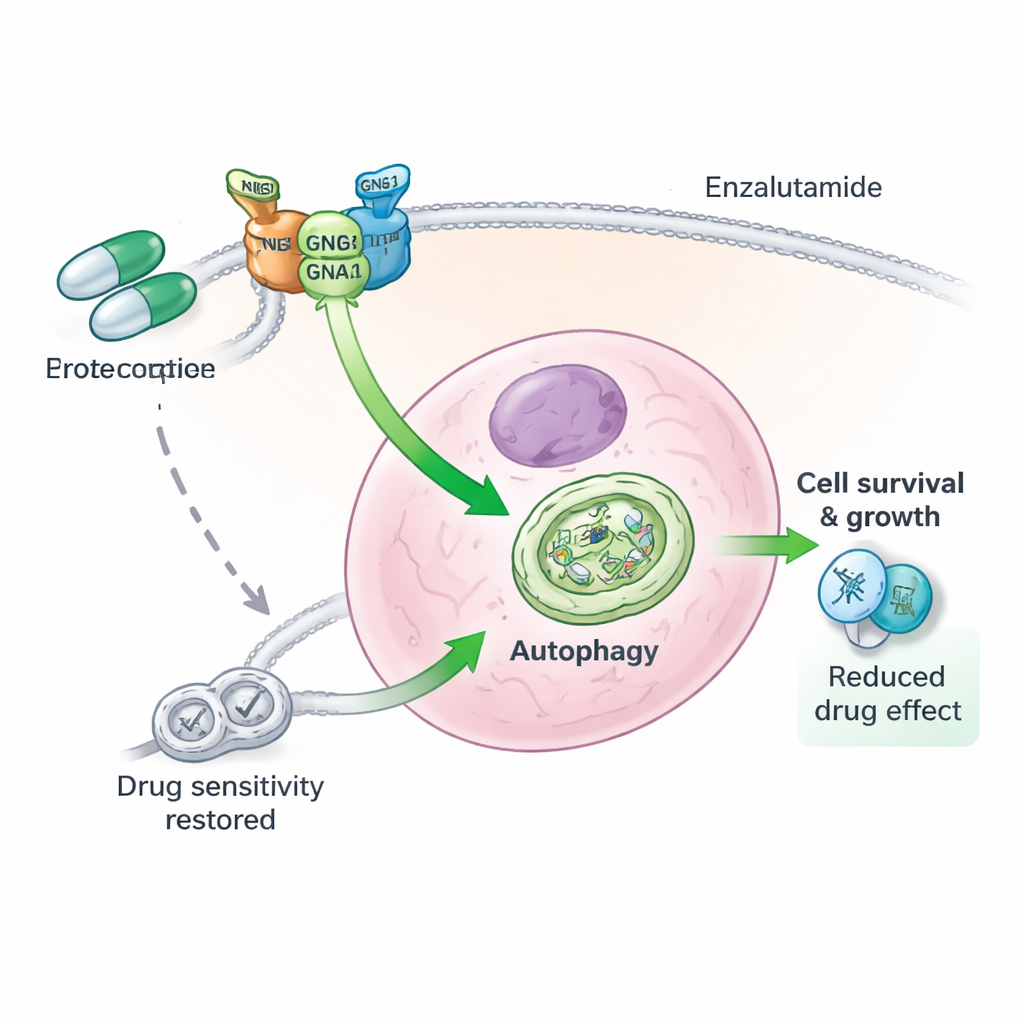
Ein dreiteiliges Proteinteam hinter der Arzneimittelresistenz
Tiefergehende Analysen zeigten, dass GNG4 nicht allein agiert. Es geht eine physische Wechselwirkung mit einer weiteren G‑Protein‑Komponente, GNB1, ein, wodurch ein drittes Protein, GNAI3, stabilisiert wird. Gemeinsam bilden diese drei Untereinheiten einen funktionellen Komplex, der die Autophagie in Prostatakrebszellen verstärkt. Bei Reduktion von GNG4 wurde GNAI3 schneller für den Abbau markiert und durch die zelluläre Entsorgungsmaschinerie abgebaut, wodurch das Autophagiesignal abgeschaltet wurde. Die Entfernung von GNAI3 hob die durch erhöhtes GNG4 verliehenen Wachstums‑ und Überlebensvorteile sowohl in Kulturzellen als auch in Maus‑Tumoren auf. Anders gesagt: GNG4 fördert Malignität und Stressresistenz weitgehend über die Achse GNG4–GNB1–GNAI3.
Aktuelle Medikamente wirksamer machen
Schließlich prüfte das Team, was passiert, wenn die Hemmung von GNG4 mit Enzalutamid kombiniert wird, einem führenden Medikament bei fortgeschrittenem Prostatakrebs. Im Labor machte GNG4‑Knockdown die Krebszellen deutlich empfindlicher gegenüber Enzalutamid und verringerte ihre Fähigkeit, nach der Behandlung Kolonien zu bilden. In Mäusen schrumpften Tumoren mit reduziertem GNG4 stärker unter Enzalutamid als Tumoren mit normalem GNG4‑Spiegel, ohne offensichtliche zusätzliche Toxizität. Die direkte Blockade der Autophagie erzielte ähnliche Verbesserungen. Diese Ergebnisse deuten darauf hin, dass das Eingreifen in die GNG4‑getriebene Autophagie Tumorzellen eine wichtige Stressbewältigungsstrategie entzieht und die bestehende Hormonblockade wirkungsvoller und dauerhafter macht.
Was das für Patienten bedeutet
Für Nicht‑Fachleute lautet die Kernbotschaft: Einige Prostatakrebse überleben Therapien, indem sie ein internes Recycling‑System einschalten, das wie ein Notstromaggregat wirkt. Diese Studie identifiziert GNG4 als zentralen Schalter, der dieses System aktiviert und zusammen mit Partnerproteinen die Krebszellen vor Enzalutamid schützt. Durch das Ausschalten dieses Schalters — entweder durch direkte Angriffe auf GNG4 oder durch eine sichere Abschwächung der Autophagie — könnten künftige Therapien das Tumorwachstum verlangsamen und die Medikamentenempfindlichkeit bei Männern wiederherstellen, deren Tumoren schwer zu behandeln geworden sind.
Zitation: Chen, L., Zhang, J., Hu, Y. et al. Targeting GNG4 inhibits tumor progression and restores enzalutamide sensitivity in prostate cancer by suppressing autophagy. Cell Death Dis 17, 160 (2026). https://doi.org/10.1038/s41419-026-08421-w
Schlüsselwörter: Prostatakrebs, Arzneimittelresistenz, Autophagie, G‑Proteine, Enzalutamid