Clear Sky Science · de
Präklinische Profilierung von Antikörper-Wirkstoff-Konjugaten, die auf onkofetales Chondroitinsulfat abzielen
Warum diese Forschung für die künftige Krebstherapie wichtig ist
Krebsmedikamente wirken oft wie Flächenbombardements: Sie treffen schnell teilende Zellen im ganzen Körper, nicht nur Tumorzellen, verursachen starke Nebenwirkungen und erreichen manchmal nicht alle Krebszellen. Diese Studie untersucht einen intelligenteren Ansatz, der die Präzision von Antikörpern mit der Wirksamkeit von Chemotherapie kombiniert und auf eine Struktur abzielt, die in Tumoren weit verbreitet, in gesunden Geweben jedoch kaum vorhanden ist. Für Laien bietet sie einen Einblick, wie künftige Krebstherapien gleichermaßen effektiver und weniger schädlich sein könnten.
Ein spezielles, nur im Krebs vorkommendes "Flagg" im Tumorgewebe
Die Forscher konzentrieren sich auf ein Molekül namens onkofetales Chondroitinsulfat, kurz ofCS. Dabei handelt es sich um eine zuckerartige Hülle, die während der fetalen Entwicklung auftaucht, in den meisten gesunden erwachsenen Geweben verschwindet und in vielen Krebserkrankungen wieder auftritt. Sie findet sich nicht nur auf den Krebszellen selbst, sondern auch im umgebenden Tumorgerüst und in den Stütz- und Kommerzellen des Tumors. Das macht sie zu einem besonders attraktiven Ziel: Die Bekämpfung von ofCS könnte bedeuten, sowohl den Tumor als auch seinen "Boden" zu treffen und dabei normale Organe weitgehend zu schonen. Das Team entdeckte zuvor ein Antikörperfragment namens Vartumab, das ofCS in einer großen Bandbreite solider Tumoren erkennt und nur sehr geringe Bindung an normales Gewebe zeigt.
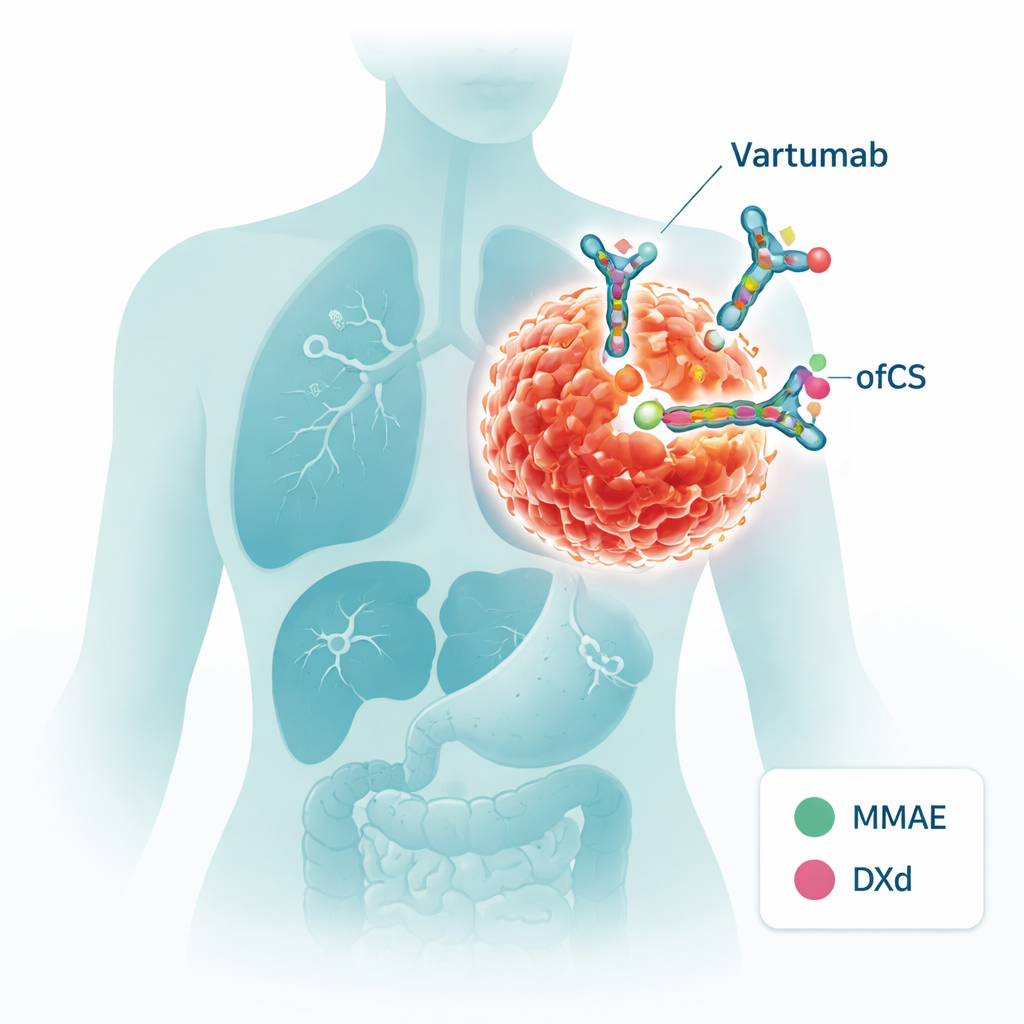
Entwurf einer gelenkten Rakete gegen Tumoren
In dieser Arbeit wird Vartumab in ein Antikörper–Wirkstoff-Konjugat (ADC) umgewandelt — im Grunde eine gelenkte Rakete mit einem toxischen Gefechtskopf. Die Wissenschaftler befestigten zwei verschiedene Chemotherapie-Wirkstoffe, MMAE und DXd, jeweils über einen chemischen "Linker", der von Enzymen im Tumorumfeld gespalten werden kann. Wenn Vartumab an ofCS bindet, können diese Linker geschnitten werden und das Medikament genau dort freisetzen, wo es gebraucht wird. Das Team überprüfte sorgfältig, dass die modifizierten Antikörper in blutähnlichen Bedingungen stabil blieben, den Wirkstoff bei Exposition gegenüber tumorassoziierten Enzymen freisetzten und vor allem ofCS genauso gut erkannten wie das ursprüngliche Vartumab.
Krebszellen und ihre Nachbarn treffen
Ein zentrales Merkmal der gewählten Wirkstoffe ist der sogenannte "Bystander-Effekt". Einmal freigesetzt, können MMAE und DXd aus der ersten Zelle, die sie töten, diffundieren und in benachbarte Zellen eindringen, selbst wenn diese Nachbarn das ofCS-Ziel nicht zeigen. Die Forscher testeten dies, indem sie ofCS-positive Melanomzellen mit gentechnisch veränderten ofCS-negativen Zellen mischten. ADCs mit MMAE oder DXd töteten nicht nur die anvisierten Zellen, sondern auch die ofCS-negativen Nachbarn — abhängig davon, wie viele ofCS-positive Zellen vorhanden waren. Im Gegensatz dazu tötete ein Kontroll-ADC mit einem weniger permeablen Wirkstoff (MMAF) nur unmittelbar anvisierte Zellen und erzeugte keinen starken Bystander-Effekt.
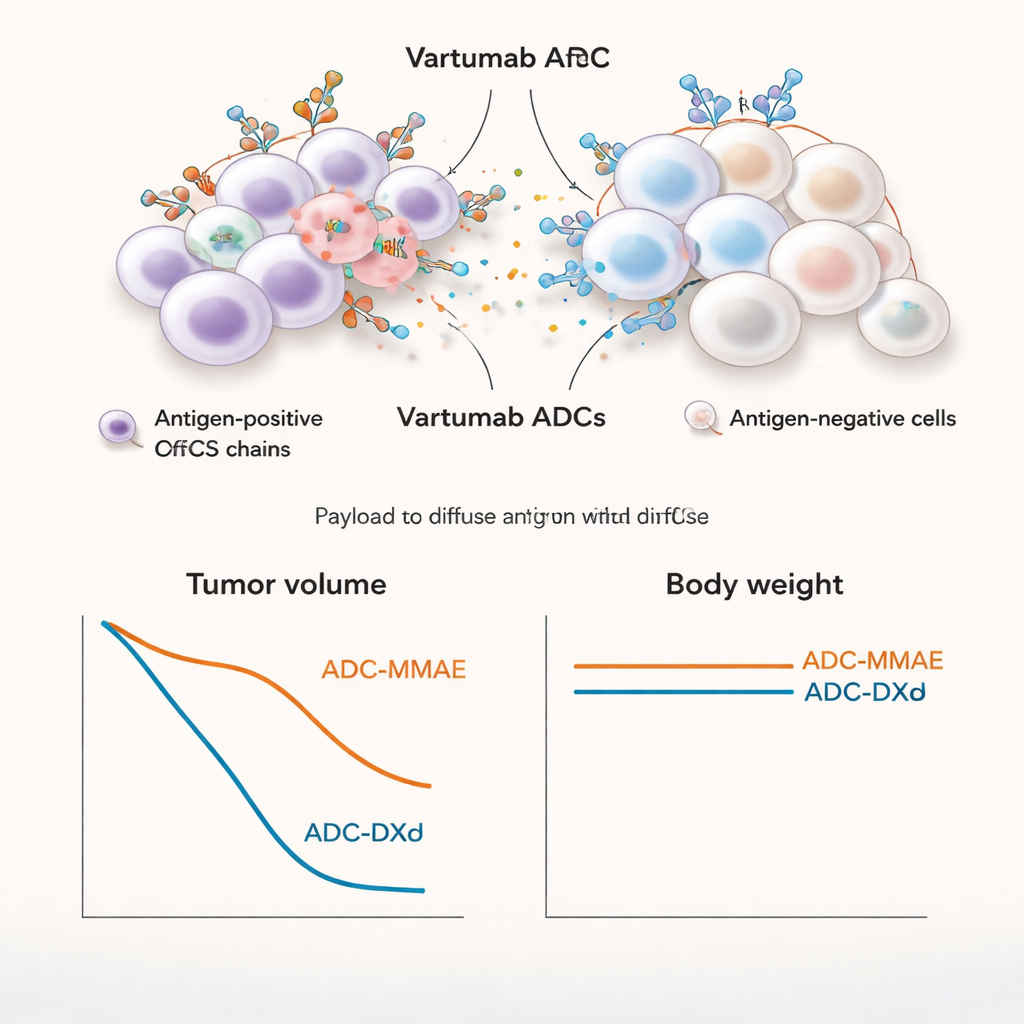
Starke Tumorverkleinerung bei begrenzten Nebenwirkungen außerhalb des Ziels
In Mausmodellen für Melanom und Lungenkrebs reichernten sich die Vartumab-ADCs stark in Tumoren an, während sie in anderen Organen deutlich geringere Werte zeigten. Die MMAE-Variante war besonders wirksam: Bei relativ niedrigen Dosen schrumpfte sie etablierte Tumoren vollständig, auch in einem Lungenkrebsmodell mit geringeren ofCS-Leveln. Auch die DXd-Variante führte zu starker Tumorrückbildung, erforderte aber in der Regel höhere Dosen. Beim Vergleich von MMAE mit dem nicht-bystanderfähigen MMAF in Mäusen erzielte nur das bystander-fähige MMAE-ADC eine vollständige und dauerhafte Tumorbeseitigung, was die Bedeutung der Eliminierung sowohl von Krebszellen als auch von unterstützenden stromalen Zellen unterstreicht. Bei Ratten war wiederholte Gabe des MMAE-ADCs bis zu 5 mg/kg gut verträglich; Gewicht, Blutwerte und Gewebeuntersuchungen zeigten nur milde, reversible Veränderungen, ähnlich den bekannten Effekten verwandter zugelassener Medikamente.
Was das für Patientinnen und Patienten bedeuten könnte
Für Nicht-Spezialisten lautet die Botschaft, dass diese Studie eine vielversprechende "suchen-und-vernichten"-Strategie im Krebs weiter verfeinert. Indem sie sich auf ofCS konzentriert — einen Marker, der in Tumoren weit verbreitet, in normalen Geweben aber selten ist — und Wirkstoffe verwendet, die auf benachbarte Zellen übergreifen können, greifen die Vartumab-ADCs nicht nur die sichtbare Tumormasse an, sondern auch deren unterstützende Umgebung und versteckte Krebszellen, die sonst entkommen könnten. Die Arbeit ist noch präklinisch, legt jedoch einen Weg zu künftigen Medikamenten nahe, die stärker tumorfokussiert sind, über viele Krebsarten hinweg wirken und einige der schwerwiegendsten Nebenwirkungen konventioneller Chemotherapie vermeiden könnten.
Zitation: Skafte, A., Vidal-Calvo, E.E., Choudhary, S. et al. Preclinical profiling of antibody drug conjugates targeting oncofetal chondroitin sulfate. Cell Death Dis 17, 162 (2026). https://doi.org/10.1038/s41419-026-08420-x
Schlüsselwörter: Antikörper-Wirkstoff-Konjugate, onkofetales Chondroitinsulfat, Nebeneffekt (Bystander-Effekt), zielgerichtete Krebstherapie, Tumormikroumgebung