Clear Sky Science · de
DNA-PKcs orchestriert durch CTLA‑4‑Verlust ausgelöste Seneszenz in Krebszellen
Den Wachstums-Schalter von Krebs in ein Stoppsignal verwandeln
Immunbasierte Krebstherapien richten sich häufig gegen ein Molekül namens CTLA‑4, das auf Immunzellen vorkommt, um dem Körper zu helfen, Tumore anzugreifen. Diese Studie offenbart eine überraschende Wendung: CTLA‑4 kommt auch innerhalb von Krebszellen selbst vor und kann dort wie ein versteckter Wachstumspartner wirken. Entfernten die Wissenschaftler dieses intrazelluläre CTLA‑4 gezielt aus Melanomzellen, stellten die Krebszellen die Vermehrung ein und glitten in einen langfristigen „Ruhestand“zustand, bekannt als zelluläre Seneszenz. Das Verständnis dieser unerwarteten Rolle eröffnet neue Wege, Tumore zu verlangsamen oder sogar zu verkleinern, indem CTLA‑4 in Krebszellen gezielt angegangen wird, nicht nur auf Immunzellen.
Wenn Zellen den Ruhestand dem unkontrollierten Wachstum vorziehen
Zellen teilen sich normalerweise, reparieren Schäden und – wenn Schäden zu schwerwiegend sind – sterben sie oder treten in die Seneszenz ein, einen dauerhaften Stopp ihres Wachstums. Seneszente Zellen vergrößern sich typischerweise, verändern ihre Form und produzieren bestimmte Marker, die Forscher im Labor nachweisen können. Die Forschenden fanden heraus, dass das Reduzieren von CTLA‑4 in Maus‑ und menschlichen Melanomzellen dazu führte, dass die Zellen größer wurden, ihr Wachstum stark abnahm und klassische Seneszenzzeichen zunahmen, einschließlich enzymatischer Aktivität, die durch spezielle Färbetests erkennbar ist, sowie Proteinen wie p16 und p21, die den Zellzyklus blockieren. Diese Veränderungen traten sowohl bei vorübergehender Stilllegung von CTLA‑4 als auch bei permanentem Ausschalten mittels Geneditierung auf.
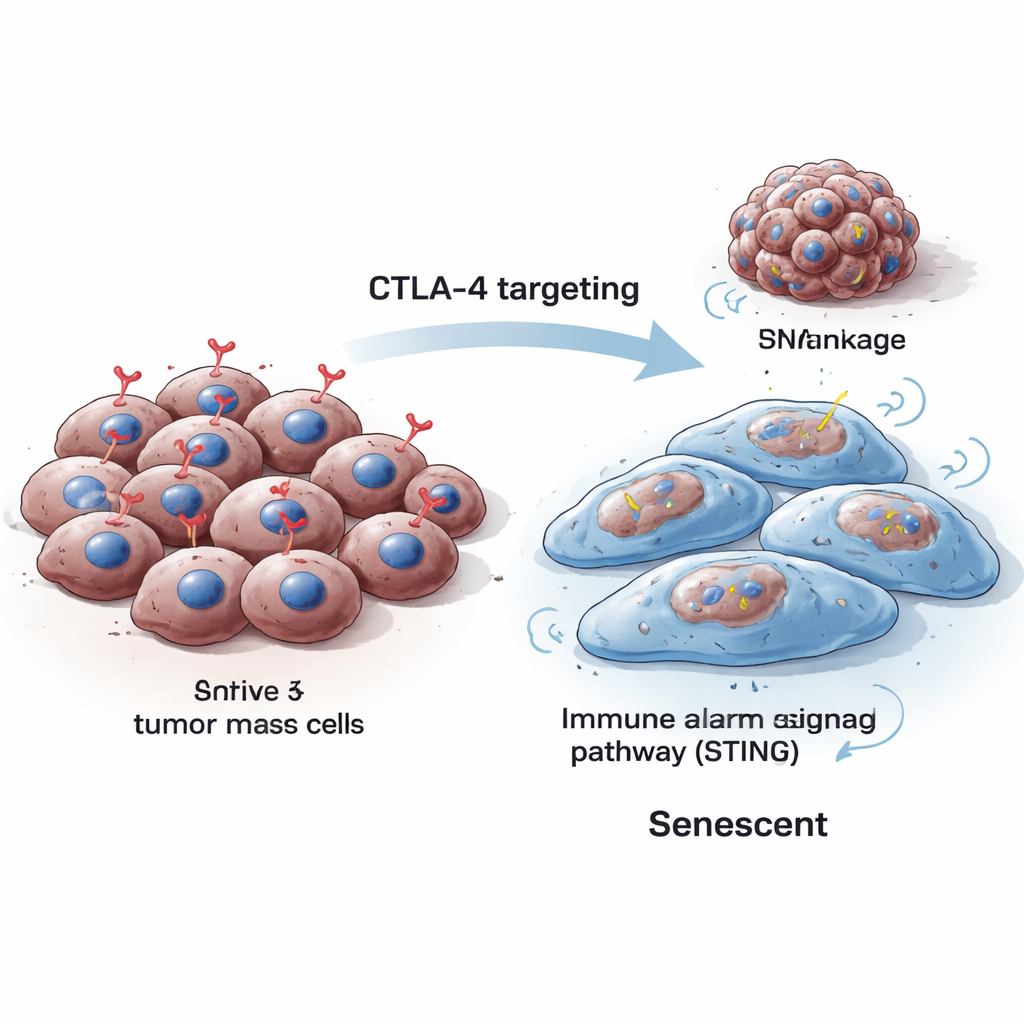
Risse im genetischen Bauplan führen zu einem Stillstand
Um zu verstehen, warum der Verlust von CTLA‑4 Krebszellen in die Seneszenz treibt, untersuchte das Team, wie diese Zellen mit ihrer DNA bei der Teilung umgehen. Sie entdeckten, dass CTLA‑4‑Mangel die Spiegel von Aurora B verringerte, einem Protein, das hilft, Chromosomen bei der Zellteilung sauber zu trennen. Fiel Aurora B ab, entwickelten die Zellen genomische Instabilität: kleine, zusätzliche DNA‑haltige Körperchen, sogenannte Mikronuklei, traten auf, und Marker für DNA‑Schäden nahmen zu. Diese Form von DNA‑Stress ist dafür bekannt, Zellen eher in die Seneszenz als in unkontrolliertes Wachstum zu treiben. Wichtig war, dass die Wiederherstellung von Aurora B die Zahl der Mikronuklei verringerte und damit den Verlust von CTLA‑4 direkt mit fehlerhafter Chromosomenhandhabung und DNA‑Schäden verband.
DNA‑Schäden lösen ein internes Alarmsystem aus
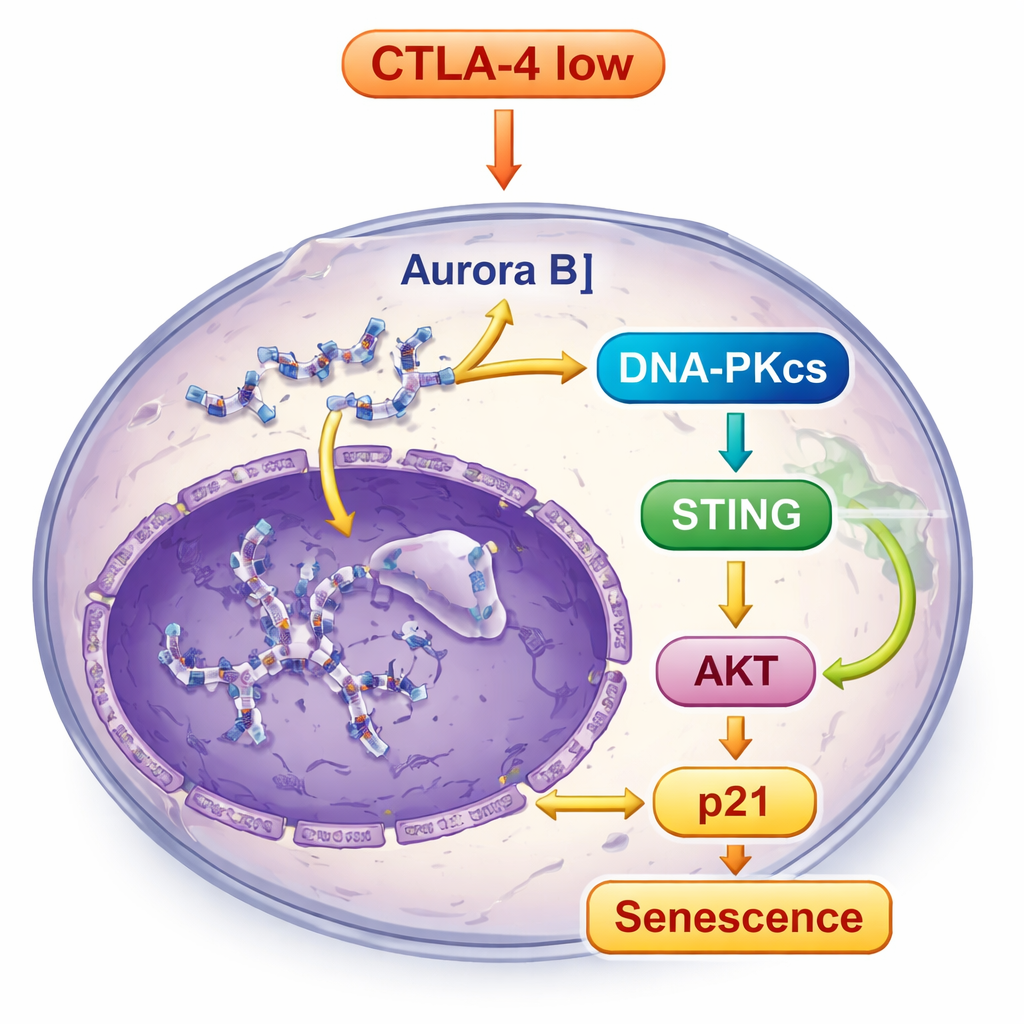
Die beschädigte und fehlplatzierte DNA in CTLA‑4‑armen Zellen blieb nicht unbemerkt. Sie aktivierte DNA‑PKcs, einen Sensor für DNA‑Schäden, der wiederum den STING‑Signalweg auslöste, ein eingebautes Alarmsystem, das auf fehlplatzierte DNA in Zellen reagiert. Sobald STING eingeschaltet war, signalisierte es an nachgeschaltete Moleküle wie TBK1 und IRF3 und aktivierte außerdem einen weiteren wichtigen Wachstumsregelungsweg, die AKT‑Signalgebung. Anstatt Wachstum zu fördern, erhöhte diese kombinierte Signalgebung letztlich p21, eine starke Bremse des Zellzyklus, und verstärkte so den seneszenten Zustand. Blockierten die Wissenschaftler DNA‑PKcs, wurden die STING‑Aktivierung und die Seneszenzmerkmale deutlich reduziert, was zeigt, dass DNA‑PKcs im Zentrum dieser Alarmkaskade steht.
Von der Zellkultur zu Tumoren in lebenden Tieren
Laboransätze erzählen nur einen Teil der Geschichte, daher prüften die Forschenden, ob der Verlust von CTLA‑4 echte Tumore in Mäusen beeinflusst. Sie setzten Melanomzellen mit oder ohne CTLA‑4 auf gegenüberliegenden Seiten derselben Tiere ein. Tumore ohne CTLA‑4 wuchsen langsamer, wogen weniger und hatten ein geringeres Volumen als ihre CTLA‑4‑haltigen Gegenstücke. Diese CTLA‑4‑defizienten Tumore zeigten zudem stärkere Seneszenzfärbung und höhere Werte für DNA‑Schäden sowie Aktivierung des STING‑Signalwegs. Die Analyse von Patientendaten aus großen öffentlichen Datenbanken unterstützte den Zusammenhang zusätzlich: In mehreren Krebsarten zeigte die CTLA‑4‑Expression tendenziell eine inverse Beziehung zu DNA‑PKcs und anderen Komponenten der DNA‑Reparatur, was die Laborbefunde auf menschliche Erkrankungen überträgt.
Was das für künftige Krebstherapien bedeutet
Insgesamt zeigt die Studie, dass CTLA‑4 innerhalb von Krebszellen ihnen hilft, genetische Stabilität zu bewahren und weiter zu proliferieren. Wird CTLA‑4 entfernt, werden Chromosomen instabil, DNA‑Brüche häufen sich, und ein internes Alarmsystem – zentriert auf DNA‑PKcs und STING – treibt die Zellen in einen dauerhaften Wachstumsstopp. Für Laien bedeutet dies: Das Abschalten von CTLA‑4 in Tumorzellen schiebt Krebszellen weg von gefährlich schnellem Wachstum hin zu einem sichereren „Ruhestand“-Zustand. Diese Erkenntnisse legen nahe, dass künftige Krebsbehandlungen nicht nur darauf abzielen sollten, das Immunsystem durch Blockade von CTLA‑4 auf Immunzellen zu entfesseln, sondern auch Tumore direkt zu entwaffnen, indem CTLA‑4 in Krebszellen gezielt angegangen und die Seneszenz als eingebauter Bremsmechanismus genutzt wird.
Zitation: Lee, JJ., Rhee, W.J., Kim, S.Y. et al. DNA-PKcs orchestrates CTLA-4 depletion-induced senescence in cancer cells. Cell Death Dis 17, 204 (2026). https://doi.org/10.1038/s41419-026-08419-4
Schlüsselwörter: zelluläre Seneszenz, Melanom, CTLA‑4, DNA‑Schäden, STING‑Signalweg