Clear Sky Science · de
Cytoplasma‑Nukleus‑Shuttling von TET2: eine intrinsische Bremse beim Fortschreiten kolorektaler Karzinome
Wie Krebszellen ihre eigene Bremse mit sich führen
Kolorektales Karzinom gehört zu den weltweit häufigsten Krebsarten und wird oft dann lebensbedrohlich, wenn Tumorzellen lernen, umliegendes Gewebe zu durchdringen und in andere Organe zu streuen. Diese Studie zeigt, dass viele dieser Krebszellen tatsächlich ein internes „Bremssystem“ mit sich tragen — ein Protein namens TET2 — das ihr Voranschreiten verlangsamen kann, wenn es in den Zellkern gelangt. Zu verstehen, wie diese eingebaute Bremse an- und ausgeschaltet wird, könnte neue Wege eröffnen, das Tumorwachstum zu bremsen, statt ausschließlich zu versuchen, Krebszellen direkt abzutöten.
Beobachtung eines Schlüsselproteins innerhalb von Tumorzellen
Die Forschenden konzentrierten sich auf TET2, ein Protein, das hilft zu steuern, welche Gene an- oder abgeschaltet sind, indem es bestimmte chemische Markierungen in der DNA entfernt. In Gewebeproben von Hunderten von Patientinnen und Patienten mit kolorektalem Karzinom verfolgten sie, wo TET2 in den Tumorzellen lokalisiert ist. Sie fanden vier Hauptmuster: überwiegend im Zellkern, überwiegend im Zytoplasma oder stark zugunsten des einen bzw. des anderen Ortes. Patientinnen und Patienten, deren Tumoren mehr TET2 im Zellkern aufwiesen, lebten tendenziell länger, während diejenigen, deren Tumoren TET2 hauptsächlich im Zytoplasma hielten, schlechter abschnitten. Mit dem Fortschreiten der Krankheit zu späteren klinischen Stadien wurde nukleares TET2 seltener, was darauf hindeutet, dass der Verlust dieses nuklearen Schutzes Teil der Verwandlung zu aggressiveren Tumoren ist.
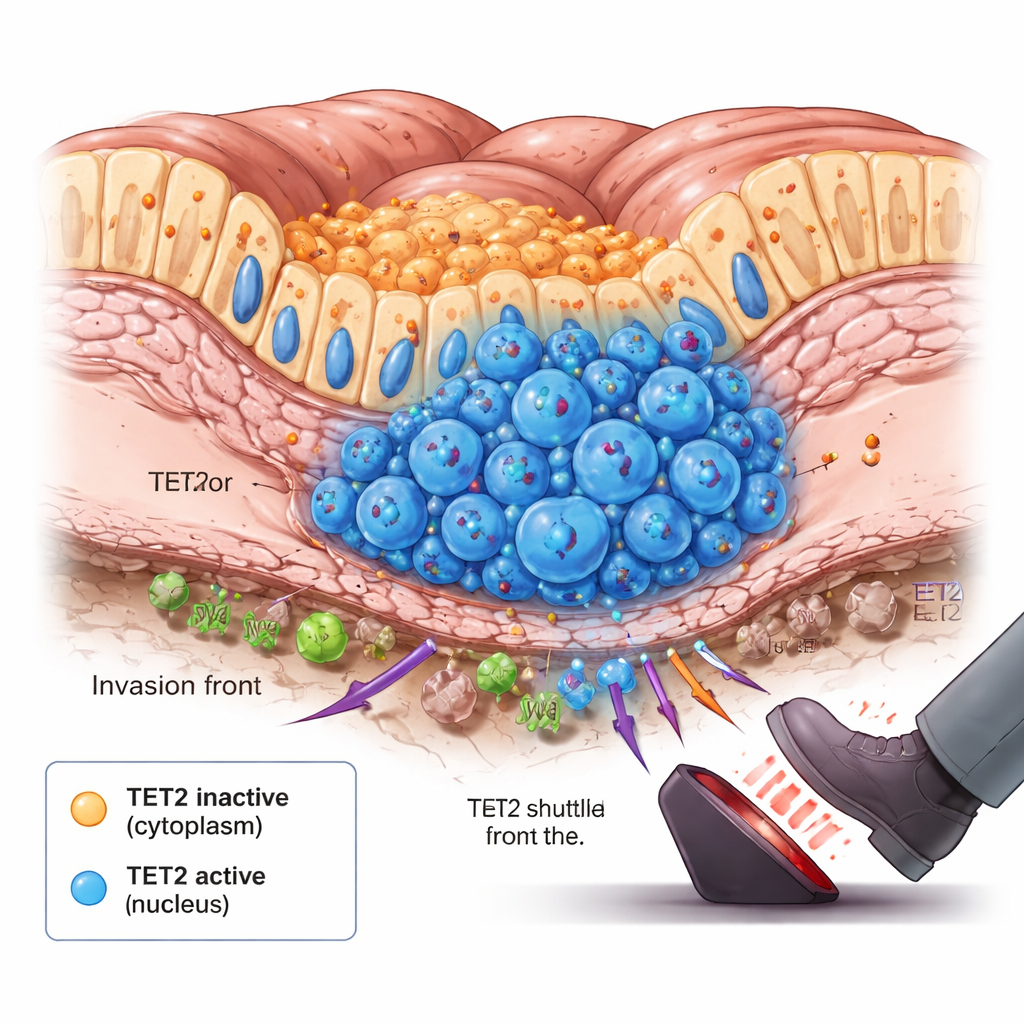
Die Frontlinie des Tumors und der Moment des Umschwungs
Bei genauerer Analyse fiel dem Team etwas Überraschendes auf: In Tumoren, die gerade zu streuen begannen, gab es einen leichten Anstieg an Zellen, in denen TET2 in den Zellkern umgesetzt war. Diese Zellen gruppierten sich an der Basis der Darmschleimhaut, an der Invasionsfront, wo Krebszellen zuerst in tieferes Gewebe vorstoßen. Tierversuche und Langzeitzellkulturmodelle, die Tumorwachstum nachahmen, zeigten über die Zeit ein ähnliches Muster. Anfangs blieb TET2 im Zytoplasma und war weitgehend inaktiv. Mit dem Wachstum der Tumoren und der damit einhergehenden Mangelversorgung innerer Regionen mit Sauerstoff und Nährstoffen lösten Signale in den Zellen das Shuttling von TET2 in den Zellkern bei spezifischen Subpopulationen aus. Einmal dort begann TET2, DNA‑Methylierungsmarken zu entfernen und das Tumorwachstum zu verlangsamen — es wirkte wie eine Notbremsung, wenn der Krebs eine kritische Schwelle überschritt.
Wenn „Vorwärts“-Signale auch eine Bremse auslösen
Kolorektale Tumoren stützen sich oft auf zwei starke „Vorwärts“-Programme: den Gestaltwandelprozess epithelial–mesenchymale Transition (EMT), der Zellen beweglicher und invasiver macht, und den WNT‑Signalweg, der Wachstum und Überleben fördert. Diese Wege werden gewöhnlich als durchweg schädlich im Krebs betrachtet. Die Studie zeigt jedoch, dass bei starker Aktivierung von EMT und WNT zugleich TET2 in den Zellkern getrieben wird. Mithilfe von Medikamenten und genetischen Werkzeugen in Zellkulturen demonstrierten die Wissenschaftler, dass das Anstoßen von EMT oder WNT dazu führte, dass mehr Zellen TET2 in ihre Kerne verschoben, während das Blockieren dieser Wege das Gegenteil bewirkte. Einmal im Zellkern dämpfte aktives TET2 anschließend EMT‑ und WNT‑assoziierte Gene, reduzierte Zellmigration und verlangsamte die Proliferation. Mit anderen Worten: Dieselben Signale, die Tumoren beim Wachsen helfen, wecken zugleich eine interne Gegenkraft.
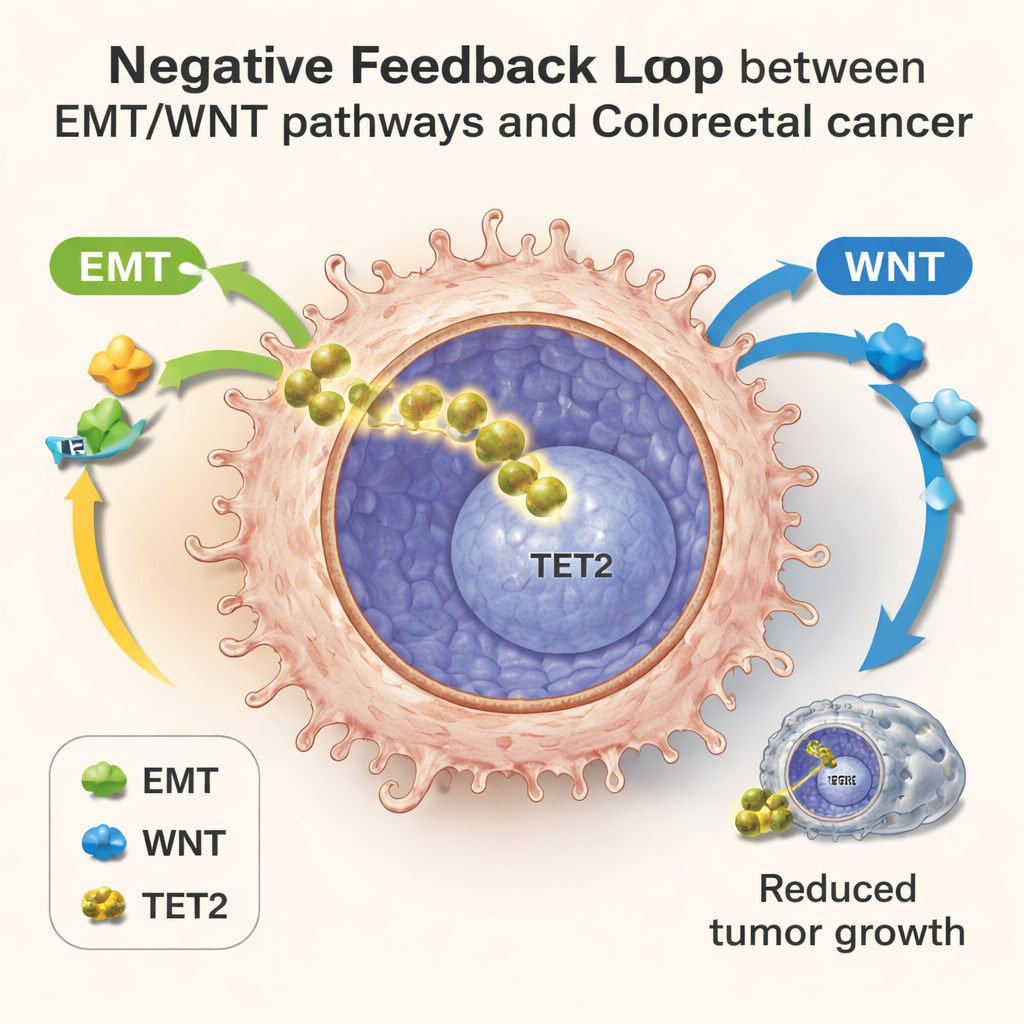
Einzelzellen decken eine verborgene Rückkopplung auf
Um dieses Tauziehen im Detail abzubilden, nutzte das Team Einzelzell‑RNA‑Sequenzierung, die ausliest, welche Gene in Tausenden einzelner Zellen gleichzeitig aktiv sind. In im Labor gezüchteten Kolonien, in Mäusetumoren und in Proben von Patientinnen und Patienten mit kolorektalem Karzinom sahen sie Zellen entlang einer Fortschrittslinie verteilt. Frühe Zellen zeigten normalen Energiestoffwechsel und schwache EMT/WNT‑Aktivität; spätere Zellen wiesen eine Umstellung des Stoffwechsels, starke EMT/WNT‑Signale und anschließend ein Ansteigen der TET2‑Zielgene auf. In diesen späteren Stadien hatten Zellen mit höherer TET2‑Aktivität niedrigere Spiegel invasionsverwandter Gene und standen mit besseren Patientenergebnissen in Verbindung, selbst bei Tumoren, die bereits begonnen hatten zu streuen. Dieses Muster stützt die Idee einer negativen Rückkopplung: Stoffwechselstress und EMT/WNT‑Aktivierung treiben TET2 in den Zellkern, und nukleares TET2 bremst wiederum genau diese aggressiven Programme.
Was das für zukünftige Krebsbehandlungen bedeutet
Für Nichtfachleute lautet die Kernbotschaft, dass das Fortschreiten des kolorektalen Karzinoms kein einfacher „Ein/Aus“-Schalter zwischen gutem und schlechtem Verhalten ist. Stattdessen existiert ein eingebauter, verzögerter Sicherheitsmechanismus: Wenn Tumorzellen invasiver werden, aktivieren sie zugleich TET2 in ihren Zellkernen, was sie teilweise zügelt. Im Laufe der Zeit entkommen viele Tumoren dieser Kontrolle, indem sie nukleares TET2 verlieren oder seine Wirkung überwältigen. Wege zu finden, TET2 im Zellkern zu halten oder seine Aktivität zu steigern — möglicherweise in Kombination mit Medikamenten, die EMT oder WNT modulieren — könnte diese natürliche Bremse stärken und die Ausbreitung des Krebses verlangsamen. Statt Krebszellen nur von außen anzugreifen, könnten künftige Therapien darauf abzielen, dieses interne Kontrollsystem wiederherzustellen und zu verstärken.
Zitation: Li, C., Meng, F., He, J. et al. Cytoplasm-nucleus shuttling of TET2: an intrinsic brake in colorectal cancer progression. Cell Death Dis 17, 163 (2026). https://doi.org/10.1038/s41419-026-08418-5
Schlüsselwörter: kolorektales Karzinom, TET2, Epigenetik, EMT WNT Signalgebung, Krebsvorstreiten