Clear Sky Science · de
Die gezielte Blockade von ENO1 programmiert Makrophagen-Umpolung neu, löst antitumorale Immunität aus und verbessert die therapeutische Wirkung der Strahlentherapie
Vom Tumorschutz zum Ziel
Krebs überlebt nicht nur durch schnelles Wachstum, sondern oft auch dadurch, dass er still die Abwehrkräfte des Körpers lahmlegt. Diese Studie untersucht ein verborgenes Molekül auf Krebszellen, ENO1, das Tumoren hilft, dem Immunsystem zu entkommen und gegen Strahlentherapie resistent zu sein. Durch die Entwicklung eines neuen Antikörperwirkstoffs, der ENO1 anvisiert, zeigen die Forschenden, dass sich die schützenden Chemikalien des Tumors abbauen lassen, Immunzellen reaktiviert werden und Strahlentherapie in Modellen von kolorektalem und triple-negativem Brustkrebs besser wirkt. 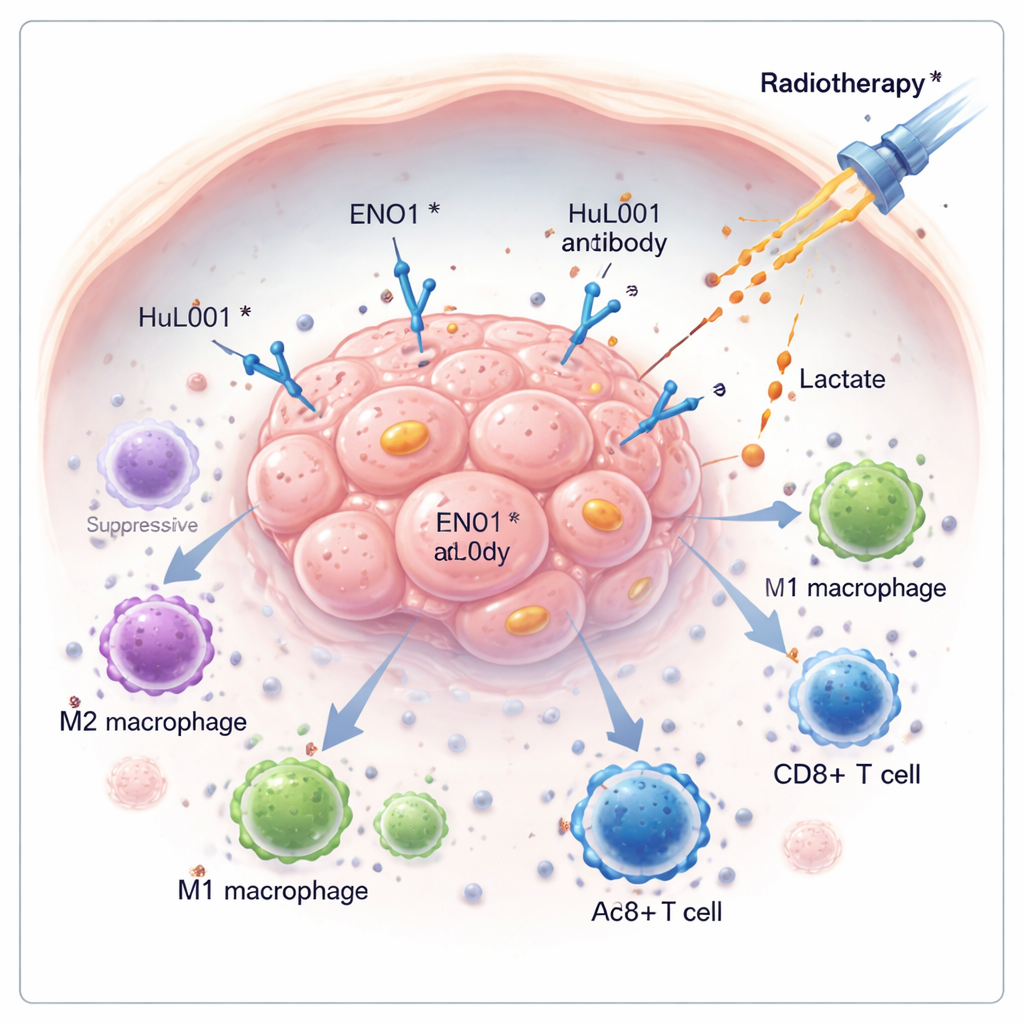
Ein metabolischer Trick, der die Immunität stumm schaltet
Viele Tumoren verändern ihren Energiestoffwechsel und bauen Zucker so ab, dass große Mengen Milchsäure (Laktat) entstehen, selbst wenn Sauerstoff vorhanden ist. Dieses Laktat wird aus den Krebszellen herausgepumpt und reichert sich rund um den Tumor an, wodurch die Umgebung sauer und ungastlich für Immunangriffe wird. In dieser Arbeit konzentrieren sich die Autorinnen und Autoren auf ENO1, ein Enzym des Zuckerabbaus, das auch an der Zelloberfläche von Krebszellen auftauchen kann. Auf der Zelloberfläche bildet ENO1 eine Partnerschaft mit einem Transporter namens MCT4, um Laktat zu exportieren — ein Zustand, der ein wachstumsförderndes, immununterdrückendes Milieu schafft.
Wie Strahlung nach hinten losgehen kann
Strahlentherapie soll die DNA von Tumoren schädigen und Immunantworten auslösen, hat aber auch Nebenwirkungen im Tumormikromilieu. Das Team fand heraus, dass Signale, die von einem Molekül namens TGFβ1 ausgelöst und durch Strahlung verstärkt werden, ein Enzym (PRMT5) aktivieren, das ENO1 chemisch modifiziert und an die Zelloberfläche verlagert. Dort interagiert ENO1 physikalisch mit MCT4, stabilisiert diesen Transporter und fördert den Laktatexport. Erhöhte ENO1-Oberflächenwerte wurden bei Patientinnen und Patienten mit fortgeschrittenem kolorektalem und triple-negativem Brustkrebs gefunden und standen im Zusammenhang mit mehr Metastasen und schlechterem Überleben, was darauf hindeutet, dass Strahlung unbeabsichtigt eine Laktat‑getriebene, immununterdrückende Schutzhülle um Tumoren verstärken kann.
Umprogrammierung von freundlichen und feindlichen Immunzellen
Im sauren Halo um Tumoren werden Immunzellen, sogenannte Makrophagen, in einen „Heiler“-Zustand gedrängt (häufig als M2 bezeichnet), der Tumoren eher hilft, indem er Entzündungen dämpft und Reparaturprozesse fördert, anstatt Krebszellen zu eliminieren. Die Forschenden entwickelten einen humanisierten Antikörper, HuL001, der ENO1 sowohl auf Mäuse- als auch auf menschlichen Krebszellen erkennt. In Zellkultur- und Mausmodellen störte HuL001 die Unterstützung von MCT4 durch ENO1, verringerte die Laktatausschüttung und verschob Makrophagen weg vom tumorfördernden M2‑Phänotyp hin zu einem M1‑Zustand, der aggressiver gegen Krebs ist und Tumorzellen eher aufnimmt. Wichtig ist, dass HuL001 Makrophagen nicht einfach abtötete, sondern sie umprogrammierte und gleichzeitig den Zelltod von Krebszellen direkt erhöhte.
Die Strahlentherapie effektiver machen
Wurde HuL001 in Mausmodellen von kolorektalem und triple-negativem Brustkrebs mit Strahlentherapie kombiniert, schrumpften Tumore stärker, wuchsen langsamer nach und verschwanden in vielen Tieren ganz. 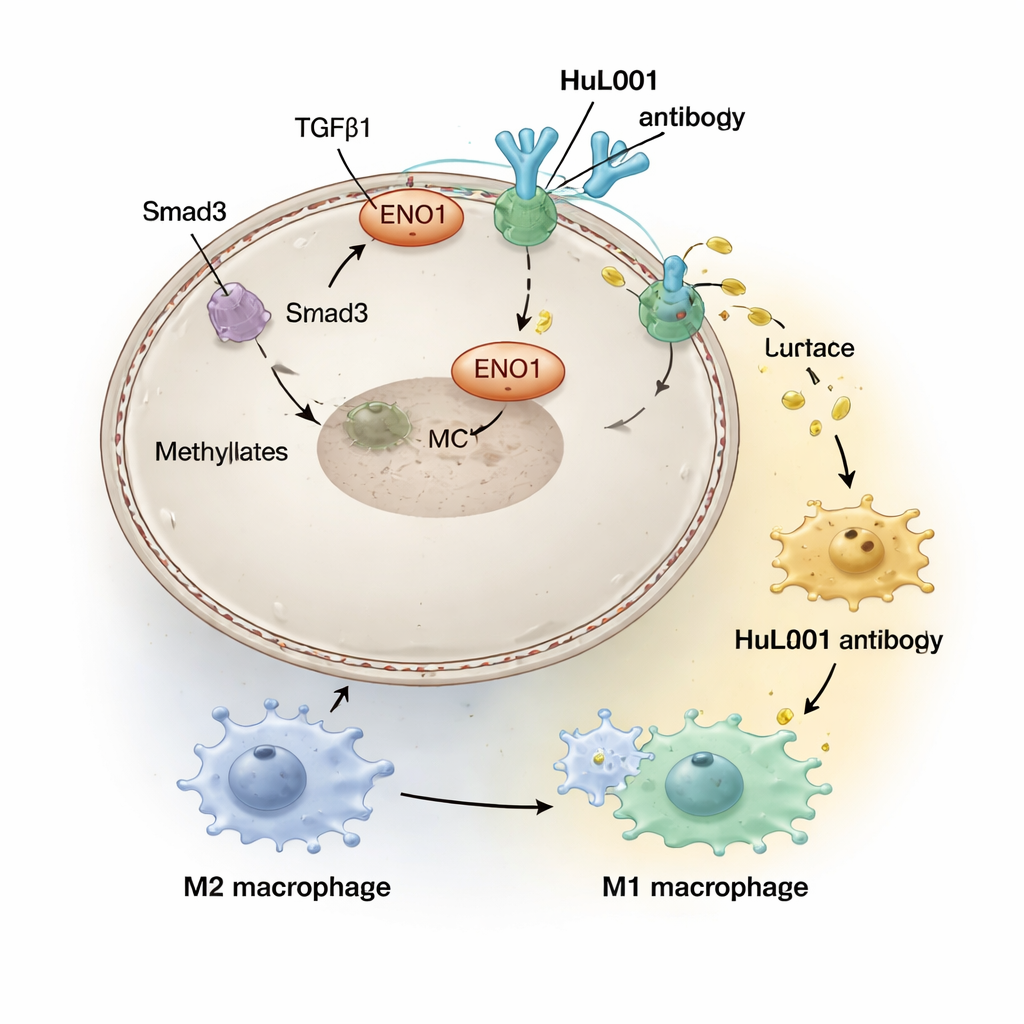
Von komplexen Signalwegen zu praktischer Aussicht
Für Nicht‑Spezialistinnen und Nicht‑Spezialisten lautet die Botschaft dieser Studie, dass die Chemie eines Tumors und seine Nachbarschaft aus Immunzellen tief miteinander verwoben sind. ENO1 steht an einer Schnittstelle: Es hilft Tumoren beim Zuckerstoffwechsel, beim Export von Laktat und beim Anziehen der falschen Art von Immunhilfe. Durch die Blockade von oberflächenlokalisiertem ENO1 mit einem zielgerichteten Antikörper konnten die Forschenden die schädliche Laktatanreicherung verringern, Makrophagen von Tumorhelfern zu Tumorkämpfern umpolen und die Strahlentherapie in schwer zu behandelnden Krebsmodellen wirksamer machen. Obwohl HuL001 noch kein klinisches Medikament ist, deutet die Arbeit darauf hin, dass das Anvisieren metabolischer Torwächter wie ENO1 ein kraftvoller Weg sein könnte, die eigenen Verteidigungsmechanismen des Tumors gegen ihn zu wenden und bestehende Therapien wie die Radiotherapie zu verstärken.
Zitation: Lin, YS., Chang, HY., Hong, WZ. et al. Targeting ENO1 reprograms macrophage polarization to trigger antitumor immunity and improves the therapeutic effect of radiotherapy. Cell Death Dis 17, 194 (2026). https://doi.org/10.1038/s41419-026-08416-7
Schlüsselwörter: Tumorstoffwechsel, Makrophagen-Polarisation, Strahlentherapie, Immuntherapie, Laktat