Clear Sky Science · de
Sec8: ein neuartiger positiver Regulator von RIG-I in der Abwehr gegen RNA‑Viren
Wie unsere Zellen hinterlistige Viren erkennen
Viele gefährliche Viren, darunter Influenza und neu auftretende Tier‑Viren, tragen ihr Erbgut in Form von RNA. Unsere Zellen sind auf innere Alarmsysteme angewiesen, um diese Eindringlinge schnell zu bemerken und eine antivirale Antwort zu starten. Diese Arbeit untersucht ein wenig bekanntes Zellprotein namens Sec8 und zeigt, dass es still und effektiv eine zentrale Rolle dabei spielt, einen unserer wichtigsten Virussensoren, RIG‑I, lange genug am Leben und aktiv zu halten, um uns zu schützen.
Ein zellulärer Alarm unter Bedrohung
RIG‑I ist ein molekularer „Hausalarm“, der das Zellinnere nach Fragmenten viraler RNA absucht. Wenn es verdächtige RNA erkennt, ändert es seine Form, schaltet sich ein und sendet Signale, die schließlich Typ‑I‑Interferone auslösen—starke Warnmoleküle, die benachbarte Zellen resistenter gegen Infektionen machen und Immunabwehr aktivieren. Weil ein überaktiver Alarm schädliche Entzündungen oder Autoimmunität hervorrufen kann, regeln Zellen die RIG‑I‑Spiegel streng. Verschiedene Proteine können RIG‑I mit kleinen Ubiquitinketten markieren und so an den zellulären „Schredder“, das Proteasom, zur Zerstörung schicken. Bisher war unklar, welche zusätzlichen zellulären Faktoren RIG‑I davor schützen, vorzeitig abgebaut zu werden, insbesondere während aktiver RNA‑Virusinfektionen.
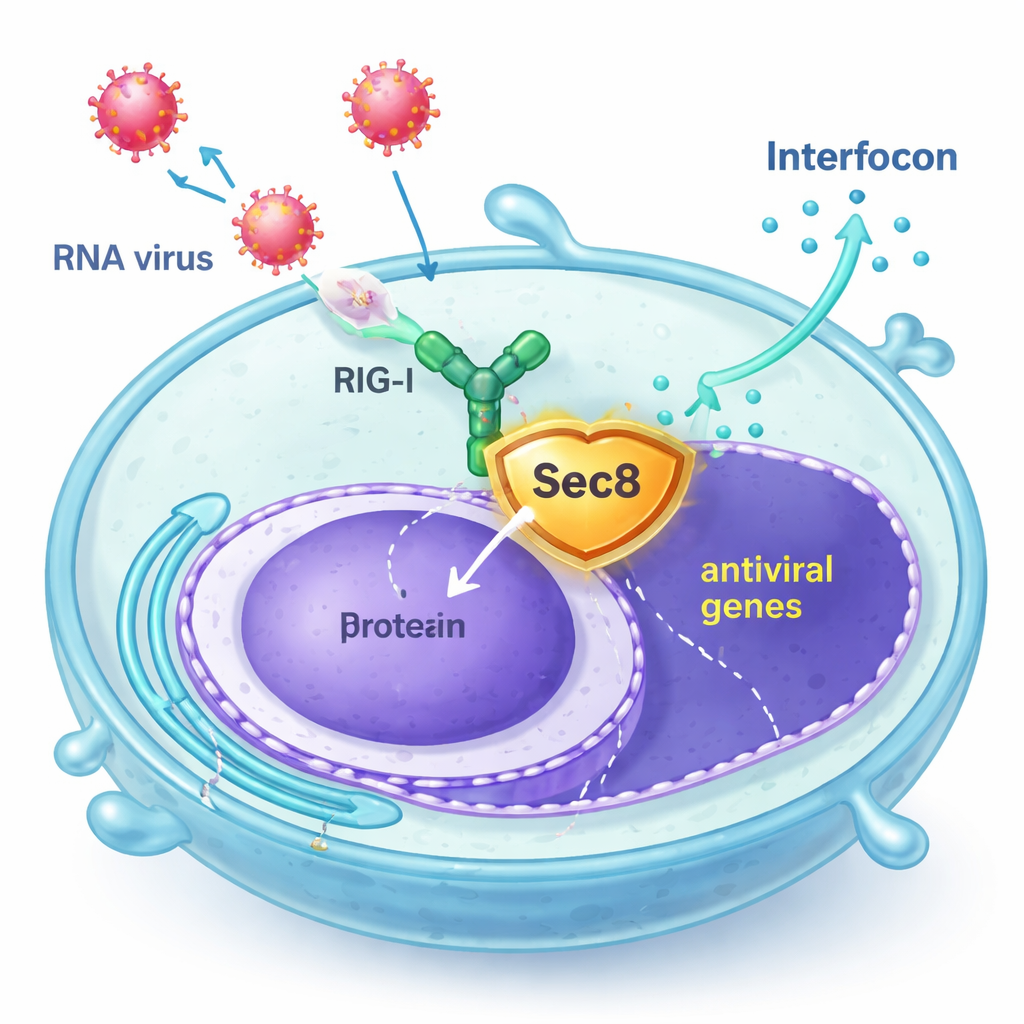
Sec8 tritt als Bodyguard auf
Die Autoren fanden heraus, dass Sec8, bekannt als Teil eines achtgliedrigen Komplexes, der sekretorische Vesikel mit der Zelloberfläche verschmelzen lässt, tatsächlich die antivirale Signalgebung verstärkt. In humanen Zelllinien und in primären Maus‑Immunzellen führte eine Erhöhung der Sec8‑Spiegel nach Infektionen mit RNA‑Viren wie dem vesikulären Stomatitisvirus (VSV) und dem Sendai‑Virus oder nach Exposition gegenüber synthetischer viraler RNA zu einer stärkeren Aktivierung interferon‑verknüpfter Gene. Umgekehrt verringerte die Reduktion von Sec8 die Produktion von Interferon und interferon‑induzierten Genen und machte die Zellen weniger fähig, die Virusvermehrung zu kontrollieren. Diese Befunde legen nahe, dass Sec8 nicht nur in der Sekretion wirkt, sondern als positiver Regulator im antiviralen Alarmweg fungiert.
Den zellulären Schredder blockieren
Bei tiefergehenden Untersuchungen zeigte sich, dass Sec8 die Genexpression von RIG‑I nicht erhöht; stattdessen bewahrt es das RIG‑I‑Protein vor dem Abbau. Wurde Sec8 entfernt, sanken die RIG‑I‑Spiegel schneller, und dieser Verlust ließ sich durch Wirkstoffe verhindern, die das Proteasom blockieren—was die Beteiligung der zellulären Proteinrecycling‑Maschinerie nahelegt. Das Team identifizierte ein weiteres Protein, STUB1, als zentralen „Markierer“, das eine spezifische Art von Ubiquitinkette (K48‑verknüpft) an RIG‑I an der Aminosäure Lysin 190 anbringt. Dieses Zeichen markiert RIG‑I zur Zerstörung. Sec8 stört diesen Prozess auf zwei Wegen: Es konkurriert physisch mit STUB1 um die Bindung an dieselbe Aktivierungsregion von RIG‑I, und es reduziert die Menge an STUB1, die die Zelle überhaupt herstellt.
Sec8, p53 und die Kontrolle des Markierers
Um zu erklären, wie Sec8 die STUB1‑Produktion verringert, richteten die Autoren den Blick auf die Genregulation. Sie identifizierten eine kurze DNA‑Sequenz, die als Kernschalter (Promoter) des STUB1‑Gens fungiert, und zeigten, dass das bekannte Tumorsuppressorprotein p53 an diese Region bindet und STUB1‑Spiegel erhöht. Sec8 dämpft sowohl die Menge als auch die aktivierende Phosphorylierung von p53, sodass p53 STUB1 nicht mehr so effektiv antreiben kann. Wenn p53 blockiert oder STUB1 stillgelegt wurde, hoben sich die schädlichen Effekte eines Sec8‑Verlusts auf die Interferonproduktion und das Virenwachstum weitgehend auf. Das ordnet Sec8 an die Spitze einer Regulationskette ein, die von p53 über STUB1 bis zur Stabilität von RIG‑I reicht.
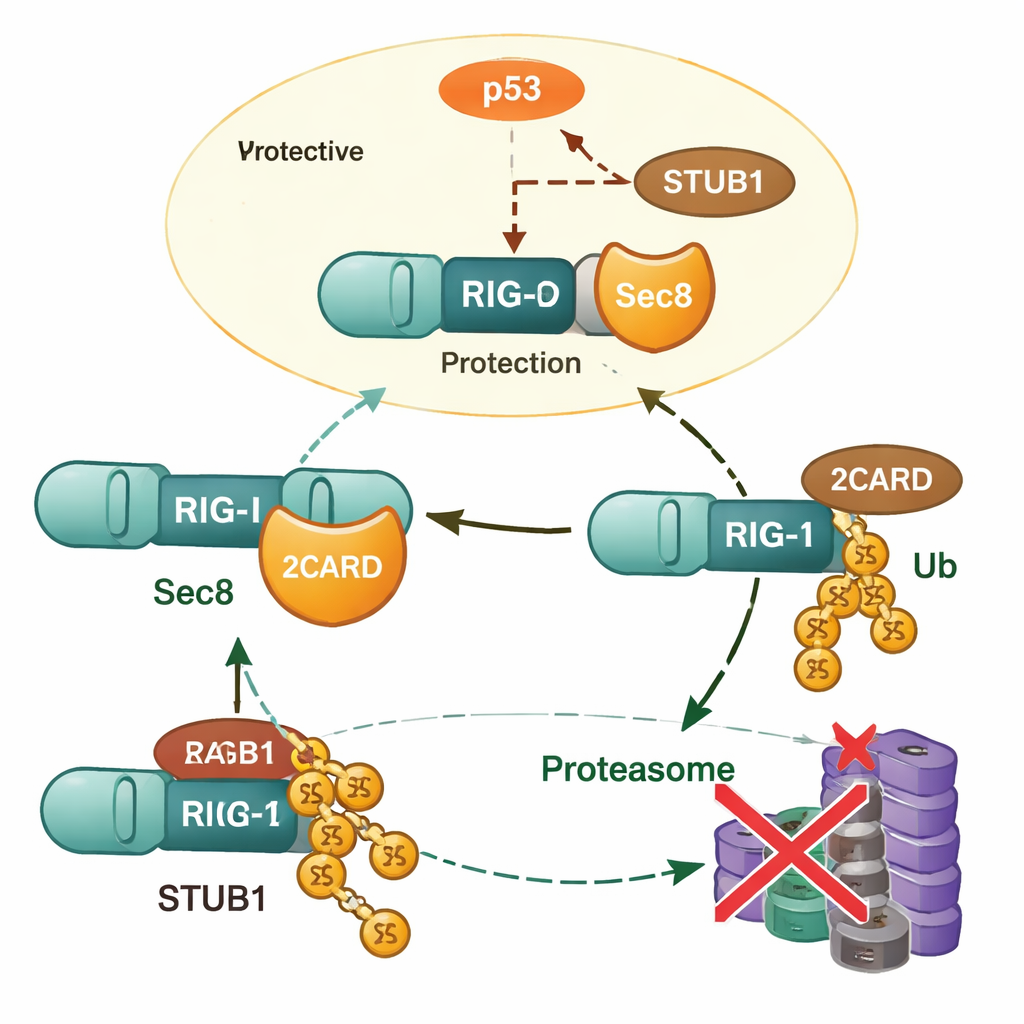
Von der Petrischale zum lebenden Tier
Das Team prüfte anschließend die Bedeutung von Sec8 in Mäusen, bei denen das Sec8‑Gen gezielt in bestimmten Immunzellen entfernt worden war. Nach einer VSV‑Infektion produzierten diese Tiere weniger Interferon, trugen höhere Virusmengen in Organen wie Milz, Leber und Lunge und zeigten stärkere Lungenschäden, größeren Gewichtsverlust und eine niedrigere Überlebensrate als Kontrollmäuse. Diese in vivo‑Ergebnisse bestätigten, dass Sec8 kein unbedeutender Akteur ist, sondern ein wichtiger Schutzfaktor gegen RNA‑Virusinfektionen im ganzen Organismus.
Warum das für zukünftige Therapien wichtig ist
Kurz gesagt zeigt diese Studie, dass Sec8 wie ein Bodyguard für den antiviralen Sensor RIG‑I wirkt. Indem es das „Markierer“-Protein STUB1 in Schach hält und RIG‑I direkt davor schützt, zum zellulären Schredder geschickt zu werden, ermöglicht Sec8 den Zellen, eine zeitnahe Interferonantwort zu entfalten und RNA‑Viren besser zu kontrollieren. Das Verständnis dieser neu beschriebenen p53–STUB1–RIG‑I‑Achse eröffnet Möglichkeiten für zukünftige antivirale Strategien, die RIG‑I stabilisieren oder Sec8s schützende Wirkung nachahmen könnten, und damit unsere Abwehr gegen ein breites Spektrum RNA‑basierter Virusinfektionen stärken.
Zitation: Wang, L., Ma, W., Hou, P. et al. Sec8: a novel positive regulator of RIG-I in anti-RNA viral defense. Cell Death Dis 17, 165 (2026). https://doi.org/10.1038/s41419-026-08414-9
Schlüsselwörter: angeborene Immunität, RNA‑Viren, RIG‑I, Ubiquitinierung, Interferon‑Signalgebung