Clear Sky Science · de
Von MFAP2 abgeleitete krebsassoziierte Fibroblasten (CAFs) fördern die Proliferation und Metastasierung von CRC und unterdrücken zugleich die CD8+-T‑Zell‑vermittelte Antitumor‑Immunität
Warum die Nachbarschaft des Tumors wichtig ist
Das kolorektale Karzinom gehört zu den weltweit häufigsten und tödlichsten Krebsarten, trotzdem fällt es Ärzten weiterhin schwer, seine Ausbreitung zu stoppen und vorherzusagen, welche Patienten eine schlechte Prognose haben werden. Diese Studie betrachtet nicht nur die Krebszellen selbst, sondern auch deren „Nachbarn“ – Stütz‑ und Immunzellen, die denselben Raum teilen. Die Forschenden zeigen, wie ein bestimmter Hilfszelltyp, die krebsassoziierten Fibroblasten, das Tumorwachstum stillschweigend fördern und die körpereigenen krebsbekämpfenden T‑Zellen lahmlegen können. Das Verständnis dieses verborgenen Austauschs könnte neue Behandlungswege eröffnen, die bestehende Therapien wirksamer machen.
Verborgene Helfer in Darmtumoren
Darmtumoren sind nicht einfach Haufen entarteter Zellen; sie sind Mini‑Ökosysteme. Zu den wichtigsten Bewohnern gehören krebsassoziierte Fibroblasten, kurz CAFs. Diese Zellen bilden Bindegewebe, gestalten das Tumorumfeld um und geben Signalstoffe ab. Anhand von Patientenproben und großen Gen‑Datenbanken fanden die Autorinnen und Autoren heraus, dass ein Protein namens MFAP2 in kolorektalen Tumoren deutlich stärker vorhanden ist als im normalen Darmgewebe und dass Patienten mit erhöhten MFAP2‑Werten tendenziell schlechtere Überlebenschancen haben. Sie zeigten, dass MFAP2 in diesen Tumoren vor allem von CAFs und nicht von den Tumorzellen selbst produziert wird. In Zellkulturversuchen und Mausmodellen korrelierten MFAP2‑reiche CAFs eng mit schnellerem Tumorwachstum und aggressiverem Verhalten.
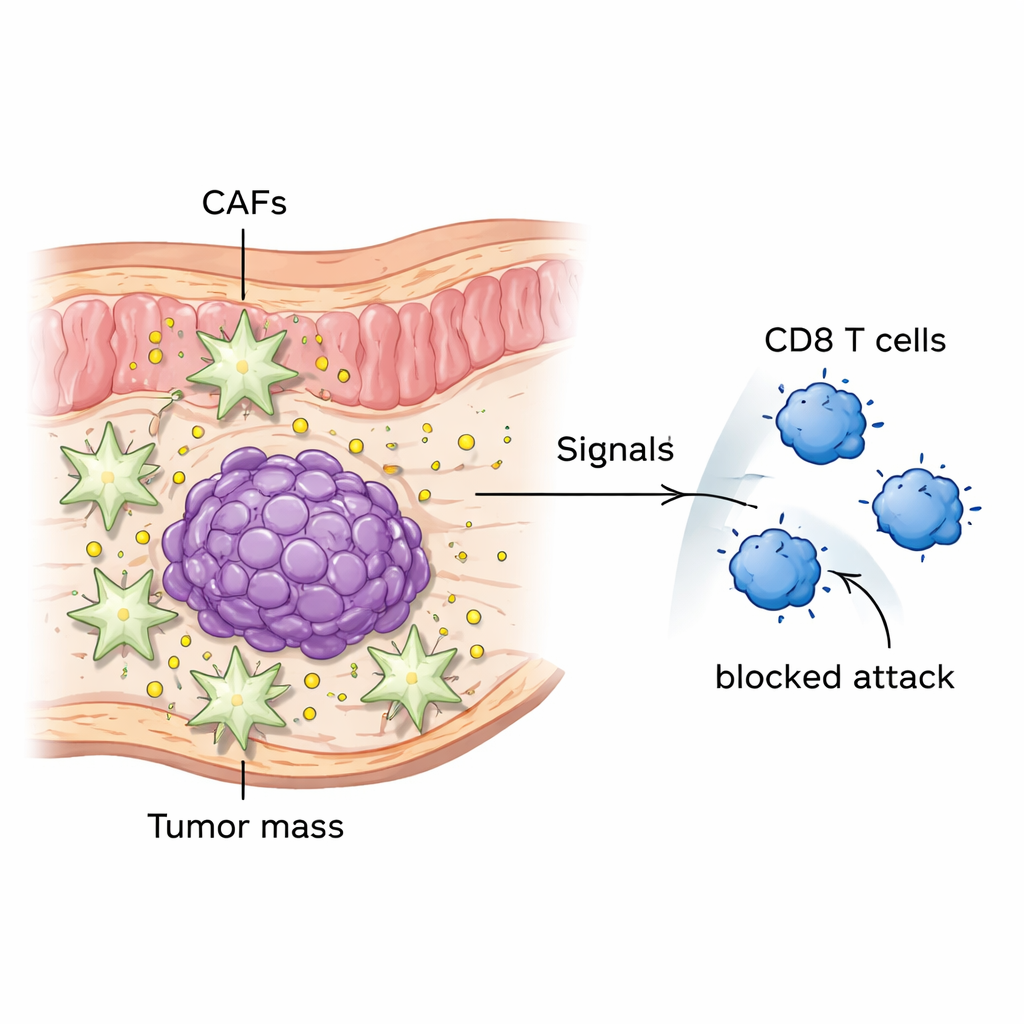
Ein Wachstumsschalter auf Krebszellen
Das Team fragte weiter, wie MFAP2 das Wachstum und die Ausbreitung von Krebszellen tatsächlich antreibt. Sie entdeckten, dass von CAFs freigesetztes MFAP2 an einen Rezeptor namens Integrin β8 (ITGB8) auf der Oberfläche kolorektaler Krebszellen bindet. Dieser Kontakt schaltet eine interne Signalkaskade namens FAK–ERK1/2 ein, die für Zellteilung und -bewegung bekannt ist. Einer der zentralen Schalter dieser Kette ist der Genregulator ETS2. Wenn ETS2 ansteigt, werden Kolonkrebszellen invasiver und überlebensfähiger, selbst wenn sie von Immunzellen angegriffen werden. Blockierten die Forschenden MFAP2 oder ITGB8 bzw. reduzierten ETS2, schrumpften Tumore bei Mäusen und es bildeten sich weniger Lebermetastasen.
Wie Tumoren Immunangriffe austrocknen
Darmtumoren werden häufig von CD8‑T‑Zellen durchdrungen – Immunzellen, die darauf spezialisiert sind, Krebszellen zu suchen und zu töten. Patienten, deren Tumoren mehr dieser Zellen enthalten, leben meist länger. Doch in Tumoren mit hohem MFAP2 fanden die Forschenden weniger CD8‑T‑Zellen und Hinweise darauf, dass die vorhandenen Zellen erschöpft und weniger funktionell waren. Sie führten diesen Effekt auf eine Veränderung im Cholesterinstoffwechsel der Tumorzellen zurück. ETS2 erhöht die Produktion eines Enzyms namens CYP27A1, das Cholesterin in ein Molekül namens 27‑Hydroxycholesterin (27‑HC) umwandelt. Dieses lipophile Molekül wirkt dann auf einen Sensor in T‑Zellen, LXRβ, der deren Aktivität dämpft. Sowohl in Zellkulturen als auch bei Mäusen führte mehr MFAP2 zu erhöhten 27‑HC‑Spiegeln im Tumorumfeld, zu verstärktem T‑Zell‑Tod und -Dysfunktion sowie zu vermehrtem Tumorwachstum.
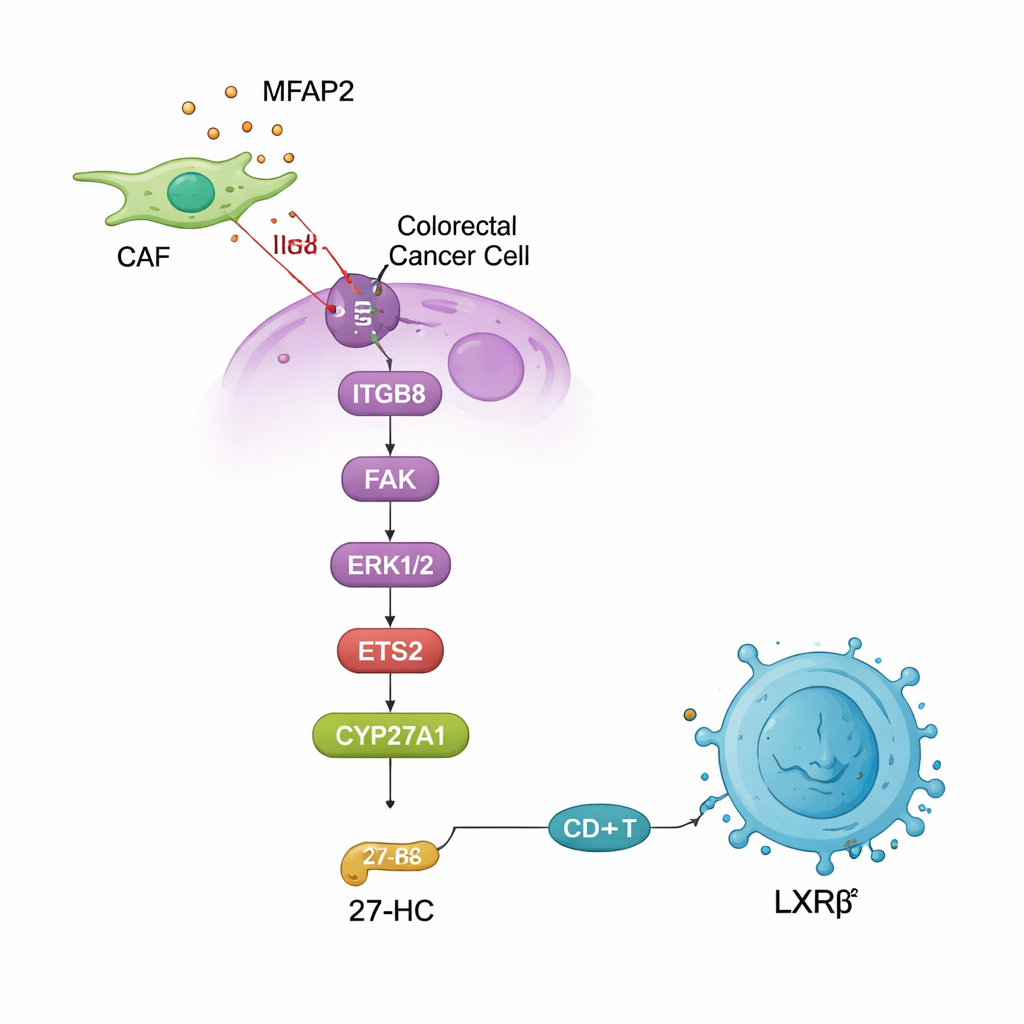
Stoffwechsel, Fibroblasten und Immunflucht verknüpft
Diese Arbeit verknüpft mehrere scheinbar getrennte Aspekte der Krebsbiologie: die Stütz‑ und Signalzellen rund um den Tumor, die intrazelluläre Signalgebung in Krebszellen und die Art und Weise, wie der Tumor den Fettstoffwechsel umlenkt, um die Immunabwehr zu schwächen. Indem sie MFAP2 an die Spitze einer Kette stellten, die über ITGB8, FAK, ERK1/2, ETS2 und CYP27A1 verläuft und mit 27‑HC endet, das CD8‑T‑Zellen über LXRβ lahmlegt, beschreiben die Forschenden einen kompletten Weg vom Fibroblasten‑Signal bis zur Immunflucht. Wichtig ist: Die Hemmung von MFAP2 oder ETS2 verlangsamte nicht nur das Tumorwachstum, sondern stellte in Mäusen auch die T‑Zell‑Infiltration und -Funktion wieder her, was darauf hindeutet, dass dieser Signalweg angepeilt werden könnte, um Immuntherapie und Standardbehandlungen zu verbessern.
Was das für künftige Therapien bedeutet
Für Nicht‑Spezialisten lautet die Kernaussage: Einige der schädlichsten Akteure beim Darmkrebs sind nicht allein die Tumorzellen, sondern ihre Komplizen und die chemischen Signale, die diese senden. MFAP2, produziert von Fibroblasten im Tumor, fördert das Wachstum der Krebszellen und schützt sie vor Angriffen, indem es die körpereigenen Killer‑T‑Zellen durch ein cholesterinbasiertes Signal schwächt. Da diese MFAP2‑getriebene Kette mehrere Angriffspunkte bietet – beim Fibroblasten, an der Tumorzelloberfläche, in der intrazellulären Signalweiterleitung und an der T‑Zelle – ergeben sich mehrere potenzielle Ansatzpunkte für neue Arzneimittel. Therapien, die diesen Signalweg unterbrechen, könnten sowohl die Tumorausbreitung verlangsamen als auch erschöpfte T‑Zellen „wiedererwecken“ und so die Ergebnisse für Patienten mit kolorektalem Krebs verbessern.
Zitation: Zhang, X., Fei, Y., Xie, C. et al. Cancer-associated fibroblasts (CAFs) derived from MFAP2 promote CRC proliferation and metastasis while suppressing CD8+ T cell-mediated antitumor immunity. Cell Death Dis 17, 159 (2026). https://doi.org/10.1038/s41419-026-08413-w
Schlüsselwörter: kolorektales Karzinom, Tumormikroumgebung, krebsassoziierte Fibroblasten, Immunevasion, Cholesterinstoffwechsel