Clear Sky Science · de
Laktatübertragung von hypoxischen Tumorzellen fördert Makrophagen‑Seneszenz und M2‑Polarisation über die DNMT1‑NHE7‑Achse und beschleunigt so das Fortschreiten des Endometriumkarzinoms
Warum es wichtig ist, Tumoren den Sauerstoff zu entziehen
Das Endometriumkarzinom, das aus der Gebärmutterschleimhaut entsteht, wird weltweit immer häufiger. Viele fortgeschrittene Tumoren sind schwer zu behandeln, weil sie wiederkehren, metastasieren oder gegen Standardtherapien resistent sind. Diese Studie untersucht, was in diesen Tumoren passiert, wenn sie wenig Sauerstoff haben – ein typisches Merkmal schnell wachsender Krebserkrankungen – und zeigt, wie ein einfaches Abbauprodukt, Laktat, nahegelegene Immunzellen so umlenken kann, dass sie dem Tumor eher helfen, statt ihn zu bekämpfen.
Wenig Sauerstoff verwandelt Tumoren in Laktatfabriken
Wenn sich Endometriumkarzinomzellen vermehren, kann ihre Blutversorgung nicht mithalten, wodurch Bereiche mit niedrigem Sauerstoffgehalt, sogenannte Hypoxie, entstehen. Die Zellen reagieren, indem sie einen zentralen Regulator namens HIF1A aktivieren, der die Energieproduktion umprogrammiert. Statt hauptsächlich auf effiziente Energiegewinnung zu setzen, erhöhen die Zellen die Glykolyse – einen schnellen, aber energieineffizienten Prozess, der große Mengen Laktat erzeugt. Die Forschenden analysierten Tumordaten von Hunderten Patienten und fanden heraus, dass höhere HIF1A‑Spiegel mit gesteigerter Aktivität vieler glykolysebezogener Gene und Transporter einhergingen, die Laktat aus den Krebszellen pumpen. Patienten, deren Tumoren mehr HIF1A zeigten, hatten tendenziell eine schlechtere Prognose, was darauf hindeutet, dass diese metabolische Umstellung eng mit aggressiver Krankheit verbunden ist.
Wie Tumorabfall hilfreiche Immunzellen umgestaltet
Makrophagen sind Immunzellen, die je nach Zustand Tumoren angreifen oder unterstützen können. In dieser Arbeit zeigten die Forschenden, dass unter Hypoxie Endometriumkarzinomzellen deutlich mehr Laktat in ihre Umgebung freisetzen. Dieses Laktat wird über einen Transporter namens MCT3 aus den Tumorzellen exportiert und dann über einen anderen Transporter, MCT1, in Makrophagen aufgenommen. Im Inneren schiebt Laktat die Makrophagen von einem defensiven Zustand in Richtung des sogenannten M2‑Zustands, der mit Gewebereparatur, Unterdrückung von Entzündungen und leider auch der Unterstützung von Tumorwachstum verbunden ist. In Laborexperimenten zeigten Makrophagen, die mit laktatreichem Tumorflüssigkeits‑Milieu behandelt wurden, vermehrt M2‑Marker, und die von ihnen sezernierte Flüssigkeit förderte wiederum Wachstum, Migration und Invasion von Krebszellen. 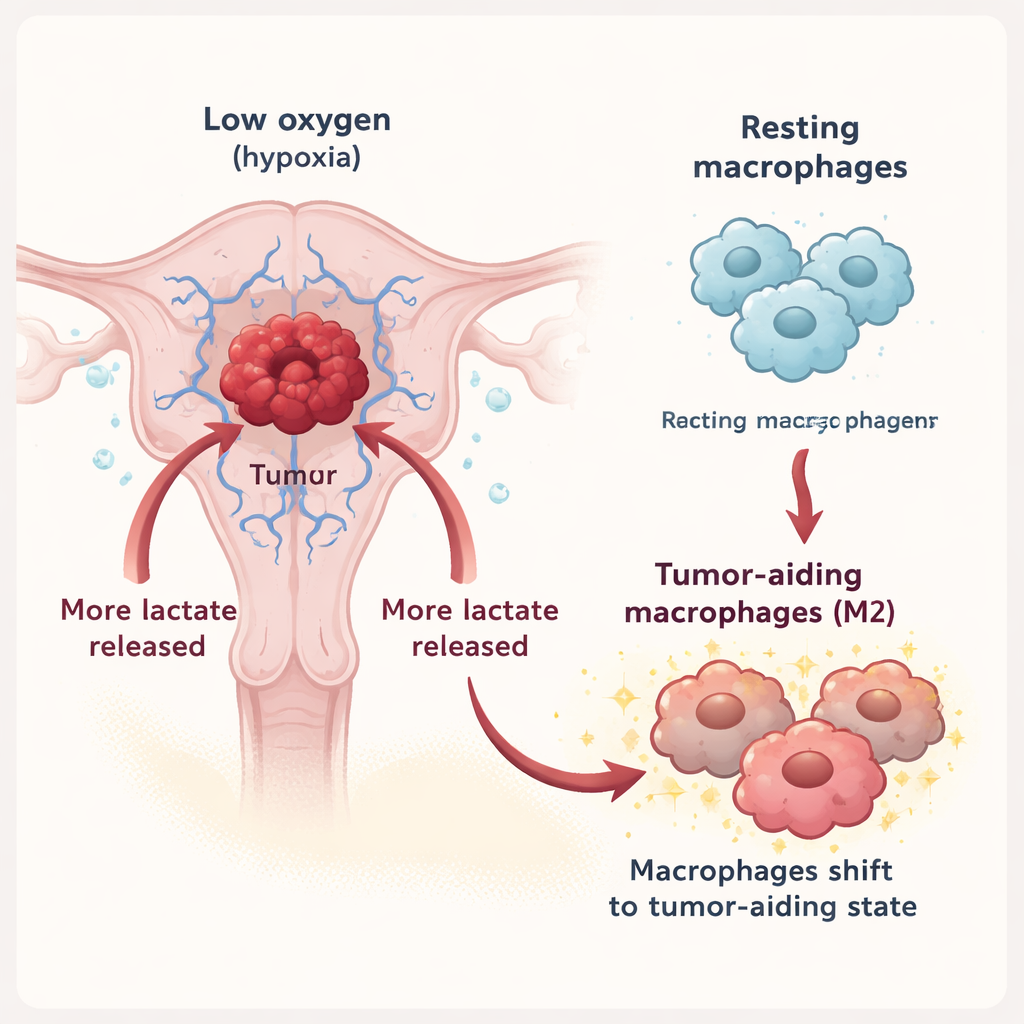
Ein epigenetischer Schalter, der ein zelluläres „pH‑Ventil“ stilllegt
Die Studie geht einen Schritt weiter und deckt den molekularen Schalter in Makrophagen auf, der tumor‑abgeleitetes Laktat mit diesem schädlichen Verhalten verbindet. Laktat treibt nicht nur Stoffwechselprozesse an; es kann auch Histonproteine im Zellkern modifizieren – eine chemische Markierung, die als Laktylierung bezeichnet wird und beeinflusst, welche Gene ein‑ oder ausgeschaltet werden. Die Forschenden fanden, dass Laktat eine spezifische Histonmarkierung in der Kontrollregion des DNMT1‑Gens erhöht und so dessen Aktivität steigert. DNMT1 ist ein Enzym, das DNA methyliert und dadurch Gene stilllegen kann. Eines seiner Ziele hier ist NHE7, ein Protein, das hilft, den Säuregehalt in bestimmten Zellkompartimenten zu regulieren. Wenn DNMT1 hochreguliert ist, erhöht sich die Methylierung des NHE7‑Gens, sodass dessen Expression sinkt. Verminderte NHE7‑Spiegel stören das interne pH‑Gleichgewicht und aktivieren eine Signalkaskade, bekannt als MAPK‑Weg. Dieser Weg treibt wiederum Makrophagen in den tumorfördernden M2‑Zustand und in eine Form des Alterns, die Seneszenz genannt wird, wodurch sie in einen chronischen, tumorfördernden Modus verriegelt werden.
Von der molekularen Kettenreaktion zu schneller wachsenden Tumoren
Um zu prüfen, ob diese Abfolge in lebenden Organismen relevant ist, erzeugten die Wissenschaftler Mausmodelle, in denen menschliche Endometriumkrebszellen zusammen mit menschenähnlichen Makrophagen wuchsen. Wenn zusätzliches Laktat zugeführt wurde, wuchsen die Tumoren stärker, zeigten mehr teilende Zellen und enthielten mehr M2‑typische, seneszente Makrophagen mit hohem DNMT1‑ und niedrigem NHE7‑Niveau. Auffällig war, dass Tumoren, in denen Makrophagen so manipuliert wurden, dass sie vermehrt NHE7 produzierten, weniger stark auf das laktatbedingte Tumorwachstum reagierten: Die Tumoren waren kleiner, wiesen mehr sterbende Zellen auf und enthielten weniger M2‑typische und seneszente Makrophagen. Die Blockade des DNMT1‑Enzyms oder des MAPK‑Wegs schwächte ebenfalls die Fähigkeit von Laktat, Makrophagen umzuprogrammieren, und untermauerte die Vorstellung, dass diese Moleküle eine verbundene Achse bilden. 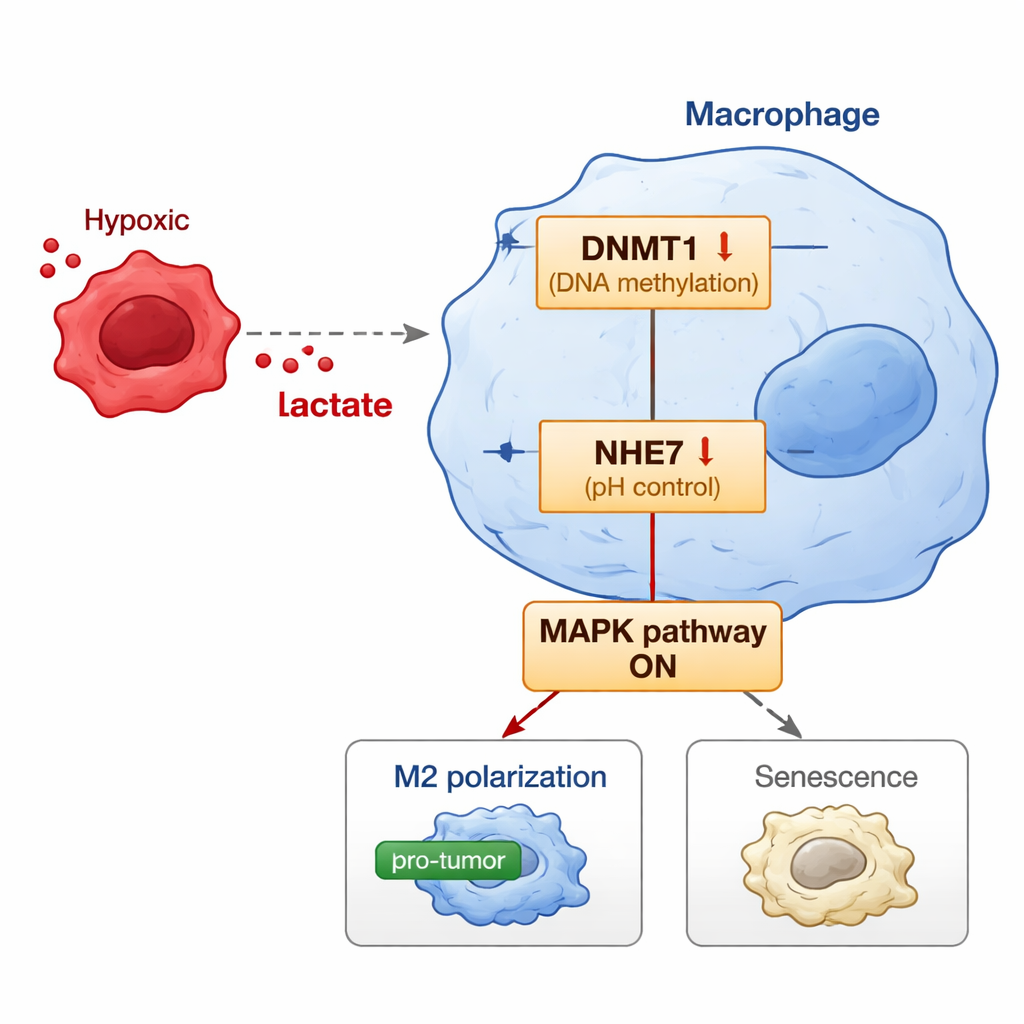
Die Tricks des Tumors als Therapieziele nutzen
Für Nicht‑Fachleute ist die Kernbotschaft, dass Endometriumtumoren niedrige Sauerstoffverhältnisse und Laktat – einst als bloße zelluläre Abfallprodukte betrachtet – einsetzen können, um nahegelegene Immunzellen zu „umerziehen“ und dem Krebs zu Hilfe zu kommen. Sie tun dies über ein epigenetisches Relay: Laktat steigert DNMT1, das NHE7 stilllegt, wodurch Signale aktiviert werden, die Makrophagen in einen tumorfreundlichen, gealterten Zustand fixieren. Durch Eingreifen in einen beliebigen Schritt dieser Laktat–DNMT1–NHE7–MAPK‑Kette könnte es möglich sein, die anti‑tumorale Immunaktivität wiederherzustellen und das Tumorwachstum zu verlangsamen. Diese Arbeit weist auf künftige Therapien hin, die nicht nur die Krebszellen direkt angreifen, sondern auch die vom Tumor umgedrehten Immunzellen neu‑programmieren.
Zitation: Yang, S., Ma, Y., Wu, T. et al. Lactate transmission from hypoxic tumor cells promotes macrophage senescence and M2 polarization via the DNMT1-NHE7 axis to accelerate endometrial cancer progression. Cell Death Dis 17, 185 (2026). https://doi.org/10.1038/s41419-026-08411-y
Schlüsselwörter: Endometriumkarzinom, Tumormikroumgebung, Laktatstoffwechsel, Makrophagenpolarisation, epigenetische Regulation