Clear Sky Science · de
Jenseits des Stoffwechsels: Erforschung der regulatorischen und therapeutischen Bedeutung von Lactat und Lactylierung beim krebsregulierten Zelltod
Warum ein „Abfallprodukt“ des Zuckers für Krebs wichtig ist
Jahrzehntelang galt Lactat – die Substanz, die überanstrengte Muskeln brennen lässt – als zellulärer Müll. Dieser Übersichtsartikel zeigt, dass Lactat beim Krebs alles andere als Abfall ist. Es dient als Brennstoff, als chemisches Signal und sogar als Schalter, der darüber entscheiden kann, ob Tumorzellen überleben oder zugrunde gehen. Dieses verborgene Wirkungsfeld zu verstehen, könnte neue Wege eröffnen, Krebszellen zur Selbstzerstörung zu bringen und gleichzeitig gesundes Gewebe zu schonen.
Die Zuckerabkürzung, die Krebszellen umprogrammiert
Krebszellen sind berüchtigt für ihren „Süßhunger“. Selbst bei ausreichender Sauerstoffversorgung bevorzugen sie, Glukose schnell zu Lactat abzubauen, statt sie vollständig in den Mitochondrien zu verbrennen – eine Umstellung, die als Warburg‑Effekt bekannt ist. Diese Strategie erlaubt Tumoren, Energie und Baustoffe in hoher Geschwindigkeit zu erzeugen. Das resultierende Lactat wird über spezielle Transporter nach außen gepumpt und schafft so ein saures, nährstoffreiches Tumormikroumfeld, das Wachstum unterstützt und Tumoren hilft, sich an Stress wie Sauerstoffmangel oder Chemotherapie anzupassen.
Lactat als Regler verschiedener Todesarten
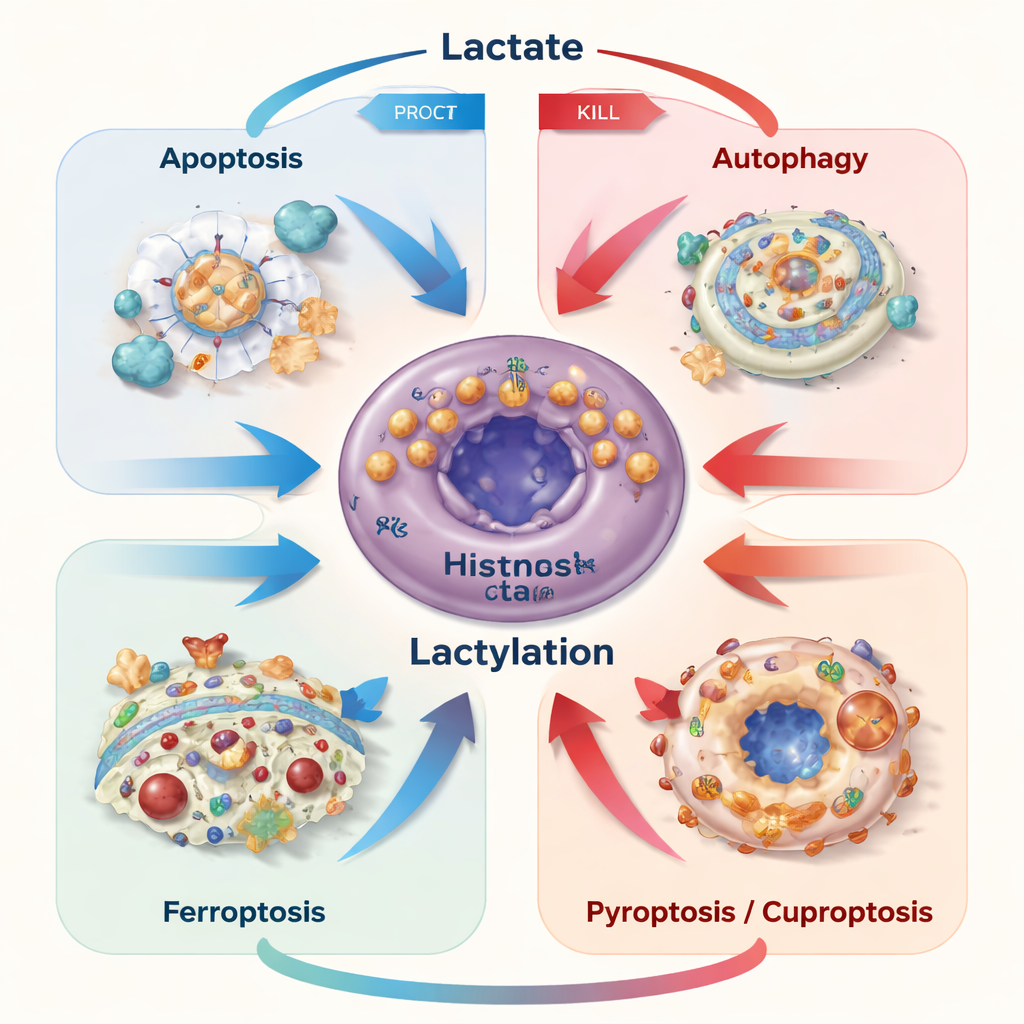
Zelltod in unserem Körper ist normalerweise streng kontrolliert, um beschädigte oder gefährliche Zellen zu entfernen. Krebszellen entziehen sich häufig diesen Programmen. Die Autoren beschreiben, wie Lactat sowohl mehrere regulierte Todeswege blockieren als auch auslösen kann – Apoptose (zellulärer „Selbstmord“), Autophagie (Selbstverdauung), Ferroptose (eisengetriebene Membranschädigung), Pyroptose (entzündliches Aufplatzen) und Cuproptose (kupfergetriebener Kollaps). Wenn Krebszellen moderate Mengen an Lactat produzieren oder aufnehmen, nutzen sie es typischerweise als Brennstoff und als Überlebenssignal, das Wege aktiviert, die sie vor Chemotherapie, Nährstoffmangel oder gezielten Medikamenten schützen. Wenn jedoch Lactat innerhalb der Zellen anreichert, etwa weil sein Export blockiert ist, können der entstehende Säurestress und mitochondriale Schäden den Schalter umlegen und Zellen in Richtung Apoptose oder Ferroptose drängen.
Lactylierung: wenn Lactat auf Proteine schreibt
Eine auffällige jüngste Entdeckung ist, dass Lactat in ein kleines chemisches Etikett umgewandelt und an Lysinreste von Proteinen angehängt werden kann – eine Modifikation, die als Lactylierung bekannt ist. Enzyme fungieren dabei als „Schreiber“ und „Radierer“ dieser Markierungen und dekorieren sowohl histongebundene DNA‑Proteine als auch viele andere Proteine. Diese Markierungen verändern, welche Gene ein- oder ausgeschaltet werden, wie Enzyme funktionieren und wie stabil zentrale Regulatoren sind. Bei Krebs feinjustiert die Lactylierung das Gleichgewicht zwischen Überleben und Selbstzerstörung. Sie kann beispielsweise Proteine erhöhen, die die Apoptose blockieren, Autophagie verstärken, Zellen vor Ferroptose schützen, indem sie die Eisenkontrolle verschärft und Antioxidantien stärkt, oder neue Todesformen wie die Cuproptose beeinflussen, indem sie den Umgang der Zellen mit kupfersensitiven Proteinen verändert.
Ein zweiseitiges Gespräch zwischen Stoffwechsel und Todesprogrammen
Die Beziehung ist nicht einseitig: Zelltodwege verändern ebenfalls, wie Tumoren Zucker nutzen und Lactat produzieren. Wenn Mitochondrien während früher Apoptose oder Mitophagie (selektive Entfernung von Mitochondrien) beschädigt werden, greifen Zellen oft wieder verstärkt auf schnelle Glykolyse zurück, was die Lactatausstoß erhöht. Umgebende Unterstützungszellen, wie krebsassoziierte Fibroblasten, können eine ähnliche Umprogrammierung erfahren und zu Lactatfabriken werden, die nahegelegene Tumorzellen versorgen. Andere Todesarten, etwa Ferroptose, neigen dazu, die Glykolyse zu unterdrücken und damit die Lactatspiegel zu senken. Das Ergebnis ist eine dynamische Rückkopplungsschleife, in der Stoffwechsel und Todesmechanismen sich beständig anpassen, während der Tumor sich entwickelt und auf Therapien reagiert.
Eine Schwäche in eine Behandlungsstrategie verwandeln
Da Lactat und Lactylierung je nach Kontext entweder Krebszellen schützen oder töten können, argumentieren die Autoren, dass Therapien mehr tun müssen als nur die Lactatproduktion zu blockieren. Zukünftige Behandlungen könnten stattdessen gezielt Lactatflüsse umlenken, dessen Transporter modulieren oder spezifische Lactylierungsmarken angreifen, um Krebszellen über die Kante zu treiben und zugleich anti‑tumorale Immunzellen wieder zu aktivieren, die derzeit durch das saure Milieu blockiert sind. Intelligente Wirkstoffabgabesysteme und Nanomedikamente, die auf lokale Lactat‑ oder pH‑Werte reagieren, zeichnen sich als präzise Anwendungsformen ab. Kurz gesagt: Was einst wie metabolischer Müll wirkte, ist tatsächlich ein mächtiger Steuerknopf für das Schicksal von Krebszellen – und die richtige Bedienung dieses Knopfs könnte bestehende Therapien deutlich wirksamer machen.
Zitation: Chen, C., Lin, A., Zhao, J. et al. Beyond metabolism: exploring the regulatory and therapeutic implications of lactate and lactylation in cancer-regulated cell death. Cell Death Dis 17, 184 (2026). https://doi.org/10.1038/s41419-026-08410-z
Schlüsselwörter: Lactat, Lactylierung, Tod von Krebszellen, Tumorstoffwechsel, Ferroptose