Clear Sky Science · de
Wirksamkeit und Sicherheit von niedrig- und hochintensivem fokussiertem Ultraschall bei Glioblastom: eine systematische Übersicht präklinischer und klinischer Studien
Die Verteidigung des Gehirns durchbrechen
Glioblastom gehört zu den tödlichsten Hirntumoren, zum Teil weil es sich hinter der natürlichen Schutzbarriere des Gehirns versteckt – der Blut‑Hirn‑Schranke –, die viele Medikamente fernhält. Diese Übersichtsarbeit betrachtet eine neue Möglichkeit, diese Tumoren ohne Schädelöffnung zu erreichen und anzugreifen: sorgfältig fokussierte Schallwellen. Anhand des Vergleichs zahlreicher Tierversuche und früher Studien am Menschen untersuchen die Autorinnen und Autoren, wie zwei Formen des fokussierten Ultraschalls zusammenwirken könnten, um Medikamente wirkungsvoller zu liefern und Teile des Tumors gezielt thermisch zu zerstören.
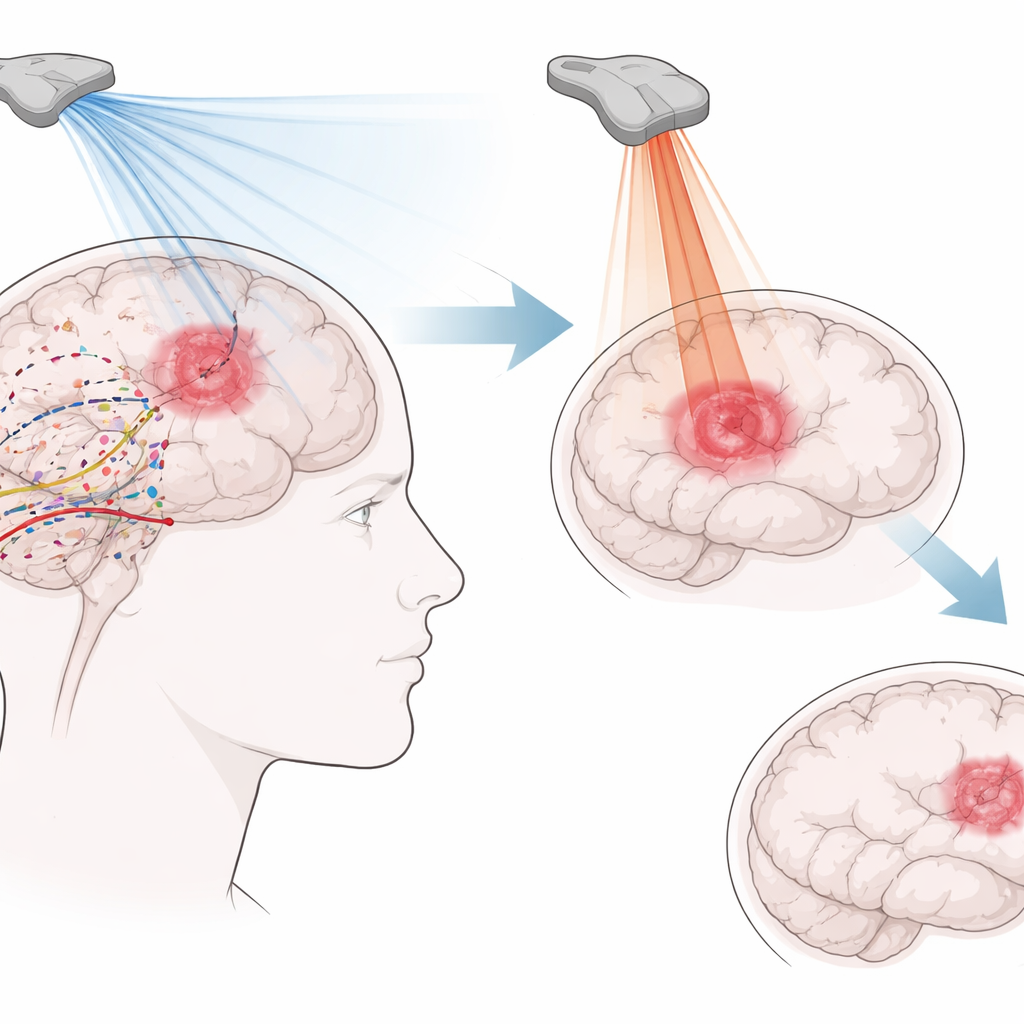
Warum sich dieser Hirntumor so schwer behandeln lässt
Die Standardbehandlung beim Glioblastom kombiniert Operation, Bestrahlung und Chemotherapie, doch die meisten Patientinnen und Patienten überleben kaum mehr als ein Jahr. Der Tumor wächst wurzelartig durch das Gehirn und macht eine vollständige Entfernung nahezu unmöglich. Zugleich blockiert die Blut‑Hirn‑Schranke, die das Gehirn normalerweise schützt, viele Krebsmedikamente daran, entkommende Zellen nach einer Operation zu erreichen. Die Umgebung des Tumors ist außerdem immunfeindlich: Es gibt nur wenige tumorbekämpfende T‑Zellen und viele Immunzellen, die das Tumorwachstum unterstützen. Dieses Zusammenwirken von Hindernissen erklärt, warum selbst vielversprechende neue Wirkstoffe im Gehirn oft wirkungslos bleiben.
Sanfter Schall, um das Tor des Gehirns zu öffnen
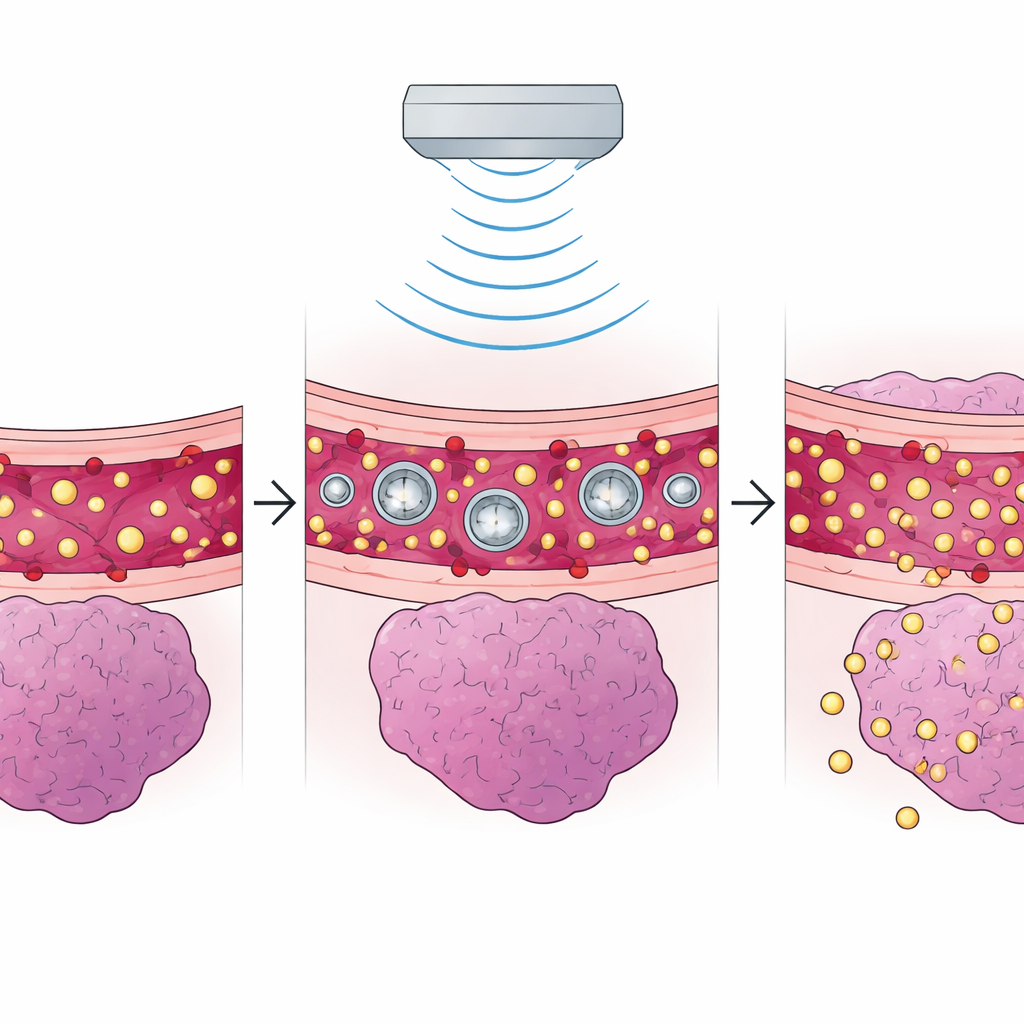
Niedrigintensiver fokussierter Ultraschall nutzt winzige Gasbläschen, die in den Blutkreislauf gegeben werden. Wenn Schallwellen hindurchgehen, beginnen diese Bläschen leicht zu vibrieren und treiben die eng anliegenden Zellen aus, die die Blutgefäße im Gehirn abdichten. In Tierstudien ermöglichte dieses temporäre "Auflockern" deutlich höhere Konzentrationen von Chemotherapeutika, Immuntherapien und sogar gentransportierenden Partikeln im Tumor. Viele Experimente zeigten Tumorverkleinerungen und verlängerte Überlebenszeiten von etwa drei bis vier Wochen auf sechs bis elf Wochen. Frühe klinische Studien bestätigen ähnliche Muster: In Kombination mit Standardmedikamenten wie Temozolomid oder Carboplatin öffnete diese Methode zuverlässig die Schranke, erhöhte die Arzneistoffkonzentration in behandelten Hirnarealen und erzeugte progressionsfreie Intervalle von einigen Monaten, wobei eine kleine Kohorte zeigte, dass alle Patienten nach einem Jahr noch lebten.
Schall als präzises thermisches Skalpell
Hochintensiver fokussierter Ultraschall wirkt anders. Hier werden stärkere Schallwellen auf einen kleinen Zielbereich konzentriert, wodurch Gewebe so erhitzt wird, dass Krebszellen direkt abgetötet werden. In Tiermodellen führte die Kombination dieses stärkeren Ultraschalls mit medikamentenbeladenen Partikeln oder Kontrastmitteln häufig zu einer etwa 70‑prozentigen Reduktion des Tumorwachstums und verbesserte das Überleben, ohne benachbarte Organe zu schädigen. Beim Menschen waren die Ergebnisse bisher jedoch zurückhaltender. Ein sorgfältig überwachter Fall erreichte nur etwa ein Zehntel des Tumorvolumens, das zerstört wurde, und eine andere frühe Studie erzielte therapeutische Temperaturen ohne sichtbare Tumorverkleinerung. Die Eigenschaft des Schädels, Ultraschallenergie zu beugen und zu absorbieren, sowie die diffuse Ausbreitung von Glioblastomzellen jenseits eines klaren Knotens machen diesen hitzebasierten Ansatz technisch anspruchsvoll.
Sicherheit, Grenzen und Ausblick
Insgesamt wirkten beide Ansätze über 40 untersuchte Studien hinweg bei sorgfältiger Anwendung bemerkenswert sicher. Niedrigintensive Behandlungen führten meist zu milden, kurzlebigen Effekten wie Kopfschmerzen, winzigen punktförmigen Blutungen, die nur im Bildgebungsverfahren sichtbar waren, oder vorübergehenden Empfindungen wie Kribbeln oder Wärme. Die Blut‑Hirn‑Schranke schloss sich in der Regel innerhalb eines Tages wieder, und es wurden keine bleibenden Hirnschäden berichtet. Hochintensive Behandlungen verursachten kurzzeitige Wärmegefühle oder Unbehagen, jedoch keine schweren Blutungen oder dauerhafte Defizite in der kleinen Zahl bislang behandelter Patientinnen und Patienten. Die Datenbasis ist jedoch uneinheitlich: Viele Tierversuche wiesen keine vollständige Verblindung oder Randomisierung auf, und die meisten Humanergebnisse stammen aus kleinen, nicht randomisierten Studien in wohlhabenden Ländern, sodass belastbare Schlussfolgerungen schwerfallen.
Was das für Patientinnen, Patienten und Angehörige bedeutet
Die Autorinnen und Autoren kommen zu dem Schluss, dass niedrig‑ und hochintensiver fokussierter Ultraschall vielversprechende, sich ergänzende Werkzeuge sind, aber keine eigenständigen Heilmittel. Niedrigintensiver Ultraschall steht am ehesten vor der klinischen Umsetzung: Er kann wiederholt und reversibel das Tor des Gehirns öffnen, sodass mehr Medikamente und Immunzellen versteckte Tumornester erreichen. Hochintensiver Ultraschall könnte eines Tages helfen, klar abgrenzbare Tumorkerne zu verkohlen, besonders in Kombination mit verbesserten Medikamentenlieferungen. Aber keine der Methoden ist derzeit bereit, Operation, Bestrahlung oder Chemotherapie zu ersetzen. Große, sorgfältig kontrollierte Studien – idealerweise multizentrisch und mit standardisierten Behandlungsprotokollen – sind weiterhin erforderlich, um zu beweisen, ob diese schallbasierten Strategien das Leben verlängern und die Lebensqualität von Menschen mit Glioblastom erhalten können.
Zitation: Alrashidi, M., Ferro, F., Almohammadi, A. et al. Efficacy and safety of low- and high-intensity focused ultrasound in glioblastoma: a systematic review of preclinical and clinical studies. Br J Cancer 134, 977–995 (2026). https://doi.org/10.1038/s41416-025-03325-6
Schlüsselwörter: Glioblastom, fokussierter Ultraschall, Blut‑Hirn-Schranke, Hirntumortherapie, nichtinvasive Onkologie