Clear Sky Science · de
Funktionelle Spuren von homologer Rekombinationsdefizienz beim Prostatakrebs, aufgedeckt durch ctDNA-Fragmentierung und Transkriptionsfaktor‑Zugänglichkeit
Warum das für Krebspatienten wichtig ist
Viele Männer mit fortgeschrittenem Prostatakrebs könnten von Medikamenten profitieren, die Schwachstellen in der DNA‑Reparatur ihrer Tumoren ausnutzen. Heute übersehen Ärztinnen und Ärzte jedoch oft, wer ansprechen wird, weil die Tests meist schwierige Gewebebiopsien erfordern und sich nur auf eine Handvoll Gene konzentrieren. Diese Studie zeigt, wie sich eine einfache Blutentnahme in eine vielschichtige, aussagekräftige Analyse dieser DNA‑Reparaturschwächen verwandeln lässt, die potenziell präzisere und schonendere Behandlungsentscheidungen unterstützen kann.
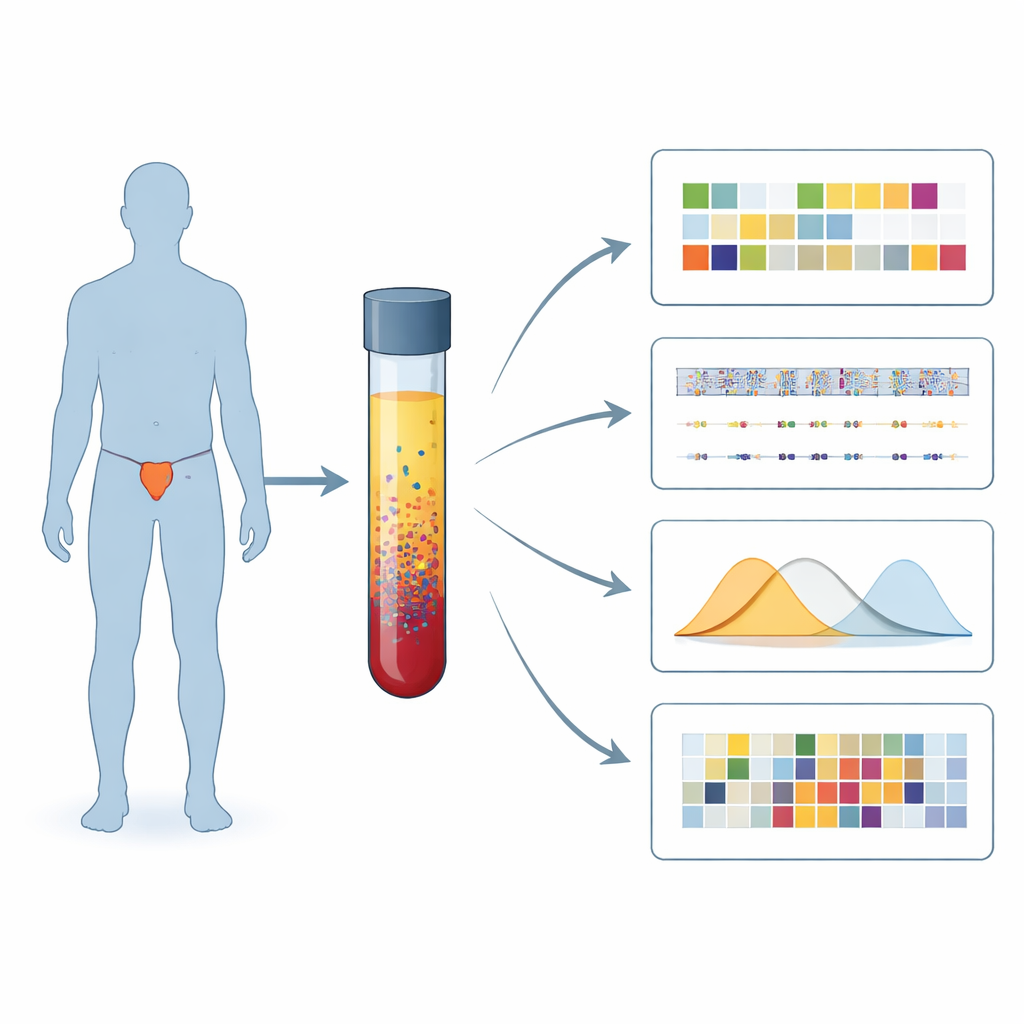
Eine neue Möglichkeit, Krebs‑Signale im Blut zu lesen
Die Forschenden konzentrierten sich auf ein spezifisches Reparaturproblem, die homologe Rekombinationsdefizienz (HRD), die Tumoren besonders anfällig für Wirkstoffe wie PARP‑Inhibitoren und für bestimmte Chemotherapien macht. Statt sich auf Tumorproben aus Knochen oder Prostata zu stützen, analysierten sie Bruchstücke von Tumor‑DNA im Blut, bekannt als zirkulierende Tumor‑DNA. Von 375 Männern mit metastasiertem Prostatakrebs wählten sie 106 aus, deren Blut genügend Tumor‑DNA für eine ausführliche Untersuchung enthielt, und wendeten mehrere sich ergänzende Tests auf dieselben Plasma‑Proben an.
Weiter denken als nur Einzelmutationen
Zunächst sequenzierten sie ein Panel zentraler DNA‑Reparaturgene, darunter bekannte Akteure wie BRCA2, BRCA1 und PALB2 sowie weitere Gene, die beeinflussen, wie aggressiv Prostatatumoren werden. BRCA2 erwies sich als das am häufigsten veränderte Reparaturgen und trat oft zusammen mit Verlusten anderer wichtiger Kontrollgene wie PTEN und RB1 auf. Das Team untersuchte jedoch auch große strukturelle Veränderungen der Chromosomen im gesamten Genom und nutzte hierfür Low‑Depth‑Whole‑Genome‑Sequencing zur Berechnung eines genomischen Instabilitäts‑Scores. Tumoren mit geschädigten BRCA‑Genen oder hohen Scores zeigten stark umstrukturierte Genome und waren mit einer geringeren Gesamtüberlebenszeit verknüpft, was hervorhebt, dass großskalige strukturelle Veränderungen genauso aussagekräftig sein können wie einzelne Mutationen.
Spuren von Reparaturversagen in Mutationsmustern
Bei einer Untergruppe von Patientinnen und Patienten gingen die Wissenschaftlerinnen und Wissenschaftler einen Schritt weiter und sequenzierten alle proteinkodierenden Regionen, um das detaillierte Muster der über die Zeit angesammelten Mutationen zu lesen. Bestimmte Kombinationen von Basenänderungen sowie kleine Insertionen oder Deletionen wirken wie Fingerspuren der Prozesse, die sie erzeugt haben. Sie fanden klassische, mit HRD assoziierte Signaturen, etwa SBS3 und das Indel‑Muster ID6, angereichert in Tumoren mit Reparaturgen‑Defekten und hoher genomischer Instabilität. Andere Signaturen deuteten auf getrennte Probleme hin, wie ein Versagen der Fehlpaarungsreparatur oder einen eigenständigen Subtyp, der von CDK12 getrieben wird, und unterstreichen, dass unterschiedliche DNA‑Reparaturausfälle erkennbare, voneinander verschiedene Spuren im Genom hinterlassen.
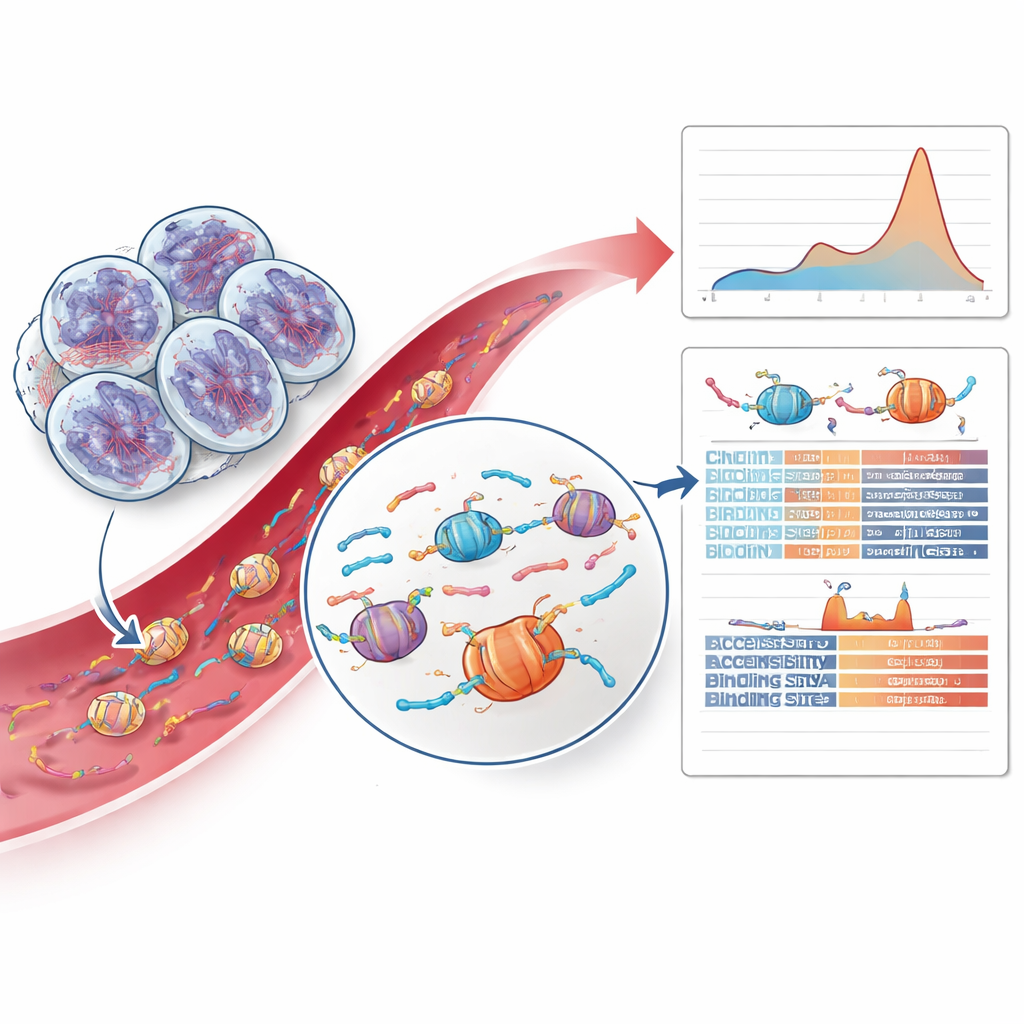
DNA‑Fragmentmuster und Chromatin‑Hinweise entschlüsseln
Der innovativste Teil der Arbeit ging über Mutationen hinaus und untersuchte, wie die Tumor‑DNA fragmentiert ist. Wenn Zellen sterben, wird ihre DNA rund um Proteinhüllen namens Nukleosomen geschnitten, wodurch Fragmente mit charakteristischen Längen und Endmustern entstehen. Das Team entdeckte, dass Tumoren mit HRD relativ häufiger etwas längere Fragmente aufwiesen, die zwei Nukleosomen entsprechen — eine Verschiebung, die in anderen Prostatatumoren oder bei gesunden Kontrollen nicht zu sehen war. Durch das Trainieren eines vorsichtigen Machine‑Learning‑Modells auf Fragmentlängen und Fragmentend‑Merkmalen konnten sie HRD‑positive Fälle allein aus dem Blut mit ermutigender Genauigkeit identifizieren. Außerdem untersuchten sie die Zugänglichkeit unterschiedlicher Genomregionen in der Umgebung von Bindungsstellen für Transkriptionsfaktoren — Proteine, die die Genaktivität steuern — und fanden, dass bestimmte Zinkfinger‑Bindungsstellen in HRD‑Tumoren weniger zugänglich waren, was auf tiefergehende, reparaturbedingte Veränderungen der Chromatin‑Organisation hindeutet.
Was das für Patientinnen und Patienten bedeuten könnte
Zusammen bilden diese Informationsschichten — von spezifischen Genmutationen und großflächigen Chromosomen‑Umordnungen bis hin zu feinen Verschiebungen in der DNA‑Fragmentgröße und der Chromatin‑Zugänglichkeit — ein vollständigeres Bild der DNA‑Reparaturschwäche beim Prostatakrebs. Für Laien lautet die Kernbotschaft: Eine sorgfältig analysierte Blutprobe kann nicht nur zeigen, ob ein bekanntes Gen wie BRCA2 mutiert ist, sondern auch, ob sich ein Tumor wie einer mit schwerer Reparaturstörung verhält, selbst wenn konventionelle Tests normal erscheinen. Wird dieser multimodale, blutbasierte Ansatz in größeren und diverseren Patientengruppen validiert, könnte er helfen, diejenigen zuverlässiger zu identifizieren, die wahrscheinlich von PARP‑Inhibitoren oder Platintherapien profitieren, Veränderungen im Zeitverlauf zu überwachen und schließlich die Therapie mittels eines einfachen, wiederholbaren Tests zu personalisieren.
Zitation: Vlachos, G., Moser, T., Lazzeri, I. et al. Functional footprints of homologous recombination deficiency in prostate cancer revealed by ctDNA fragmentation and transcription factor accessibility. Br J Cancer 134, 949–960 (2026). https://doi.org/10.1038/s41416-025-03301-0
Schlüsselwörter: Prostatakrebs, Liquid Biopsy, DNA‑Reparatur, zirkulierende Tumor‑DNA, PARP‑Inhibitoren