Clear Sky Science · de
Immunosuppressive immune microenvironment landscapes in VISTA-high gastric cancer
Warum die Abwehr des Körpers manchmal gegen Magenkrebs versagt
Moderne Krebstherapien setzen zunehmend darauf, das Immunsystem zu reaktivieren, damit es Tumore angreift. Bei vielen Menschen mit fortgeschrittenem Magenkrebs wirken diese starken Medikamente jedoch schlecht oder verlieren an Wirkung. Diese Studie untersucht einen wichtigen Grund dafür: ein Bremsmolekül namens VISTA, das die lokale Umgebung des Tumors umgestaltet und Immunzellen von Angreifern in Beobachter oder sogar Helfer des Krebses verwandelt. Das Verständnis dieses versteckten Schalters könnte den Weg zu präziseren und wirksameren Immuntherapien öffnen.
Eine verborgene Bremse in der Tumornachbarschaft
Die Autoren konzentrierten sich auf VISTA, ein Protein, das vor allem auf bestimmten weißen Blutkörperchen vorkommt, die in und um Tumore sitzen. VISTA wirkt als Stoppsignal für Immunantworten. Während andere Bremsen wie PD‑1 und PD‑L1 bereits durch zugelassene Medikamente adressiert werden, war die Rolle von VISTA beim Magenkrebs unklar. Um das zu untersuchen, analysierte das Team Gewebe von 172 Patienten mit fortgeschrittener Mehrfarben-Färbung, um viele Zelltypen gleichzeitig zu kartieren. Darüber hinaus nutzten sie Einzelzell-RNA-Sequenzierung und räumliche Transkriptomik an kleineren Probenmengen, um zu prüfen, welche Zellen VISTA tragen, was diese Zellen tun und wo genau sie sich in der Tumorlandschaft befinden. 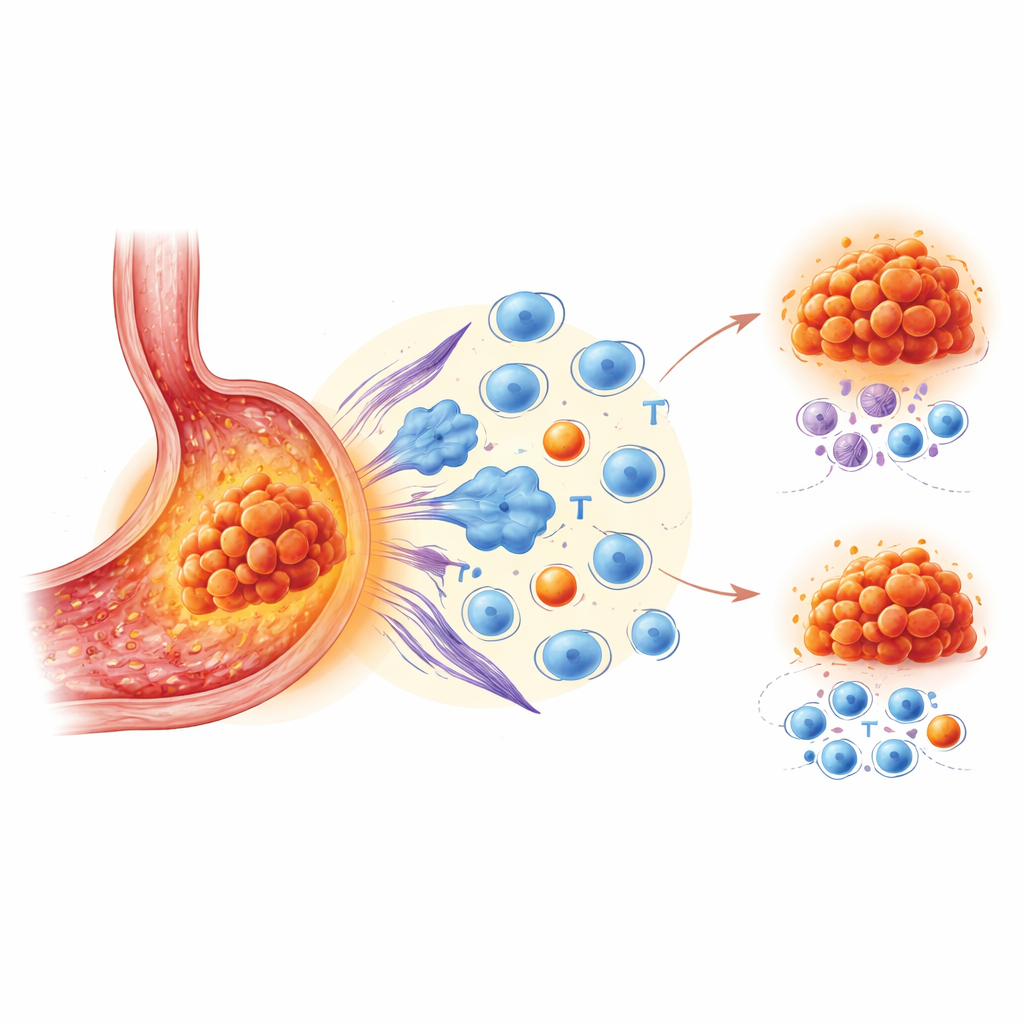
Wenn VISTA hoch ist, wird das Immunsystem gedämpft
Beim Vergleich von Tumoren mit hohen gegenüber niedrigen VISTA-Werten fanden die Forschenden ein konsistentes Muster. VISTA-reiche Tumore waren von Immunzellen umgeben, aber nicht von solchen, die einen starken Angriff führen. Stattdessen gab es eine Anhäufung erschöpfter Killer-T-Zellen, die ihre Schlagkraft verloren hatten, regulatorischer T‑Zellen, die Immunantworten dämpfen, narbenbildende Stütz-Zellen (Fibroblasten) und Makrophagen, die in Richtung eines tumorfördernden Zustands verschoben waren. Patientinnen und Patienten, deren Tumorregionen mehr VISTA enthielten, hatten kürzere Zeiträume bis zum Fortschreiten ihrer Erkrankung nach einer Immuntherapie, selbst unter Berücksichtigung anderer klinischer Faktoren. Anders ausgedrückt: Eine von VISTA dominierte Umgebung sah unter dem Mikroskop aktiv aus, funktionierte aber als „immun‑stille“ bzw. unterdrückende Zone.
Makrophagen als zentrale Vermittler
Bei näherer Betrachtung zoomten die Wissenschaftler auf Monozyten und Makrophagen—Immunzellen, die entweder Krebs fressen oder ihn schützen können. Auf Einzelzellebene war das Gen, das VISTA kodiert (VSIR genannt), besonders aktiv in mehreren Makrophagen-Untergruppen, besonders in solchen, die Tumorproteinfragmente effizient präsentieren, und in solchen mit Merkmalen sogenannter M2- bzw. wundheilungsähnlicher Makrophagen. Mithilfe einer computergestützten Zeitlinie der Zellentwicklung beobachtete das Team, wie VISTA eingeschaltet wurde, als sich Zellen von frühen Monozyten zu reiferen Makrophagen entwickelten, die sich um Tumorzellen gruppierten. Räumliche Kartierung bestätigte, dass VISTA-positive Makrophagen tendenziell in der Nähe von Krebszellen lagen, und Patientinnen und Patienten, deren Tumore mehr dieser Zellen genau an diesen Orten aufwiesen, schnitten nach Behandlung mit Checkpoint-Inhibitoren schlechter ab. 
Wie VISTA-positive Zellen T-Zellen aushöhlen
Die Studie untersuchte außerdem, wie VISTA-tragende Makrophagen mit T‑Zellen kommunizieren. Kommunikationskarten, die aus Genexpressionsdaten erstellt wurden, legen nahe, dass diese Makrophagen häufig über molekulare Paare wie LGALS9 und PTPRC sowie über Moleküle, die an der Präsentation von Tumorfragmenten an T‑Zellen beteiligt sind, mit T‑Zellen in Kontakt treten. Diese ständige Präsentation kann im Laufe der Zeit T‑Zellen von einem frühen, aktiven Zustand in einen chronisch stimulierten, erschöpften Zustand treiben, der durch mehrere inhibitorische Signale an ihrer Oberfläche gekennzeichnet ist. In Proben, in denen Makrophagen höhere VSIR‑Expression zeigten, fanden sich mehr regulatorische T‑Zellen und mehr erschöpfte Killer-T‑Zellen, was die Vorstellung stärkt, dass VISTA-positive Makrophagen zur Immun‑Erschöpfung beitragen statt zu einem scharfen, effektiven Angriff.
Was das für zukünftige Behandlungen bedeuten könnte
Insgesamt zeichnet die Arbeit VISTA als zentralen Schalter, der Magentumore dabei unterstützt, eine immunsuppressive Nische aufzubauen, insbesondere durch spezialisierte Makrophagen, die sowohl Tumormaterial präsentieren als auch inhibitorische Signale an T‑Zellen senden. Für Patientinnen und Patienten deutet dies darauf hin, dass hohe VISTA‑Expression eine Form von Resistenz gegen die derzeitigen Immunmedikamente markiert, die allein PD‑1 oder PD‑L1 anvisieren. Das Blockieren von VISTA—möglicherweise in Kombination mit bestehenden Checkpoint‑Inhibitoren—könnte T‑Zellen wiederbeleben und das Gleichgewicht wieder zugunsten der Tumorkontrolle verschieben. Zwar sind weitere Labor‑ und klinische Studien nötig, doch liefert diese Forschung einen Fahrplan für die Entwicklung neuer Behandlungskombinationen und für die Identifizierung derjenigen Patienten, die am ehesten profitieren dürften.
Zitation: Luo, Y., Peng, H., Yao, Q. et al. Immunosuppressive immune microenvironment landscapes in VISTA-high gastric cancer. Br J Cancer 134, 1066–1079 (2026). https://doi.org/10.1038/s41416-025-03290-0
Schlüsselwörter: Magenkrebs, Tumor-Mikroumgebung, Immun-Checkpoint, Makrophagen, T-Zell-Erschöpfung