Clear Sky Science · de
Spektrum und Funktionen von Ionenkanälen und Transportern in Osteoklasten
Warum unsere Knochen winzige Torwächter brauchen
Unser Skelett wirkt fest und unveränderlich, wird aber ständig abgebaut und neu aufgebaut. Spezialzellen, die Osteoklasten genannt werden, übernehmen die Abrissarbeiten und lösen alten Knochen auf, damit neuer Knochen entstehen kann. Dieser Übersichtsartikel beleuchtet eine verborgene Besetzung mikroskopischer „Torwächter“ – Ionenkanäle und Transporter –, die geladene Atome und Nährstoffe in und aus Osteoklasten passieren lassen. Indem Forscher verstehen, wie diese winzigen Tore den Knochenabbau steuern, hoffen sie, bessere Behandlungen gegen Osteoporose und andere Knochenerkrankungen zu entwickeln.
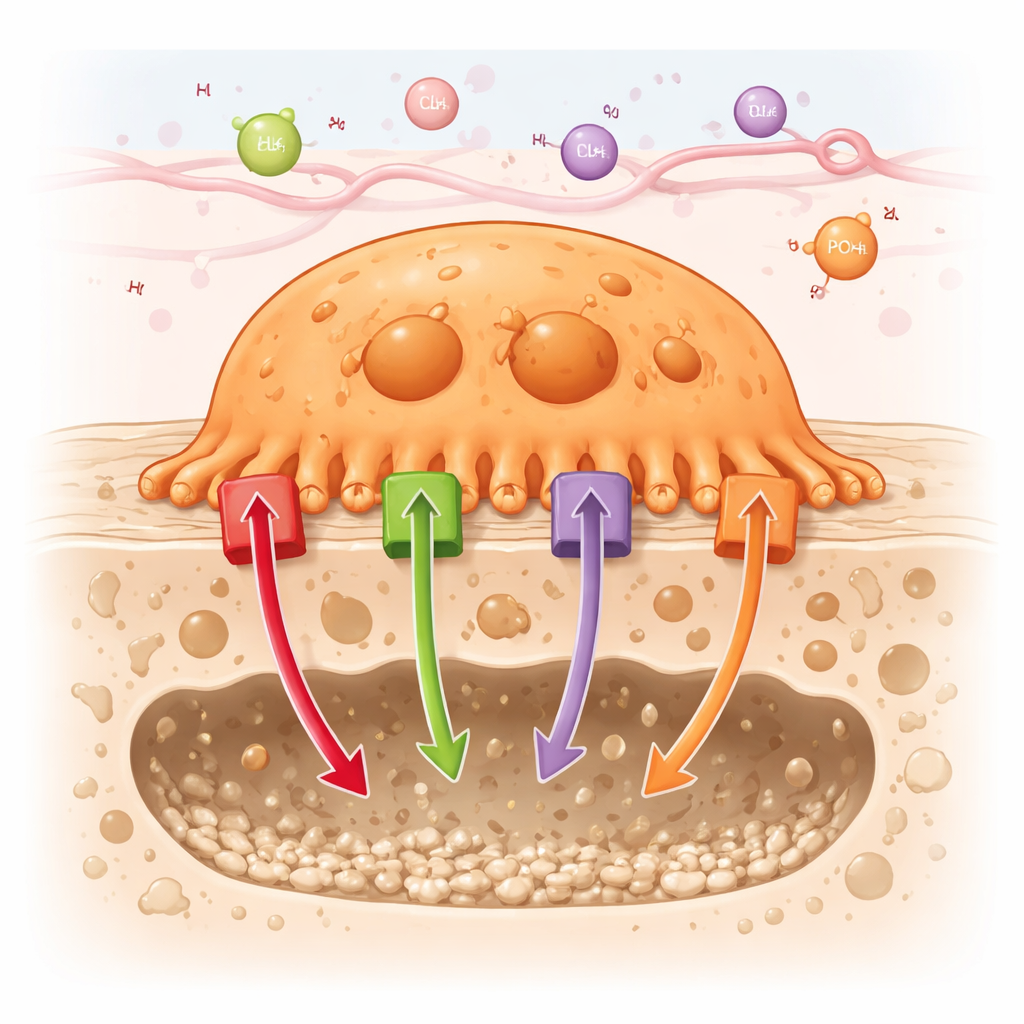
Wie knochenfressende Zellen ihre Aufgabe erfüllen
Osteoklasten arbeiten, indem sie sich eng an die Knochenoberfläche anheften und eine abgedichtete Kammer schaffen, in der sie Mineralien auflösen und Proteine verdauen können. Um diese winzige „Verdauungskammer“ sehr sauer zu machen, pumpen Osteoklasten große Mengen Protonen (Wasserstoffionen) in die Kammer. Gleichzeitig transportieren sie andere Ionen – etwa Chlorid, Kalzium und Phosphat – durch ihre Membranen und in interne Kompartimente. Der Artikel untersucht rund 90 verschiedene Kanäle und Transporter, die in Osteoklasten vorkommen, und ordnet sie sechs Familien zu, darunter energiegetriebene Pumpen (ATPasen), Kationen- und Anionenkanäle, gekoppelte Transporter, Nährstofftransporter und ATP‑bindende Kassetten(ABC)-Transporter.
Säure, Salz und Energie: Die Kernmaschinerie
Zwei Proteinsysteme stechen als zentral für die Knochenresorption hervor. Erstens treiben vakuoläre Protonenpumpen, bekannt als V-ATPasen, aktiv Protonen in die Resorptionskammer und machen sie so sauer genug, um Knochenmineral aufzulösen und proteolytische Enzyme zu aktivieren. Bestimmte V‑ATPase-Untereinheiten, wie a3, d2 und mehrere V1-Komponenten, sind am gekräuselten Rand der Osteoklasten und in Lysosomen angereichert, und genetische Defekte in diesen Untereinheiten können entweder zu geschwächtem Knochen oder zu abnormer Knochenverdickung führen. Zweitens bringt ein Chlorid–Protonenaustauscher namens ClC‑7, der mit einem Protein namens OSTM1 zusammenarbeitet, Chloridionen in denselben Bereich. Das gleicht die elektrische Ladung aus und ermöglicht kontinuierliches Protonenpumpen. Wenn ClC‑7 mutiert ist, entwickeln Menschen und Mäuse Osteopetrose, eine Erkrankung, die durch übermäßig dichte, aber brüchige Knochen gekennzeichnet ist, und zeigt so, wie wesentlich ein korrekter Ionenfluss für die normale Skelettgesundheit ist.
Kalzium, Phosphat und weitere unterstützende Akteure
Über die Säureproduktion hinaus sind Osteoklasten auf fein abgestimmte Handhabung von Kalzium und Phosphat angewiesen. Ein Netz aus Kalziumkanälen und Pumpen in der Zellmembran, dem endoplasmatischen Retikulum, Lysosomen und Mitochondrien erzeugt rhythmische Kalzium‑„Oszillationen“, die Schlüssengene für die Bildung und Fusion von Osteoklasten aktivieren. Transporter am gekräuselten Rand und an der gegenüberliegenden Seite der Zelle transportieren Kalzium und Phosphat aus dem aufgelösten Knochen, entweder um sie innerhalb der Zelle wiederzuverwenden oder sie ins Blut zurückzugeben. Weitere Metalle und Mineralien – wie Mangan, Magnesium, Zink, Kupfer und Eisen – werden ebenfalls von spezialisierten Transportern kontrolliert und beeinflussen, wie aggressiv Osteoklasten Knochen resorbieren. So können Eisen und bestimmte Formen des eisenbedingten Zelltods die Osteoklastenaktivität ankurbeln oder dämpfen, während Zinktransporter dazu tendieren, übermäßigen Knochenverlust zu begrenzen.
Verkehrsregelung innerhalb der Zelle
Ionenkanäle sind nicht auf die Außenmembran beschränkt. Viele sitzen auf internen Kompartimenten wie Lysosomen, Endosomen, dem Golgi-Apparat und Mitochondrien und bilden ein geschichtetes Transportnetz. Diese internen Tore helfen, den pH-Wert in Verdauungsvesikeln einzustellen, die Energieproduktion in Mitochondrien zu unterstützen und den Transport von Enzymen und Abfallstoffen zu steuern. Die Übersichtsarbeit hebt hervor, wie mehrere Kanalsysteme zusammenwirken: Natrium–Wasserstoff‑Austauscher regulieren die interne Säure, Kalium–Chlorid‑Kotransporter helfen, Membranpotenzial und Chloridbalance aufrechtzuerhalten, und purinerge sowie mechanosensitive Kanäle wandeln chemische oder mechanische Signale in Veränderungen der Knochenresorption um. Nährstofftransporter für Glukose, Aminosäuren, Nukleoside und Vitamin C stützen zudem die hohen Energie‑ und biosynthetischen Anforderungen aktiv resorbierender Osteoklasten.
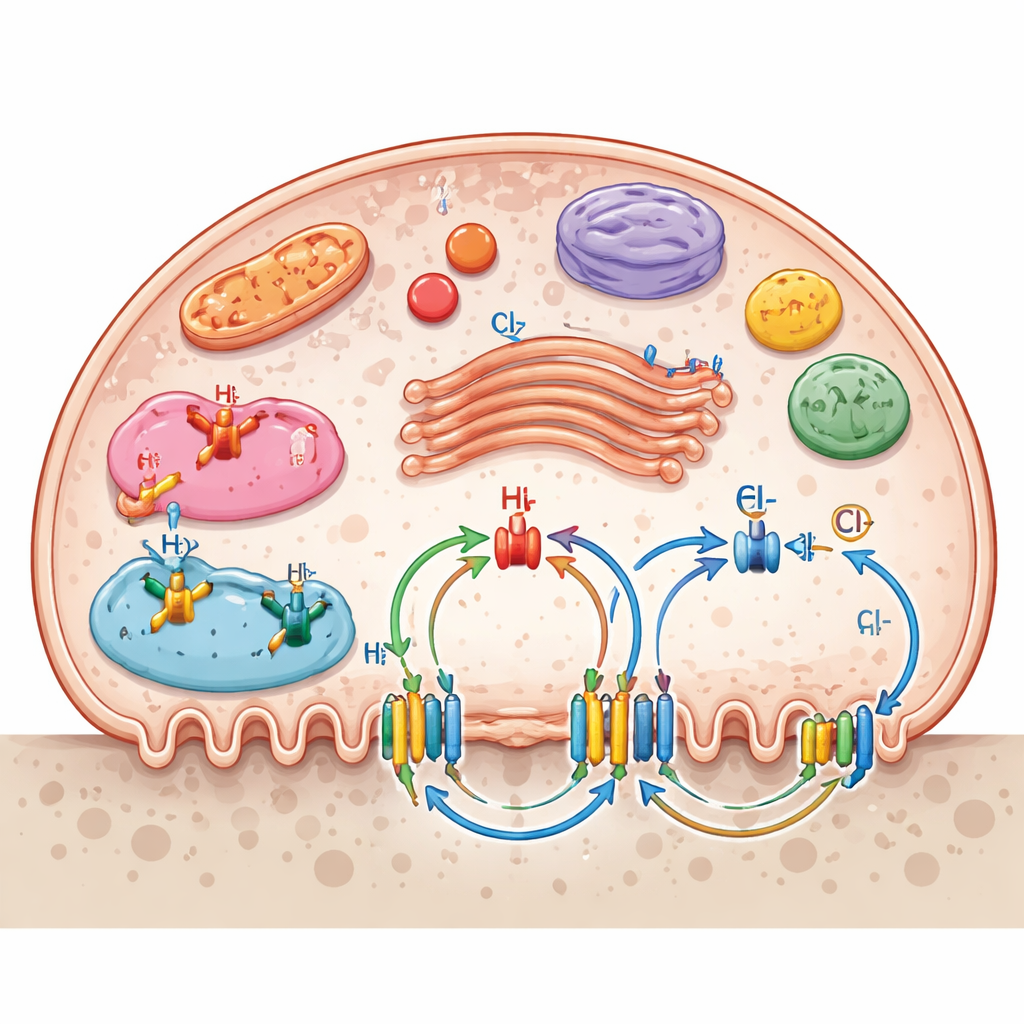
Von der Grundlagenbiologie zu neuen Therapien
Da viele Knochenerkrankungen entstehen, wenn Osteoklasten überaktiv oder unteraktiv sind, sind die Kanäle und Transporter, die ihr Verhalten lenken, attraktive Arzneimittelziele. Die Autoren besprechen bestehende und experimentelle Verbindungen, die V‑ATPasen, TRP‑Kalziumkanäle, Chloridaustauscher, purinerge Rezeptoren und andere Transporter blockieren, sowie neuere Ansätze wie die Störung spezifischer Untereinheiten‑Interaktionen oder den Einsatz zielgerichteter Nanopartikel zur direkten Medikamentenabgabe an den Knochen. Sie betonen, dass viele dieser Proteine auch in anderen Geweben vorkommen, sodass eine echte Osteoklast‑Spezifität weiterhin eine Herausforderung darstellt. Dennoch wird die sich erweiternde „Ionenkarte“ der Osteoklasten, die durch Genomik und bildgebende Verfahren zunehmend präzisiert wird, voraussichtlich präzisere Therapien für Osteoporose, entzündlich bedingten Knochenabbau und seltene genetische Knochenerkrankungen ermöglichen.
Zitation: Chen, H., Zhang, Y., Zhu, Y. et al. Spectrum and functions of ion channels and transporters in osteoclasts. Bone Res 14, 35 (2026). https://doi.org/10.1038/s41413-026-00513-9
Schlüsselwörter: Osteoklasten, Ionenkanäle, Knochenresorption, V-ATPase, Osteoporose